Пирофосфатная артропатия: что это такое, симптомы и лечение, пирофосфат кальция, диагностика и клинические рекомендации
Организм человека – сложный саморегулирующийся и саморазвивающийся механизм. Эта система едина и все процессы, протекающие в ней, взаимосвязаны между собой. Поэтому нарушение работы какого-либо одного биологического процесса может привести к серьезным патологическим изменениям во всем организме.
Зачастую именно сбои в обмене веществ приводят к развитию различных заболеваний, в том числе и патологиям опорно-двигательного аппарата (ОДА). Одна из таких болезней — пирофосфатная артропатия. Что это такое, как проявляется и какими способами лечится – обо всем этом далее в статье.
Что такое пирофосфатная артропатия
Пирофосфатная артропатия – суставное заболевание, обусловленное формированием и накоплением в соединительной ткани вещества – пирофосфата кальция.
Справка. В МКБ-10 заболевание находится в группе М11 «Другие кристаллические артропатии».
В большинстве случаев патология поражает организм людей пожилого возраста. Частота возникновения у мужчин и женщин практически одинаковая.
Заболевания разделяется на несколько клинических форм:
- псевдоподагрическая (25% всех случаев) – наблюдаются острые, либо подострые приступы псевдоподагры. Чаще поражаются коленные суставы, но может распространиться и на прочие крупные суставы ног;
- псевдоартрозная (50%) – отличается хроническим течением. Симптомы и результаты диагностики напоминают артроз;
- псевдорематоидная (5%) – симптоматика схожа с течением ревматоидного артрита. Редко поражается один сустав, чаще патология распространяется на соседние крупные и мелкие суставы;
- деструктивная (20%) – прогрессирующее течение патологического процесса, сопровождающееся тяжелыми поражениями костей и околосуставных тканей;
- латентная (точный процент заболеваемости не установлен) – характеризуется бессимптомным течением и выявляется случайно при проведении рентгенографии.
В некоторых случаях может наблюдаться комбинация из вышеперечисленных форм, что значительно усложняет диагностирование и терапию.
Причины появления и механизм развития
Причины возникновения патологии медицине неизвестны. Однако принято разделять ее на две формы: первичную и вторичную.
Первичная форма заболевания связана с наследственной предрасположенностью и диагностируется у нескольких членов семьи. Эта форма наблюдается практически в 90% всех клинических случаев.
Вторичная форма развивается на фоне заболеваний, сопровождающихся нарушением процессов обмена:
- гемохроматоз – генетическое заболевание, характеризующееся ускорением всасывания железа в пищеварительном тракте;
- гипофосфатазия – снижение активности щелочной фосфатазы и минерализация костной ткани;
- первичный гиперпаратиреоз – поражение эндокринной системы, при котором в результате сбоя обменных процессов наблюдается стимуляция выделения кальция из костной ткани в кровь;
- патология Коновалова-Вильсона – наследственная болезнь, характеризующаяся накоплением магния в крови и внутренних органах из-за сбоя в процессе его выведения;
- гипомагнезиемия – снижение уровня магния в крови.
К факторам риска относятся травматические повреждения, повышенные нагрузки, пожилой возраст.
Основа механизма возникновения кроется в нарушении метаболизма кальция.
Справка. Пирофосфат кальция – соль неорганического происхождения, которая присутствует в организме.
Если нарушается процесс выведения этой соли, она начинает скапливаться в тканях гиалинового хряща. Кристаллы объединяются в обширные образования. При их прорастании в ткани хряща происходит растрескивание и формирование остеофитов на костях.
Образованные кристаллы проникают в синовиальную жидкость, где их концентрация непостоянна. Так, перед обострением уровень микрокристаллов во внутрисуставной жидкости резко увеличивается, после чего постепенно снижается.
Симптомы
Пирофосфатная артропатия – хроническая болезнь, при которой периоды обострения сменяются периодами ремиссии.
Справка. Обострение длится от нескольких дней до двух-трех недель.
Симптоматика разнообразна и зависит от формы заболевания.
Общие проявления болезни:
- боль различной выраженности;
- припухлость в зоне больного сустава;
- покраснение кожного покрова;
- слабость;
- озноб, повышение температуры тела;
- ухудшение функционирования пораженной конечности;
- чувство скованности по утрам.
Зачастую происходит поражение суставов кисти, плеч, коленей. Количество пораженных суставов зависит от вида и стадии заболевания.
Методы диагностики
Диагностика болезни – сложный процесс, поскольку пирофосфатная артропатия проявляется приступами, схожими с артритом, артрозом, подагрой.
Важно! Диагноз «пирофосфатная артропатия» ставится только в том случае, если в ходе обследования в суставных отделах были обнаружены кристаллы пирофосфата кальция.
В ходе обследования применяются следующие диагностические методы:
- опрос и осмотр – определяются визуальные отклонения, характер симптомов, их выраженность, время проявления;
- рентгенография – точный способ диагностирования заболевания. Позволяет определить кальцификацию гиалинового хряща. На снимке это выглядит как узкая линейная тень. Она повторяет контуры суставных поверхностей;
- исследование внутрисуставной жидкости – биологическая жидкость внутри пораженного сустава становится насыщенного желтого цвета. При лабораторном анализе выявляется наличие микрокристаллов кальция пирофосфата;
- общий и биохимический анализ крови – проводится для получения сведений об общем состоянии организма и протекающих в нем процессах;
- МРТ и КТ – назначаются при наличии сопутствующих заболеваний;
- анализы на выявление сывороточного уровня кальция, магния, железа, фосфора, гормонов щитовидной железы – для определения возможного наличия метаболических нарушений.
В некоторых случаях требуется консультация ревматолога, эндокринолога и прочих специалистов.
Методы лечения
Симптомы и лечение пирофосфатной артропатии взаимосвязаны. Только полная клиническая картина позволит назначить адекватную терапию и добиться положительных результатов.
Справка. Цели – снижение болевого синдрома и терапия сопутствующей патологии.
Основа лечения — консервативные методики. Стандартная схема включает следующие терапевтические способы:
- Снижение нагрузки на пораженные суставы – по возможности ограничить передвижение, не носить тяжести.

- Ортопедический режим – рекомендуется использовать ортезы, бандажи для фиксации и поддержания пораженной области. Модель подбирается врачом.
- Диета – позволяет в значительной степени уменьшить число периодов обострения заболевания. Рекомендуется питаться дробно четыре-пять раз в день. Пища должна быть приготовленной на пару или в духовке. Запрещено употреблять сдобу, сладкое, бульоны, бобовые, соленья, копченые, острые блюда, алкоголь, чай, кофе. Рекомендуется обогатить рацион постным мясом и рыбой, кисломолочными продуктами, фруктами, овощами, орехами, сухофруктами, вегетарианскими супами, кашами, фруктовыми соками.
- Снижение массы тела – для предотвращения избыточной нагрузки на суставы.
- Медикаментозное лечение – назначаются различные препараты, обладающие разносторонним воздействием на организм.
- Физиотерапия – процедуры назначаются после преодоления острого периода. Способствуют нормализации обменных процессов и кровообращения, снижению выраженности боли и воспаления.
- Массаж – назначается в период ремиссии. Улучшает кровообращение, питание тканей, нормализует тонус мышц.
- ЛФК – комплекс упражнений подбирается строго специалистом. Предназначен для улучшения микроциркуляции крови, улучшения функционирования суставов, повышения подвижности, укрепления мышечно-связочного аппарата.
Если пирофосфатная артропатия вызывает тяжелую деформацию сустава с нарушением его функционирования, то назначается хирургическое вмешательство. Основной метод – эндопротезирование (замена пораженного сустава искусственным имплантатом).
Медикаменты
Специфических лекарственных средств для лечения данного заболевания не разработано, поскольку полностью не выяснены точные причины и механизм его развития.
Клинические рекомендации для проведения медикаментозной терапии заключаются в применении препаратов различных лекарственных групп, направленных на снятие обострения и улучшение самочувствия больного:
- НПВС («Диклофенак», «Ацеклофенак», «Ибупрофен») – для снятия боли и воспаления во время острого течения патологии.

- Противоподагрические средства («Колхицин») – применяются в начале острого приступа псевдоподагры.
- Глюкокортикостероиды («Дипроспан») – вводятся внутривенно или внутрисуставно. Применяются при тяжелом течении патологии, сопровождающейся интенсивной болью и воспалением.
- Органопрепараты («Румалон») – для нормализации нарушенного обмена веществ в хрящевой ткани и стимуляции ее регенерации.
- Метаболические средства («Натрия аденозитрифосат») – для улучшения процессов метаболизма и питания тканей.
- Витаминно-минеральные комплексы («Компливит», «Витрум») – для восполнения запасов организма необходимыми веществами.
- Витаминные комплексы группы В («Мильгамма», «Витагамма») – назначаются для поддержания нормального функционирования нервно-мышечной передачи.
Комбинация необходимых препаратов подбирается специалистом исходя из формы заболевания, тяжести его течения, индивидуальных особенностей организма больного.
Физиотерапия
Физиотерапевтическое лечение применяется после купирования острой симптоматики и стабилизации состояния.
Назначаются следующие физиотерапевтические процедуры:
- радоновые ванны – воздействие на организм при помощи минеральной воды, обогащенной радоном;
- сероводородные ванны – вид бальнеотерапии, который заключается в применении минеральной воды, насыщенной сероводородом;
- грязелечение – использование лечебных свойств грязей минерального и органического происхождения.
Все эти процедуры способствуют улучшению обмена веществ, нормализации кровообращения, устранению боли, а также обладают рассасывающим эффектом.
Также для предотвращения повторных приступов рекомендуется регулярно проходить лечение в санаторно-курортных учреждениях, специализирующихся на лечении суставных болезней.
Заключение
Лечение пирофосфатной артропатии имеет относительно благоприятный прогноз. Своевременная терапия позволяет остановить развитие патологии. При этом почти в половине клинических случаев происходит существенное улучшение самочувствия пациентов. Однако у многих больных случаются рецидивы. Это связано с тем, что полностью вывести из организма избыток пирофосфата кальция невозможно.
Что такое пирофосфатная артропатия – симптомы, диагностика, лечение
Пирофосфатная артропатия – это заболевание суставов, которое возникает в том случае, когда в них откладывается пирофосфат кальция дигидрата. Чаще всего такая проблема встречается у людей старше 45 лет. Существует три вида пирофосфатной артропатии:
Пирофосфатная артропатия- Первичная. Возникает как самостоятельное заболевание.
- Вторичная. Это заболевание возникает в качестве осложнения других болезней и травм.
- Генетическая. Это заболевание передается по наследству в основном по мужской линии.
Содержание страницы
Причины
Точная причина возникновения заболевания неизвестна, но оно часто возникает, если есть наследственная предрасположенность. Отложение кристаллов кальция может быть связано с другими заболеваниями, например сахарным диабетом или остеоартрозом.К тому же, в пожилом возрасте в организме нарушаются обменные процессы и ферментов, расщепляющих кальция дигидрат вырабатывается недостаточно.
Спровоцировать заболевание может хирургическая операция, тяжелые заболевание, например инфаркт или инсульт, травмы различного характера и тяжести.
Симптомы заболевания
Боли в суставах – симптомы артропатииЗаболевание может протекать бессимптомно, особенно в пожилом возрасте и проявляться только на рентгеновских снимках. В случаях, когда болезнь проявляет себя, наблюдаются такие симптомы, как:
- Появляется резкая, постоянная и сильная боль в коленном суставе ( в редких случаях в любом другом), которая сопровождается отечностью, покраснением. Болеть могут оба колена сразу.
- Длительность приступа может составлять несколько недель и сопровождаться повышением температуры, ознобом.
- Постепенно состояние ухудшается, поражаются другие суставы.
- Суставы разрушаются незаметно для пациента, так как боль в период приступа достаточно интенсивная.
Диагностика
Для диагностики и последующего лечению пациенту нужно обратиться к терапевту и ревматологу. Ревматолог на первом приеме опрашивает больного, составляет анамнез и назначает ряд необходимых анализов, по итогам которых и ставит диагноз.
Диагностика артропатииВ первую очередь пациенту назначают исследование синовиальной жидкости. Это вещество, которое заполняет сустав, в норме его умеренное количество. При пирофосфатной артропатии жидкость становится желтого оттенка, похожего на гной, а при изучении в лаборатории в ней обнаруживают кристаллы кальция, размером 20 мкм и лейкоциты.
Также назначается анализ крови, по которому врач может определить, насколько сильно сустав подвержен воспалению. О воспалительном процессе говорит повышенное содержание лейкоцитов и большая скорость оседания эритроцитов. Кроме того, врач назначает рентген – самый достоверный метод, на котором отчетливо видно отложение кристаллов.
Лечение
Лечение обычно назначается комплексное:
- медикаментозное;
- физиотерапия;
- ЛФК.
Пациенту рекомендуется соблюдать покой, врач назначает холодные компрессы для снятия отека, линю суставную жидкость удаляют. Для снятия воспаления назначаются нестероидные противовоспалительные препараты, например диклофенак.
Если заболевание проходит тяжело и сопровождается сильной болью, пациенту назначают постоянное применение обезболивающих препаратов. Ацеклофинак – одно из самых эффективных и безопасных в этом случае средств.
После того, как приступ проходит, пациенту назначают физиолечение. Также рекомендуется употреблять витамины, заниматься лечебной физкультурой, но пораженные суставы сильно нагружаться нельзя, так как они подвержены разрушению.
Профилактика
В качестве профилактики приступа рекомендуется не нагружать сустав. К сожалению, предупредить болезнь полностью невозможно, так как не известны точные причины ее возникновения.
Профилактика артропии – здоровый образ жизниВажно! Чтобы снизить риск пирофосфатной артропатии, нужно вести здоровый образ жизни, придерживаться правильного питания и не перегружать суставы, но ежедневная гимнастика необходима.
Как питаться при пирофосфатной артропатии
Правильно подобранное питание играет важную роль в профилактике и лечении любых заболевания, особенно связанных с суставами. Злоупотребление жирной едой приводит к лишнему весу и увеличению нагрузки на пораженные суставы, провоцируя их разрушение.
При пирофосфатной артропатии питаться нужно дробно, не менее 5 раз в день, маленькими порциями. Еда должна быть полезной и низкокалорийной. Необходимо ограничить потребление соли, вся пища должна казаться немного недосоленной.
Разрешенные продукты:
- постное мясо, рыба, субпродукты;
- сезонные овощи и фрукты;
- крупы и макароны;
- молочные и кисломолочные продукты;
- орехи, ягоды, сухофрукты.
Запрещенные продукты:
- блюда быстрого приготовления, полуфабрикаты;
- соленья;
- копченые и острые продукты;
- жареное, жирное;
- сладкое.
Всю еду рекомендуется варить, запекать или готовить на пару.
Народные методы лечения
Облегчить боль при пирофосфатной артропатии помогут рецепты народной медицины.
- Мазь. 1 ч.л. скипидара, куриный желток, 1 ст.л. яблочного уксуса необходимо смешать и втирать в больной сустав дважды в день.
- Прополис. Хорошим противовоспалительным действием обладает прополис, из него необходимо делать примочки. Для этого чистую ткань кладут в улей на зиму, весной ее вынимают и используют в качестве примочек.
Пирофосфатная артропатия: симптомы, признаки, диагностика и лечение
Описание
Пирофосфатная артропатия — ревматологическое заболевание, которое вызывается отложением в полости суставов пирофосфата кальция дигидрата.

В медицине принято выделять три формы пирофосфатной артропатии: первая форма – генетическая (самая тяжелая), вторая форма – вторичная пирофосфатная артропатия, и третья форма – первичня пирофосфатная артропатия.
Генетическая пирофосфатная артропатия передается по наследству генетическим путем, чаще всего по мужской линии. Клиническая картина при этой форме заболевания достаточно яркая и своеобразная.
Вторичная пирофосфатная артропатия – это осложнения или побочное действие других патологий (в основном в области желез внутренней секреции). Механизмы развития вторичной формы артропатии пирофосфатной на сегодняшний день в медицине не установлены.
Первичная пирофосфатная артропатия – это самостоятельная патология, причины которой тоже пока не выявлены и не установлены. Во время ее развития нарушается работа ферментов, отвечающих в организме за преобразования пирофосфата кальция дигидрата.
Симптомы
В зависимости от формы течения болезни клиническая картина может быть разнообразной.
Форма течения пирофосфатной артропатии - псевдоостеоартроз – поражает тазобедренные, коленные и лучезапястные суставы. Одновременно поражение захватывает от двух до четырех суставов. При этом больной жалуется на боли в пораженных суставах во время длительных физических нагрузках (особенно во время долгого стояния). Визуально проявляется только небольшая припухлость и сниженная двигательная способность пораженного сустава.
Псевдоподагра – еще одна форма течения данного заболевания – начало развития внезапное, приступообразное и с резкими болями. Поражение при этом обычно захватывает коленные суставы, где больной ощущает боли. Кожные покровы над пораженными суставами краснеют, болезненность возникает при любом, даже самом незначительном движении. Более того, в этой форме течения артропатии может повышаться температура тела.
Псевдоревматоидный артрит – третья форма течения заболевания – это воспалительные процессы в малых суставах кистей и стоп. Своей симптоматикой эта форма крайне схожа с ревматоидным артритом.
Псевдонейропатическая форма течения пирофосфатной артропатии проявляется так же как врожденные неврологические болезни, а в суставах выявляются деструктивные процессы.
И последняя форма течения данного заболевания – моноформа. При ней поражение наступает, как правило, в одном суставе, коленном. И главным ее проявлением является потеря подвижности пораженного сустава.
Диагностика
Диагностируется пирофосфатная артропатия исключитиельно на основании лабораторных исследований. Проводится общий клинический анализ крови, в котором, в остром периоде болезни, явно видны признаки воспаления – крайне высокий уровень численности лейкоцитов и высокая скорость оседания эритроцитов.

Затем проводится исследование суставоной жидкости, в которой выявляют кристаллы пирофосфата кальция.
Профилактика
Артропатия пирофосфатная не имеет профилактических разработок и методик, поскольку в медицине не установлены причины ее развития. Но, стоит заметить, что в любой форме течения это заболевание никогда не угрожает жизни человека.
Лечение
Лечение пирофосфатной артропатии является симптоматическим. Назначаются противовоспалительные препараты, при острых приступообразных болях, в больших дозировках.
Так же в тяжелых случаях заболевания, при поражениях более двух суставов назначаются гормоны коры надпочечников.
Когда основные симптомы сняты, пациента направляют на санаторное лечение.
Пирофосфатная артропатия: что это, причины, симптомы и лечение
Пирофосфатная артропатия относится к микрокристаллическим артритам. О данном диагнозе стало известно еще в 10 веке. Появляется в виде псевдоподагры или хронической артропатии.
Является довольно распространенной патологией. Среди взрослых людей такой диагноз имеют около 5% населения. С возрастом вероятность развития заболевания увеличивается и среди пожилых людей пирофосфатной артропатией страдают 27%. У молодых людей и детей такое заболевание не выявляется.
Механизм развития
Заболевание появляется из-за отложения пирофосфата кальция в синовиальной сумке или хряще. Это напоминает слияние маленьких жемчужин в большое образование. При микроскопическом исследовании кристаллы образуют форму ромба или треугольника. Это является главной отличительной чертой от мононатриевого урата, который при микроскопическом исследовании напоминает форму иглы.
Причины
Конкретная причина заболевания не установлена и по сей день. Однако выделены факторы риска, которые, по мнению ученых, способствуют развитию пирофосфатной артропатии:
- Пожилой возраст (старше 55 лет)
- Отягощенная наследственность.
- Травмы суставов.
- Гемохроматоз.
- Заболевания эндокринной системы.
- Синдром Гительмана.
- Гиперкалиемия.
- Гипотиреоидизм.
Людям, имеющим данные факторы риска, рекомендуется следить за своими суставами.
Формы
Официально выделено три формы заболевания: генетическая, первичная и вторичная.
Генетическая форма передается по наследству, чаще по мужской линии. Является наиболее тяжелой формой, имеет своеобразные симптомы и яркую клиническую картину.
Первичная форма развивается самостоятельно и причина ее появления не выявлена. Происходит сбой в работе ферментов, которые отвечают за преобразование пирофосфата кальция дегидратата.
Вторичная форма появляется в виде осложнения уже имеющейся патологии. Причины появления также не выяснены, но предположительно появляется из-за патологий желез внутренней секреции.
Клиническая картина и варианты течения
У пирофосфатной артропатии не имеется специфических симптомов. В основном ее клинические проявления легко перепутать с другими заболеваниями суставов. Имеется три варианта течения: псевдоподагра, псевдоостеоартроз и псевдоревматоидный артрит. Во всех случаях имеется подагрический приступ, который проявляется следующими симптомами:
- Опухолью.
- Болевым синдромом.
- Лихорадкой с повышением температуры.
- Ознобом.
- Недомоганием.
Чаще поражаются коленные суставы и суставы большого пальца стопы. Иногда болевой синдром достаточно сильный и пирофосфатную артропатию часто путают с септическим артритом.
Псевдоподагра
Данный вариант течения имеет большое сходство с подагрой. Характеризуется периодическими приступами боли и отеком сустава. Чаще поражается один сустав, преимущественно коленный. От подагры отличается длительностью периода обострения. В это время появляется не только недомогание, но и повышение температуры тела.
Приступ обострения длится около трех недель. После него все симптомы исчезают. Причиной обострения могут служить травмы, операции, инфаркт и друге заболевания.
Псевдоостеоартроз
У половины пациентов, имеющих пирофосфатную артропатию, имеется клиническая картина, напоминающая остеоартроз. Поражается несколько крупных суставов. Боль умеренная, но постоянная. Из-за этого возникают короткие приступы псевдоподагры. В период обострения имеется скованность движений.
Псевдоревматоидный артрит
Достаточно редкая форма пирофосфатной артропатии и выявляется у 5% пациентов. Иногда заболевание путают с ревматоидным артритом, так как поражаются симметричные суставы. Появляется припухлость, болевой синдром и отечность. Поражается множество суставов одновременно. Клиническая картина не такая яркая, как при других формах и может держаться на протяжении нескольких месяцев.
Диагностика
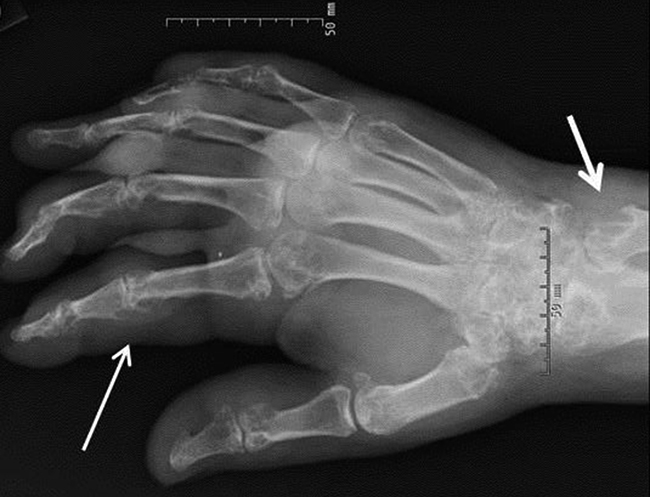
Диагноз выставляется на основе инструментальных и лабораторных данных. Главным методом является рентгенография суставов. При обследовании выявляется двухконтурность кости. Если заболевание имеет наследственный характер, то такое изменение на снимке может быть замечено даже на маленьких суставах.
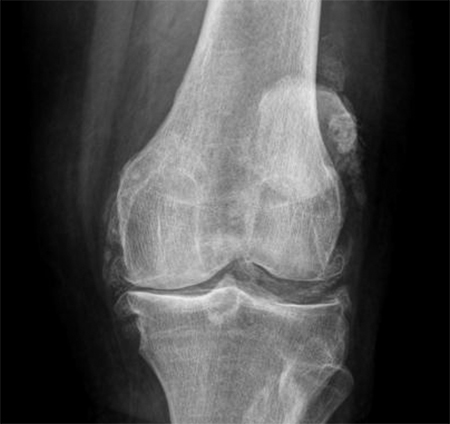
Для уточнения диагноза необходимо исследование синовиальной жидкости. По внешнему виду она напоминает гной и имеет желто-белый цвет. С помощью микроскопа можно выявить большое количество кристаллов кальция и лейкоцитов. Кристаллы кальция имеют форму ромба.
Общий анализ крови не имеет специфических показателей, касающихся данного заболевания. Однако с помощью него можно выявить, насколько сильно выражен воспалительный процесс. В таком случае будет значительное повышение СОЭ и лейкоцитов.
Лечение
Так как причина не выяснена, то специфического лечения не разработано. Проводится только симптоматическая терапия.
При приступе назначается Колхицин. Однако начинает действовать он через длительное время, а предупредить приступы невозможно.
Для снятия болевого синдрома применяются нестероидные противовоспалительные препараты: Ортофен, Кетанов, Найз. Спустя 3-4 дня симптомы значительно уменьшаются.

Если прием НПВС не уменьшает болевой синдром, то в условиях стационара проводится введение глюкокортикостероидов. Они вводятся в полость сустава. Действуют достаточно быстро. Снимают болевой синдром и воспаление.
При хроническом течении заболевания используются следующие методы:
- Снижение нагрузки на сустав.
- Прием витаминных комплексов.
- Массаж и физиотерапия.
При сильной деформации сустава может проводиться хирургическое лечение.
Диета
Важным пунктом в лечении пирофосфатной артропатии является диета. Назначается диета №10, которая улучшает обмен веществ. Ограничивается количество углеводов, жиров, соли, а также жидкости.
Рекомендуется употреблять:
- Овощные супы.
- Мясо и рыбу нежирных сортов.
- Яйца.
- Макароны.
- Молочные продукты.
- Зеленый чай.
Запрещено употреблять:
- Жирные бульоны.
- Жирные сорта мяса и рыбы.
- Сдобные хлебобулочные изделия и сладости.
- Алкоголь.
- Крепкий кофе и чай.
- Соленые продукты, пряности, специи.
Соблюдение диеты способствует улучшению результатов лечения.
Профилактика
Специфической профилактики заболевания не существует. При появлении артропатии есть ряд мероприятий, которые помогут уменьшить вероятность появления приступов:
- Снижение нагрузок на сустав.
- Ношение удобной обуви.
- Самомассаж сустава.
- Устранение лишнего веса при его наличии.
Также после 40 лет следует регулярно проходить профилактические осмотры.
Прогноз
При своевременной диагностике и лечении прогноз благоприятный. В запущенных случаях заболевание приводит к инвалидности. В таком случае требуется хирургическая операция. Однако она требуется только 10% пациентов.
Похожие материалы:
 Артропатия: что это, классификация, симптомы и лечение
Артропатия: что это, классификация, симптомы и лечение Реактивная артропатия: что это, классификация, симптомы и лечение
Реактивная артропатия: что это, классификация, симптомы и лечение Малая хорея: что это, причины, симптомы и лечение
Малая хорея: что это, причины, симптомы и лечение Перелом мизинца на ноге: симптомы, диагностика и лечение
Перелом мизинца на ноге: симптомы, диагностика и лечение Артроз височно-нижнечелюстного сустава: симптомы, диагностика и лечение
Артроз височно-нижнечелюстного сустава: симптомы, диагностика и лечение Мелоксикам: инструкция по применению, аналоги, отзывы
Мелоксикам: инструкция по применению, аналоги, отзывы Метотрексат: показания, инструкция по применению, отзывы
Метотрексат: показания, инструкция по применению, отзывы Остеоартрит: что это, причины, симптомы и лечение
Остеоартрит: что это, причины, симптомы и лечение
Диагностика Пирофосфатной артропатии:
Рентгенологические изменения при ПФА достаточно изучены. Наиболее характерным признаком является кальцификация суставного гиалинового хряща (хондрокальциноз) в виде нежной, линейной тени, повторяющей контуры суставной поверхности (двойной контур сустава). При поражении коленных суставов эти изменения сопровождаются более грубой кальцификацией менисков в виде небольших треугольников в боковых частях межсуставной щели (снимок в прямой проекции) (рис. 46). Обнаруживаются также очаговые точечные кзльцификаты в области синовиальной оболочки и капсулы. Кальцификаты могут быть и в периартикулярных тканях, сухожилиях и мышцах, а также в крестообразных связках коленного сустава. Они обычно множественные и симметричные, сопровождаются дегенеративными изменениями сустава, идентичными артрозу, нередко локализующемуся в лучезапястном и пястнофаланговом суставах. Наиболее часто дегенеративные изменения развиваются в феморопателлярном суставе. Следует помнить, что при значительной костнохрящевой деструкции кальцификация может исчезнуть, и наоборот, в некоторых случаях она обнаруживается на рентгенограмме у больных, не имеющих клинических проявлений ПФА.
Весьма характерный симптом ПФА — поражение кисти. На рентгенограммах обнаруживают кальцификацию суставов запястья (в 60% случаев), кальцификацию треугольной связки запястья (в 52%) и пястнофаланговых суставов (в 22%). Очень часто в суставах запястья и лучезапястном суставе выявляются признаки дегенеративной артропатии (сужение суставной щели, уплотнение субхондральной кости, субхондральные кисты), что может указывать на возможность развития этого заболевания даже без видимой кальцификации. Дегенеративные изменения (включая остеофиты) могут обнаруживаться и в проксимальных пястнофаланговых суставах.
Поражение коленного и тазобедренного суставов наблюдается в 52 % всех случаев ПФА. При этом поражение тазобедренного сустава часто сопровождается кальцификацией симфиза в виде плотной линии посредине этого сочленения. В 25 % случаев не обнаруживается поражение плечевого сустава.
Поражение позвоночника также наблюдается часто. В процесс вовлекается главным образом периферическое фиброзное кольцо. И только при семейных формах кальцифицируется весь диск (как при охронозе).
Диагноз ПФА можно поставить на основании двух характерных признаков: множественной кальцификации суставного хряща на рентгенограмме — хондрокальциноза и наличия кристаллов пирофосфата кальция в синовиальной жидкости, синовиальной оболочке и хряще. Каждый из этих признаков характерен только для ПФА и подтверждает диагноз даже при отсутствии другого признака.
Так, кальцификация хряща может отсутствовать в ранней стадии болезни, когда отложения кальция еще небольшие, а также при деструктивных формах, когда суставной хрящ почти полностью разрушен. В этих случаях диагноз подтверждается исследованием синовиальной жидкости, в которой обнаруживаются маленькие прямоугольные или квадратные кристаллы, слабо светящиеся в поляризационном свете. В неясных случаях кристаллы можно обнаружить при микроскопировании биоптатов синовиальной оболочки и хряща.
Выявление на рентгенограмме изолированной кальцификации (например, только мениска коленного сустава или отдельных кальцификатов в мягких тканях) не позволяет говорить о хондрокальцинозе, так как подобная кальцификация обусловлена кальциевой солью, отличающейся от пирофосфата. Наличие на рентгенограмме характерной множественной кальцификации суставных тканей позволяет поставить диагноз ПФА даже при отсутствии видимых кристаллов пирофосфата в синовиальной жидкости.
Часто труден, поскольку ПФА может носить маску подагры, острого септического артрита и деформирующего остеоартроза.
Клиническая картина и течение болезни могут быть такими же, как при подагре. Поэтому первоначально обычно ставят диагноз подагры. Однако при повторных исследованиях крови обнаруживают нормальное содержание мочевой кислоты, а при исследовании синовиальной жидкости находят кристаллы не урага натрия, а пиршросфаш кальция. Внимагельное изучение рентгенограмм нескольких суставов позволяет выявить кальцификацию суставных тканей (иногда очень слабо различимую), что подтверждает диагноз ПФА.
При остром приступе болезни, особенно при моноартрите крупного сустава, иногда можно подозревать септический артрит. В этих случаях имеют значение наличие у больного подобных же приступов в прошлом, довольно быстрое течение приступа с полным обратным развитием всех суставных явлений, отсутствие «септических» сдвигов в крови, заметного влияния антибиотиков, а также характерные изменения на рентгенограммах.
При пирофосфатной псевдоартрозной артропатии развивается картина, чрезвычайно схожая с деформирующим остеоартрозом и с идентичными признаками на рентгенограмме (сужение суставной щели, субхондральный остеосклероз, остеофиты). Однако локализация поражения кисти иная. Характерное для ПФА поражение мелких суставов запястья и пястнофаланговых суставов обычно отсутствует при артрозе, для которого типично поражение главным образом дистальных и проксимальных межфаланговых суставов. Эти заболевания можно различать следующим образом: при ПФА на фоне хронической артропатии в 50 % случаев наблюдаются псевдоподагрические приступы, тогда как при артрозе может быть небольшой реактивный синовит, развивающийся лишь после перегрузки сустава, быстро исчезающий в покое. При подозрении на ПФА следует внимательно изучить рентгенограммы нескольких суставов для выявления диффузной кальцификации (при поражении кисти, особенно в области треугольной связки запястья и пястнофаланговых суставов), а также исследовать синовиальную жидкость на наличие в ней кристаллов пирофосфата, что и решает диагноз. Следует помнить также о возможности сочетания этих заболеваний.
Сочетание подагры и болезни депонирования пирофосфатов кальция: трудности диагностики и лечения | Елисеев М.С., Желябина О.В.
В статье рассмотрены трудности диагностики и лечения сочетания подагры и болезни депонирования пирофосфатов кальция. Описано применение современных методов диагностики. Обсужден подбор адекватной противовоспалительной терапии при остром, в т. ч. часто рецидивирующем, артрите у пациента с учетом противопоказаний и сопутствующих заболеваний.
Микрокристаллические артриты – группа заболеваний, обусловленных воспалением в местах отложения образующихся in vivo кристаллов. К ним относятся заболевания с принципиально различной этиологией и патогенезом. И хотя провоспалительный потенциал для различных кристаллов отличается (кристаллов моноурата натрия, пирофосфата кальция, гидроксиапатита и др.), все они клинически могут проявляться острым воспалением, чаще артритом или периартикулярным поражением одного или нескольких суставов. Наиболее часто микрокристаллические артриты вызываются кристаллами уратов (подагра) и пирофосфата кальция (болезнь депонирования пирофосфатов кальция (БДПК)).Подагра является наиболее частой причиной артритов у взрослых, не реже, по крайней мере в пожилом и старческом возрасте, выявляется БДПК. Клиническая картина БДПК нередко напоминает подагру – примерно в четверти случаев клинически она проявляется острыми приступами артрита, практически неотличимыми от таковых при подагре, полностью оправдывая один из исторических вариантов названия заболевания – «псевдоподагра» [1]. Кроме того, возможно сочетание двух заболеваний, что значительно затрудняет не только диагностику, но и подбор терапии [2–4]. Более того, по некоторым данным, подагра может быть также фактором риска развития БДПК [5].
Эпидемиологических исследований сочетания подагры и БДПК не проводилось. Однако в клинической практике сочетание двух микрокристаллических артритов – довольно частое явление [3, 6]. Ниже приведен клинический случай выявления у пациента двух микрокристаллических артритов.
Пациент Е., 56 лет, дебют заболевания в 2011 г. с развития острого олигоартрита (1-го плюснефалангового и голеностопного суставов). Артрит купировался самостоятельно в течение 8 дней. В последующем отмечались рецидивы артрита 1-х плюснефаланговых, голеностопных, предплюсны с частотой до 3–4 раз в год, при обострении с успехом применял НПВП (диклофенак натрия в/м). Уровень мочевой кислоты (МК) стойко превышал 500 мкмоль/л. С 2014 г. – резкое учащение частоты приступов (ежемесячно), стали вовлекаться коленные суставы, применение диклофенака стало менее действенным, потребность в нем увеличилась. Тогда же появились боли в эпигастрии после приема пищи, по результатам эзофагогастродуоденоскопии впервые выявлен эрозивный гастрит. Вскоре (в ноябре 2014 г.) был консультирован в ФГБНУ НИИР им. В.А. Насоновой, где был верифицирован диагноз подагры, подтвержденный результатами поляризационной микроскопии, выявившей кристаллы моноурата натрия в синовиальной жидкости. Сывороточный уровень МК составил 585 мкмоль/л. После купирования артрита была инициирована уратснижающая терапия – аллопуринол в стартовой дозе 100 мг/сут с последующим постепенным увеличением до 600 мг/сут, к апрелю 2015 г. был достигнут целевой уровень МК (360 мкмоль/л). Низкий сывороточный уровень МК, не превышающий целевой, сохранялся и в дальнейшем. Приступы артрита сохранялись вплоть до июня 2015 г., от профилактики приступов и противовоспалительной терапии воздерживался, т. к. прием НПВП приводил к возникновению болей в эпигастральной области.
В декабре 2015 г., при сохраняющейся нормоурикемии, было отмечено последовательное развитие артритов коленных, затем плечевых суставов, суставов кистей. Пациент самостоятельно принимал НПВП (эторикоксиб 120 мг), боли уменьшались, но при этом происходило неконтролируемое повышение АД, требующее назначения антигипертензивной терапии. В апреле 2016 г. пациент повторно обратился в НИИ ревматологии с жалобами на боль, припухлость в плечевых, коленных суставах, суставах кистей. При осмотре были определены артриты проксимальных межфаланговых суставов обеих кистей, плечевого сустава справа, коленного сустава справа. Уровень МК сыворотки сохранялся стабильно ниже 300 мкмоль/л. C целью исключения дебюта ревматоидного артрита (РА) проведено иммунологическое исследование, по результатам РФ и АЦЦП – в норме, СРБ – 23 мл/мл, СОЭ –27 мм/ч, число болезненных суставов – 6, число припухших суставов – 4. В диагностический поиск был включен среди возможных и диагноз БДПК. В результате обследования проведена также рентгенография коленных суставов, выявившая типичные признаки БДПК (хондрокальциноз) (рис. 1).
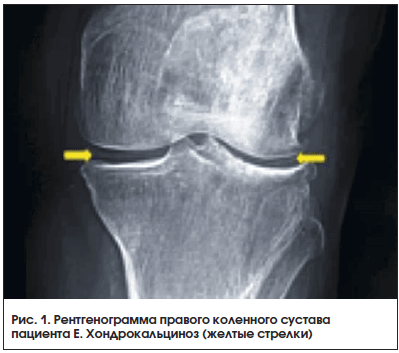
При повторном исследовании синовиальной жидкости были выявлены кристаллы пирофосфатов кальция, тогда как кристаллы моноурата натрия не определялись. Таким образом, был верифицирован диагноз второго микрокристаллического заболевания – БДПК. С целью купирования артрита пациенту был назначен колхицин в дозе 1 мг/сут, эффект расценен как недостаточный, повышение дозы до 1,5 мг/сут привело к выраженной диарее, потребовавшей отмены препарата. Несмотря на анамнестические данные о нежелательных явлениях при приеме НПВП (диклофенак – эрозивный гастрит, эторикоксиб – повышение АД), был назначен амтолметин гуацин (Найзилат) в суточной дозе 1200 мг (600 мг 2 р./сут). В течение 1 нед. артрит был полностью купирован, однако менее через 1 мес. развился рецидив артрита коленных суставов, прием Найзилата был возобновлен в прежней дозе, со столь же хорошим эффектом. После купирования приступа через 7 дней приема доза препарата была снижена до поддерживающей (600 мг/сут). При дальнейшем динамическом наблюдении на протяжении 6 мес. приступов артрита зарегистрировано не было, боли в суставах не беспокоили.
Обсуждение
Диагностика подагры и БДПК нередко вызывает затруднения – частое пересечение отдельных клинических симптомов у пациентов с микрокристаллическими артритами не позволяет выставить определенный диагноз только на основании клинической картины заболевания. Как правило, в начале болезни и подагра, и, нередко, пирофосфатная артропатия проявляются приступами острого артрита, характеризующимися сильнейшей болью, припуханием окружающих тканей, гиперемией и гипертермией кожного покрова над пораженным суставом, которые сменяются межприступными периодами. Кроме того, и подагра, и БДПК могут часто сочетаться как между собой, так и с другими ревматическими заболеваниями, что также затрудняет установление достоверного диагноза [3, 6–10].У данного пациента трудности при верификации диагноза БДПК возникли не только из-за наличия у него достоверного диагноза подагры, на который при желании можно было бы списать новые приступы артрита, но и из-за возможности симулирования БДПК еще одного ревматического заболевания – РА. Так, наличие стойких симметричных артритов суставов верхних конечностей, в т. ч. кистей, повышение сывороточного уровня СРБ потребовало включения в диагностический поиск РА. Однако число вовлеченных суставов не превышало шести, а мелких суставов кистей – двух; повышение уровня СРБ было незначительным (менее чем 2-кратным). И даже если брать за основу диагностические критерии АСR/EULАR, то диагноз РА выставлен быть не может [11–13].
Напротив, диагноз подагры сомнению не подлежал исходно, кроме того, был подтвержден выявлением кристаллов моноурата натрия в синовиальной жидкости, а после подбора уратснижающей терапии пациент находился в состоянии ремиссии (полное отсутствие клинических проявлений заболевания). При подагре это отсутствие приступов острого артрита может быть достигнуто только при достижении стойкой нормоурикемии, под которой подразумевается уровень МК менее 360 мкмоль/л [14].
Именно факт наличия стойкой нормоурикемии позволил предположить наличие второго заболевания, вызвавшего обострение. Решающее значение в диагностике этих заболеваний имело выявление соответствующих кристаллов в синовиальной жидкости [1, 15]. И если исчезновение кристаллов моноурата натрия объясняется стойкой нормоурикемией, при которой имеющиеся кристаллы рассасываются, то, напротив, появление кристаллов пирофосфата кальция связано с «выходом» их в синовиальную жидкость из постепенно разрушающегося хряща в достаточном количестве, т. к. насыщаемость ими синовиальной жидкости не столь велика. Таким образом, сочетание двух основных признаков БДПК: выявление кристаллов пирофосфата кальция в синовиальной жидкости и типичные признаки хондрокальциноза по результатам рентгенологического исследования суставов позволили выставить пациенту диагноз достоверной БДПК. При этом даже при отсутствии рентгенологических признаков хондрокальциноза диагноз БДПК этому пациенту не исключался бы, т. к. рентгенография обладает низким разрешением при выявлении небольших депозитов кристаллов. В этом отношении более информативным является УЗИ, использование которого для выявления депозитов кристаллов пирофосфатов кальция может быть дополнительным инструментом ранней диагностики (табл.1) [1, 16].

Другим вопросом, который предстояло решить, был выбор оптимальной симптоматической терапии. Несмотря на высокую частоту БДПК, полиморфизм симптомов, диктующий необходимость дифференцированного подхода к выбору оптимальной схемы терапии, исследования, посвященные изучению эффективности и безопасности лекарственных препаратов при БДПК, крайне малочисленны, а рандомизированные контролируемые исследования и вовсе отсутствуют. В то же время список лекарственных средств, применяемых при БДПК, достаточно широк: НПВП, колхицин, низкие дозы глюкокортикоидов, гидроксихлорохин, метотрексат, биологические агенты (ингибиторы интерлейкина 1) [17]. Согласно рекомендациям, при остром приступе возможно назначение НПВП, колхицина [1, 18]. Однако назначение колхицина в необходимых дозах вызывало у пациента развитие нежелательных явлений, ограничивающих его применение (как и использовавшиеся ранее НПВП).
Очевидно, что когда НПВП используются в течение короткого или относительно короткого времени, в большей степени важен контроль побочных эффектов, связанных с ЖКТ. Хорошо известно, что опасная патология ЖКТ (язвы, кровотечение, перфорация) может возникать в первые дни или даже часы после парентерального введения или перорального приема НПВП. В этом плане очень показательны данные финских исследователей A. Helin-Salmivaara et al., которые оценили зависимость риска развития ЖК-осложнений от длительности приема НПВП. Материалом для анализа стало популяционное исследование по типу «случай/контроль», в котором в основную группу был включен 9191 больной с ЖК-кровотечением, язвой или перфорацией, а в контрольную группу – 41 780 лиц без данной патологии. Оказалось, что опасность развития данных осложнений была максимальной в первые 2 нед. приема НПВП (ОШ 3,2), а затем существенно снижалась [19].
У данного пациента упорный рецидивирующий артрит обусловил необходимость постоянного приема НПВП, с одной стороны, обладающих достаточно выраженной противовоспалительной активностью, с другой – не вызывающих нежелательных явлений со стороны ЖКТ. Для лечения требовался препарат, который обладал бы анальгетической и противовоспалительной активностью традиционных представителей этой лекарственной группы, но не имел бы при этом свойственных им специфических недостатков. К сожалению, ни одно из предложенных на сегодня решений этой проблемы нельзя признать идеальным [20].
Наш выбор пал на амтолметин гуацил (Найзилат). Амтолметин гуацил как молекула был синтезирован в Италии в 1985 г. Его предшественник толметин – это хорошо изученный неселективный НПВП, который никогда не был представлен в России, однако широко применялся во всем мире. Толметин характеризуется хорошим обезболивающим и противовоспалительным эффектом, а дополнительное его преимущество заключается во влиянии на таламические центры болевой чувствительности. Амтолметин гуацил унаследовал все положительные свойства толметина, при этом получив дополнительные преимущества. Основное отличие этого препарата от всей группы НПВП – наличие в составе ванилиновой группы, которая имеет высокую аффинность к капсаициновым рецепторам слизистой оболочки желудка, двенадцатиперстной и тонкой кишки. В результате раздражения последних запускается локальная выработка оксида азота, который наравне с физиологическими простагландинами играет значимую роль в системе гастропротекции. Последующее неизбежное снижение выработки физиологических простагландинов в результате действия неселективного НПВП в значимой степени компенсируется данным механизмом, что позволяет заметно уменьшить частоту побочных эффектов со стороны ЖКТ при применении данного препарата. Таким образом, амтолметин гуацил совмещает в себе, казалось бы, несочетаемые свойства: положительные качества неселективного НПВП (хорошее обезболивающее и противовоспалительное действие) и протективный эффект в отношении слизистой оболочки ЖКТ [21]. Клинические исследования, проведенные в различных странах Европы, показали, что по своим основным свойствам амтолметин гуацил не уступает таким препаратам, как диклофенак и индометацин, в то время как частота развития поражения ЖКТ при применении амтолметина гуацила значительно ниже [20–22].
Назначение Найзилата пациенту с сочетанием двух микрокристаллических артритов в течение 6 мес. оказалось эффективным и безопасным как для купирования обострения, так и для длительного приема.
Диагностика и лечение микрокристаллических артритов, несмотря на их широкое распространение, до сих пор вызывают затруднение. На практике невозможно создать оптимальный алгоритм диагностики микрокристаллических артритов, который позволил бы поставить достоверный диагноз у каждого пациента. Однако при использовании современных методов диагностики верификация сходных по клинической картине заболеваний максимально вероятна. Подбор адекватной противовоспалительной и анальгетической терапии при остром, в т. ч. часто рецидивирующем, артрите должен осуществляться индивидуально у каждого пациента с учетом противопоказаний и сопутствующих заболеваний.


 Артропатия: что это, классификация, симптомы и лечение
Артропатия: что это, классификация, симптомы и лечение Реактивная артропатия: что это, классификация, симптомы и лечение
Реактивная артропатия: что это, классификация, симптомы и лечение Малая хорея: что это, причины, симптомы и лечение
Малая хорея: что это, причины, симптомы и лечение Перелом мизинца на ноге: симптомы, диагностика и лечение
Перелом мизинца на ноге: симптомы, диагностика и лечение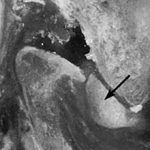 Артроз височно-нижнечелюстного сустава: симптомы, диагностика и лечение
Артроз височно-нижнечелюстного сустава: симптомы, диагностика и лечение Мелоксикам: инструкция по применению, аналоги, отзывы
Мелоксикам: инструкция по применению, аналоги, отзывы Метотрексат: показания, инструкция по применению, отзывы
Метотрексат: показания, инструкция по применению, отзывы Остеоартрит: что это, причины, симптомы и лечение
Остеоартрит: что это, причины, симптомы и лечение