Углеводный обмен — Википедия
Углеводный обмен, или метаболизм углеводов в организмах животных и человека. Метаболизм углеводов в организме человека состоит из следующих процессов:
- Расщепление в пищеварительном тракте поступающих с пищей поли- и дисахаридов до моносахаридов, дальнейшее всасывание моносахаридов из кишечника в кровь.

- Синтез и распад гликогена в тканях
 (гликогенез и гликогенолиз), прежде всего в печени.
(гликогенез и гликогенолиз), прежде всего в печени. - Гликолиз — распад глюкозы.

 в отличие от «анаэробного гликолиза»,
в отличие от «анаэробного гликолиза»,
- Анаэробный путь прямого окисления глюкозы или, как его называют, пентозофосфатный путь (пентозный цикл).

- Взаимопревращение гексоз.
- Анаэробный метаболизм пирувата. Этот процесс выходит за рамки углеводного обмена, однако может рассматриваться как завершающая его стадия: окисление продукта гликолиза — пирувата.
- Глюконеогенез — образование углеводов из неуглеводных продуктов
 (пирувата, лактата, глицерина, аминокислот, липидов, белков и т. д.).
(пирувата, лактата, глицерина, аминокислот, липидов, белков и т. д.).
Углеводы входят в состав живых организмов и вместе с белками, липидами и нуклеиновыми кислотами определяют специфичность их строения и функционирования. К углеводам относят соединения, обладающие разнообразными и зачастую сильно отличающимися функциями. Углеводы участвуют во многих метаболических процессах, но прежде всего они являются основными поставщиками энергии. На долю углеводов приходится примерно 75 % массы пищевого суточного рациона и более 50 % от суточного количества необходимых калорий. Однако неправильно сводить функцию углеводов только к энергетическому обеспечению процессов жизнедеятельности организма. Следует отметить и структурную роль углеводов. Так, в виде гликозаминогликанов углеводы входят в состав межклеточного матрикса. Большое число белков (ферменты, белки-транспортёры, белки-рецепторы, гормоны) — гликопротеины, углеводная составляющая которых повышает их специфичность. Например, различия в строении олигосахаридных фрагментов клеточной оболочки эритроцитов обеспечивают групповую принадлежность крови. Из углеводов в процессе метаболизма образуется большое число органических соединений, которые служат исходными субстратами для синтеза липидов, аминокислот, нуклеотидов. Производные углеводов — глюкурониды — участвуют в детоксикации ксенобиотиков и инактивации веществ эндогенного происхождения
- Углеводы, потребляемые с пищей
-

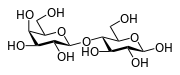
Лактоза или молочный сахар, впервые была обнаружена в коровьем молоке, откуда и получила своё название.
-

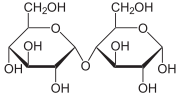
Мальтоза или солодовый сахар, входит в состав семян зерновых культур (ячменя, ржи, пшеницы итд.).
-

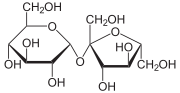
Сахароза — один из самых потребляемых углеводов в мире.
Переваривание и всасывание углеводов[править | править код]
Пищеварение углеводов можно разделить на несколько этапов:
- Пищеварение, происходящее в полости рта
- Пищеварение в желудке
- Пищеварение и всасывание в тонком кишечнике.
Эпителиальные клетки кишечника способны всасывать только моносахариды. Поэтому процесс переваривания заключается в ферментативном гидролизе гликозидных связей в углеводах, имеющее олиго- или полисахаридное строение.
Переваривание углеводов в полости рта[править | править код]
В полости рта начинается расщепление крахмала (и гликогена) под действием фермента слюны — амилазы. Известны 3 вида амилаз, которые различаются главным образом по конечным продуктам их ферментативного действия:
- α-амилаза
- β-амилаза
- γ-амилаза
α-Амилаза (КФ 3.2.1.1) расщепляет в полисахаридах внутренние α-1,4-связи, поэтому её иногда называют эндоамилазой. Молекула α-амилазы содержит в своих активных центрах ионы Ca2+ необходимые для ферментативной активности. Кроме того, характерной особенностью α-амилазы животного происхождения является способность активироваться одновалентными анионами. Прежде всего Сl
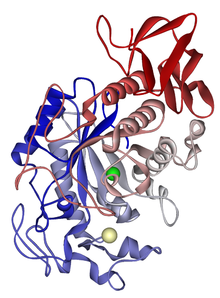 Структура α-амилазы слюнных желез. Катион кальция показан жёлтым цветом, анион хлора — зелёным.
Структура α-амилазы слюнных желез. Катион кальция показан жёлтым цветом, анион хлора — зелёным.Слюнная α-амилаза представляет собой смесь близких электрофоретически разделяемых изоферментов. Каждый из них — одноцепочечный полипептид (мол. масса 56000 Да), к которому присоединен олигосахарид. Структура этого олигосахарида, а также число его молекул на одну молекулу белка и способ прикрепления к белку неизвестны. Удивительно, что не существует соответствующих ферментов в слюне некоторых приматов, например у бабуинов или резусов.
В ротовой полости не может происходить полное расщепление крахмала, так как действие фермента на крахмал кратковременно. Кроме того, амилаза слюны не расщепляет α- 1,6-гликозидные связи (связи в местах разветвлений), поэтому крахмал переваривается лишь частично с образованием крупных фрагментов — декстринов и небольшого количества мальтозы. Следует отметить, что амилаза слюны не гидролизует гликозидные связи в дисахаридах.
Под действием β-амилазы от крахмала отщепляется дисахарид мальтоза, то есть β-амилаза является экзоамилазой. Она обнаружена у высших растений где играет важную роль в мобилизации резервного (запасного) крахмала.
γ-Амилаза отщепляет один за другим глюкозные остатки от конца полигликозидной цепочки. Различают 2 вида γ-амилаз: кислые и нейтральные, в зависимости от того в какой области pH они проявляют максимальную активность. В органах и тканях человека и млекопитающих кислая γ-амилаза локализована в лизосомах, а нейтральная — в микросомах и гиалоплазме. Амилаза слюны является α-амилазой. Под влиянием этого фермента происходят первые фазы распада крахмала (или гликогена) с образованием декстринов (в небольшом количестве образуется и мальтоза). Затем пища смешанная со слюной попадает в желудок.
Желудочный сок не содержит ферментов расщепляющие сложные углеводы (например целлюлозу). В желудке действие α-амилазы слюны прекращается так как желудочное содержимое имеет очень кислую среду (pH 1,5 — 2,5). Однако в более глубоких слоях пищевого комка, куда не сразу проникает желудочный сок, действие амилазы некоторое время продолжается и происходит расщепление полисахаридов с образованием декстринов и мальтозы. Наиболее важная фаза распада крахмала (или гликогена) протекает в двенадцатиперстной кишке под действием α-амилазы поджелудочного сока. Здесь pH возрастает до нейтральных значений, при этих условиях α-амилаза панкреатического сока обладает почти максимальной активностью. Этот фермент завершает превращение крахмала и гликогена в мальтозу, начатое амилазой слюны.
Переваривание углеводов в кишечнике[править | править код]
Расщепление крахмала и гликогена до мальтозы в кишечнике происходит под действием 3-х ферментов:
- панкреатической α-амилазы
- амило-1,6-глюкозидазы
- олиго-1,6-глюкозидазы
Образующаяся мальтоза оказывается только временным продуктом, так как она быстро гидролизуется под влиянием фермента мальтазы (α-глюкозидазы) на 2 молекулы глюкозы. Кишечный сок также содержит активную сахаразу, под действием которой образуются глюкоза и фруктоза.
Панкреатическая α-амилаза[править | править код]
В двенадцатиперстной кишке рН среды желудочного содержимого нейтрализуется, так как секрет поджелудочной железы имеет рН 7,5-8,0 и содержит гидрокарбонаты (НСО3—). С секретом поджелудочной железы в кишечник поступает панкреатическая α-амилаза. Этот фермент гидролизует α-1,4-гликозидные связи в крахмале и декстринах.
Продукты переваривания крахмала на этом этапе — дисахарид мальтоза, содержащая 2 остатка глюкозы, связанные α-1,4-связью. Из тех остатков глюкозы, которые в молекуле крахмала находятся в местах разветвления и соединены α-1,6-гликозидной связью, образуется дисахарид изомальтоза. Кроме того, образуются олигосахариды, содержащие 3-8 остатков глюкозы, связанные α-1,4- и α-1,6-связями
α-Амилаза поджелудочной железы, так же, как α-амилаза слюны, действует как эндогликозидаза. Панкреатическая α-амилаза не расщепляет α-1,6-гликозидные связи в крахмале. Этот фермент также не гидролизует β-1,4-гликозидные связи, которыми соединены остатки глюкозы в молекуле целлюлозы. Целлюлоза, таким образом, проходит через кишечник неизменённой. Тем не менее непереваренная целлюлоза выполняет важную функцию балластного вещества, придавая пище дополнительный объём и положительно влияя на процесс переваривания. Кроме того, в толстом кишечнике целлюлоза может подвергаться действию бактериальных ферментов и частично расщепляться с образованием спиртов, органических кислот и СО2. Продукты бактериального расщепления целлюлозы важны как стимуляторы перистальтики кишечника.
Мальтоза, изомальтоза и триозосахариды, образующиеся в верхних отделах кишечника из крахмала, — промежуточные продукты. Дальнейшее их переваривание происходит под действием специфических ферментов в тонком кишечнике. Дисахариды пищи сахароза и лактоза также гидролизуются специфическими дисахаридазами в тонком кишечнике.
Особенность переваривания углеводов в тонком кишечнике заключается в том, что активность специфических олиго- и дисахаридаз в просвете кишечника низкая. Но ферменты активно действуют на поверхности эпителиальных клеток кишечника.
Тонкий кишечник изнутри имеет форму пальцеобразных выростов — ворсинок, покрытых эпителиальными клетками. Эпителиальные клетки, в свою очередь, покрыты микроворсинками, обращёнными в просвет кишечника. Эти клетки вместе с ворсинками образуют щёточную каёмку, благодаря которой увеличивается поверхность контакта гидролитических ферментов и их субстратов в содержимом кишечника. На 1 мм2 поверхности тонкой кишки у человека приходится 80-140 млн ворсинок.
Ферменты, расщепляющие гликозидные связи в дисахаридах (дисахаридазы), образуют ферментативные комплексы, локализованные на наружной поверхности цитоплазматической мембраны энтероцитов.
Сахаразо-изомальтазный комплекс[править | править код]
Этот ферментативный комплекс состоит из двух полипептидных цепей и имеет доменное строение. Сахаразо-изомальтазный комплекс прикрепляется к мембране микроворсинок кишечника с помощью гидрофобного (трансмембранного) домена, образованного N-концевой частью полипептида. Каталитический центр выступает в просвет кишечника. Связь этого пищеварительного фермента с мембраной способствует эффективному поглощению продуктов гидролиза клеткой.
Сахаразо-изомальтазный комплекс гидролизует сахарозу и изомальтозу, расщепляя α-1,2- и α-1,6-гликозидные связи. Кроме того, оба ферментных домена имеют мальтазную и мальтотриазную активности, гидролизуя α-1,4-гликозидные связи в мальтозе и мальтотриозе (трисахарид, образующийся из крахмала). На долю сахаразо-изомальтазного комплекса приходится 80 % от всей мальтазной активности кишечника. Но несмотря на присущую ему высокую мальтазную активность, этот ферментативный комплекс назван в соответствии с основной специфичностью. К тому же сахаразная субъединица — единственный фермент в кишечнике, гидролизующий сахарозу. Изомальтазная субъединица с большей скоростью гидролизует гликозидные связи в изомальтозе, чем в мальтозе и мальтотриозе.
В тощей кишке содержание сахаразо-изомальтазного ферментативного комплекса достаточно высокое, но оно снижается в проксимальной и дистальной частях кишечника.
Гликоамилазный комплекс[править | править код]
Этот ферментативный комплекс катализирует гидролиз α-1,4-связи между глюкозными остатками в олигосахаридах, действуя с восстанавливающего конца. По механизму действия этот фермент относят к экзогликозидазам. Комплекс расщепляет также связи в мальтозе, действуя как мальтаза. В гликоамилазный комплекс входят две разные каталитические субъединицы, имеющие небольшие различия в субстратной специфичности. Гликоамилазная активность комплекса наибольшая в нижних отделах тонкого кишечника.
β-Гликозидазный комплекс (лактаза)[править | править код]
Лактаза расщепляет β-1,4-гликозидные связи между глюкозой и галактозой в лактозе.
Этот ферментативный комплекс по химическому составу является гликопротеином. Лактаза, как и другие гликозидазные комплексы, связана с щёточной каёмкой и распределена неравномерно по всему тонкому кишечнику. Активность лактазы колеблется в зависимости от возраста. Так, активность лактазы у плода особенно повышена в более поздние сроки беременности и сохраняется на высоком уровне до 5-7 летнего возраста. Затем активность фермента снижается, составляя у взрослых 10 % от уровня активности, характерного для детей.
Трегалаза[править | править код]
Трегалаза (КФ 3.2.1.28) — также гликозидазный комплекс, гидролизующий связи между мономерами в трегалозе — дисахариде, содержащемся в грибах.
Совместное действие всех перечисленных ферментов завершает переваривание пищевых олиго- и полисахаридов с образованием моносахаридов, основной из которых — глюкоза. Кроме глюкозы, из углеводов пищи также образуются фруктоза и галактоза, в меньшем количестве — манноза, ксилоза, арабиноза.
Всасывание моносахаридов в кишечнике[править | править код]
Моносахариды образовавшиеся в результате переваривания, всасываются эпителиальными клетками тощей и подвздошной кишок с помощью специальных механизмов транспорта через мембраны клеток.
Транспорт моносахаридов в клетки слизистой оболочки кишечника может осуществляться разными способами: путём облегчённой диффузии и активного транспорта. В случае активного транспорта глюкоза и Na+ проходят через мембраны с люминальной стороны, связываясь с разными участками белка-переносчика. При этом Na+ поступает в клетку по градиенту концентрации, и одновременно глюкоза транспортируется против градиента концентрации (вторично-активный транспорт). Следовательно, чем больше градиент Na+, тем больше поступление глюкозы в энтероциты. Если концентрация Na+ во внеклеточной жидкости уменьшается, транспорт глюкозы снижается. Градиент концентрации Na+, являющийся движущей силой активного сим-порта, создаётся работой Nа+, К+-АТФ-азы. Перенос в клетки слизистой оболочки кишечника по механизму вторично-активного транспорта характерен также для галактозы.
При разной концентрации глюкозы в просвете кишечника «работают» различные механизмы транспорта. Благодаря активному транспорту эпителиальные клетки кишечника могут поглощать глюкозу при её очень низкой концентрации в просвете кишечника. Если же концентрация глюкозы в просвете кишечника велика, то она может транспортироваться в клетку путём облегчённой диффузии. Таким же способом может всасываться и фруктоза. Следует отметить, что скорость всасывания глюкозы и галактозы гораздо выше, чем других моносахаридов.
После всасывания моносахариды (главным образом, глюкоза) покидают клетки слизистой оболочки кишечника через мембрану, обращённую к кровеносному капилляру, с помощью облегчённой диффузии. Часть глюкозы (более половины) через капилляры кишечных ворсинок попадает в кровеносную систему и по воротной вене доставляется в печень. Остальное количество глюкозы поступает в клетки других тканей.
Транспорт глюкозы из крови в клетки[править | править код]
Потребление глюкозы клетками из кровотока происходит также путём облегчённой диффузии. Следовательно, скорость трансмембранного потока глюкозы зависит только от градиента её концентрации. Исключение составляют клетки мышц и жировой ткани, где облегчённая диффузия регулируется инсулином (гормон поджелудочной железы). В отсутствие инсулина плазматическая мембрана этих клеток непроницаема для глюкозы, так как она не содержит белки-переносчики (транспортёры) глюкозы. Транспортёры глюкозы называют также рецепторами глюкозы. Например, описан транспортёр глюкозы, выделенный из эритроцитов. Это трансмембранный белок, полипептидная цепь которого построена из 492 аминокислотных остатков и имеет доменную структуру. Полярные домены белка расположены по разные стороны мембраны, гидрофобные располагаются в мембране, пересекая её несколько раз. Транспортёр имеет участок связывания глюкозы на внешней стороне мембраны. После присоединения глюкозы конформация белка изменяется, в результате чего глюкоза оказывается связанной с белком в участке, обращённом внутрь клетки. Затем глюкоза отделяется от транспортёра, переходя внутрь клетки. Считают, что способ облегчённой диффузии по сравнению с активным транспортом предотвращает транспорт ионов вместе с глюкозой, если она транспортируется по градиенту концентрации.
Глюкозные транспортёры[править | править код]
Глюкозные транспортёры или ГЛЮТ представляют собой несколько семейств мембранных белков, обнаруженных во всех тканях организма млекопитающих. На данный момент существуют несколько десятков разновидностей ГЛЮТ, они пронумерованы в соответствии с порядком их обнаружения[3].
Структура белков семейства ГЛЮТ отличается от белков, транспортирующих глюкозу через мембрану в кишечнике и почках против градиента концентрации. Описанные 4 типа ГЛЮТ имеют сходные первичную структуру и доменную организацию (все 4 типа относятся к I классу переносчиков глюкозы). ГЛЮТ-5 имеет несколько иную структуру и относится ко II классу переносчиков глюкозы.
Распределение белков-транспортёров глюкозы (ГЛЮТ)
| Типы ГЛЮТ | Локализация в органах |
|---|---|
| ГЛЮТ-1 | Преимущественно в мозге, плаценте, почках, толстом кишечнике. |
| ГЛЮТ-2 | Преимущественно в печени, почках, β-клетках островков Лангерганса, эритроцитах. |
| ГЛЮТ-3 | Во многих тканях, включая мозг, плаценту, почки. |
| ГЛЮТ-4(инсулинзависимый) | В мышцах (скелетных и сердечной), жировой ткани. Содержится в отсутствии инсулина почти полностью в цитоплазме. |
| ГЛЮТ-5 | В апикальном отделе энтероцитов тонкого кишечника. Является переносчиком фруктозы[4]. |
Все типы ГЛЮТ могут находиться как в плазматической мембране, так и в цитозольных везикулах. ГЛЮТ-4 (и в меньшей мере ГЛЮТ-1) почти полностью находятся в цитоплазме клеток. Влияние инсулина на такие клетки приводит к перемещению везикул, содержащих ГЛЮТ, к плазматической мембране, слиянию с ней и встраиванию транспортёров в мембрану. После чего возможен облегчённый транспорт глюкозы в эти клетки. После снижения концентрации инсулина в крови транспортёры глюкозы снова перемещаются в цитоплазму, и поступление глюкозы в клетку прекращается.
Перемещение глюкозы из первичной мочи в клетки почечных канальцев происходит вторично-активным транспортом, подобно тому, как это осуществляется при всасывании глюкозы из просвета кишечника в энтероциты. Благодаря этому глюкоза может поступать в клетки даже в том случае, если её концентрация в первичной моче меньше, чем в клетках. При этом глюкоза реабсорбируется из первичной мочи почти полностью (99 %).
Известны различные нарушения в работе транспортёров глюкозы. Наследственный дефект этих белков может лежать в основе инсулинонезависимого сахарного диабета В то же время причиной нарушения работы транспортёра глюкозы может быть не только дефект самого белка. Нарушения функции ГЛЮТ-4 возможны на следующих этапах:
- передача сигнала инсулина о перемещении этого транспортёра к мембране;
- перемещение транспортёра в цитоплазме;
- включение в состав мембраны;
- отшнуровывание от мембраны и т. д.
Нарушения переваривания и всасывания углеводов[править | править код]
В основе патологии переваривания и всасывания углеводов могут быть причины двух типов:
- дефекты ферментов, участвующих в гидролизе углеводов в кишечнике;
- нарушение всасывания продуктов переваривания углеводов в клетки слизистой оболочки кишечника.
В обоих случаях возникает осмотическая диарея, которую вызывают нерасщеплённые дисахариды или невсосавшиеся моносахариды. Эти невостребованные углеводы поступают в дистальные отделы кишечника, изменяя осмотическое давление содержимого кишечника. Кроме того, оставшиеся в просвете кишечника углеводы частично подвергаются ферментативному расщеплению микроорганизмами с образованием органических кислот и газов. Всё вместе приводит к притоку воды в кишечник, увеличению объёма кишечного содержимого, усилению перистальтики, спазмам и болям, а также метеоризму.
Термином «мальабсорбция» называют недостаточное всасывание переваренных продуктов углеводов. Но поскольку клинические проявления при недостаточном переваривании и всасывании сходны, то термином «мальабсорбция» называют оба вида нарушений.
Нарушение переваривания углеводов в кишечнике[править | править код]
Нарушения переваривания могут быть связаны как с недостаточной активностью отдельных дисахаридаз, так и с недостаточностью всего ферментативного комплекса, например сахаразо-изомальтазного.
Известны наследственные и приобретённые формы недостаточности активности ферментов. Симптомы врождённых форм проявляются достаточно рано, например после первых кормлений грудным молоком (при дефиците лактазы), после перехода на искусственное вскармливание или при добавлении в рацион сахара и крахмала (при дефиците ос-амилазы или специфических дисахаридаз). В случае недостаточного лечения врождённые формы патологии сопровождаются хроническим дисбактериозом и нарушениями физического развития ребёнка.
Приобретённые формы патологии могут наблюдаться при кишечных заболеваниях, например гастритах, колитах, энтеритах. Следует заметить, что в этих случаях особенно заметно снижение активности лактазы. Как уже говорилось, активность лактазы в кишечнике ниже, чем других дисахаридаз, поэтому уменьшение её активности становится заметным для организма в первую очередь.
Дефицит лактазы у взрослых людей может иметь и другую причину. Возможно снижение экспрессии гена лактазы возрастного характера. Уже упоминалось, что активность лактазы у взрослых людей в норме значительно ниже, чем у детей. Поэтому снижение активности лактазы относительно уже имеющегося низкого уровня у отдельных людей может проявляться непереносимостью молока. Носителями патологии, связанной с дефицитом лактазы, являются чаще всего лица африканского и азиатского происхождения. Средняя частота данной формы патологии в странах Европы составляет 7-12 %, в Китае — 80 %, в отдельных районах Африки — до 97 %. Подобные наблюдения распространения лактазной недостаточности связывают с исторически сложившимся рационом питания и отсутствием молочного скотоводства в упомянутых регионах. Примеры и причины нарушения переваривания дисахаридов перечислены в таблице.
Существуют редкие формы нарушения переваривания углеводов. Например, известна наследственная недостаточность трегалазы, которая проявляется диспепсией после употребления грибов, содержащих трегалозу.
В отдельных случаях мальабсорбция может быть вызвана несколькими причинами. Например, после операции на желудке возможны ухудшение смешивания пищи с пищеварительными соками, снижение их секреции, ускорение прохождения пищи через кишечник, колонизация бактериями слепой и приводящей петель.
Нарушения всасывания моносахаридов[править | править код]
Для диагностики различных нарушений переваривания используют пробы с нагрузкой определёнными углеводами. Нарушения всасывания могут быть следствием дефекта какого-либо компонента (белка или фермента), участвующего в системе транспорта моносахаридов через мембрану. Описаны патологии, связанные с дефектом натрийзависимого белка переносчика глюкозы. Недостаточность кишечных дисахаридаз можно диагностировать с помощью введения дисахарида и последующего определения концентрации глюкозы в крови. Для большей чувствительности этот тест проводят, вводя сначала дисахарид (50 г), а затем эквивалентное количество составляющих его моносахаридов (по 25 г каждого). После нагрузки концентрация глюкозы в крови увеличивается примерно на 50 % относительно нормы. При патологии отмечают незначительную гипергликемию.
Нарушения переваревания дисахаридов
| Причина заболевания | Клинические проявления и лабораторные данные |
|---|---|
| Наследственный дефицит лактазы | Встречается относительно редко. После приёма молока наблюдаются рвота, диарея, спазмы и боли в животе, метеоризм. Симптомы развиваются сразу после рождения. |
| Недостаточность лактазы вследствие снижения экспрессии гена фермента в онтогенезе | Характерна для взрослых и детей старшего возраста. Является следствием возрастного снижения количества лактазы. Симптомы непереносимости молока аналогичны наследственной форме дефицита лактозы. |
| Недостаточность лактазы вторичного характера | Это временная, приобретённая форма. Непереносимость молока может быть следствием кишечных заболеваний, например, колитов, гастритов. Кроме того, временный дефицит лактазы может быть следствием операций на ЖКТ. |
| Наследственная недостаточность сахаразо-изомальтазного комплекса | Проявляется, когда в рацион детей добавляют сахарозу и крахмал. Больные дети обычно неохотно едят сладкое. После нагрузки сахарозой отмечается незначительная гипергликемия. Другие сахара (глюкоза, фруктоза, лактоза) переносятся хорошо. |
| Приобретённая недостаточность сахаразо-изомальтазного комплекса | Может возникать вследствие кишечных заболеваний. Проявляется диспепсией, провоцируемой крупами, крахмалом, а также пивом и другими напитками на основе солода. |
Если тест при нагрузке моносахаридом сопровождается адекватным повышением его концентрации в крови, а нагрузка дисахаридом не даёт нормальной реакции, то это, скорее всего, указывает на дефект кишечной дисахаридазы, а не системы транспорта.
О недостаточности лактазы можно судить, определяя водород в выдыхаемом воздухе (водородный тест). Водород образуется в результате действия бактериальных ферментов на лактозу.
Многие ткани синтезируют в качестве резервной формы глюкозы гликоген. Синтез и распад гликогена обеспечивают постоянство концентрации глюкозы в крови и создают депо для её использования тканями по мере необходимости.
Гликоген — одна из самых главных форм запасания углеводов у грибов, животных и человека.
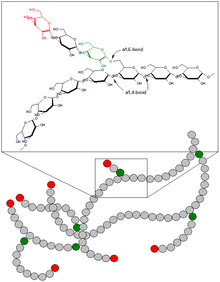 Структура гликогена
Структура гликогенаГликоген — разветвлённый гомополимер глюкозы, в котором остатки глюкозы соединены в линейных участках α-1,4-гликозидной связью. В точках ветвления мономеры соединены α-1,6-гликозидными связями. Эти связи образуются примерно с каждым десятым остатком глюкозы. Следовательно, точки ветвления в гликогене встречаются примерно через каждые десять остатков глюкозы. Так возникает древообразная структура с молекулярной массой >107Д, что соответствует приблизительно 50 000 остатков глюкозы. Таким образом, в молекуле гликогена имеется только одна свободная аномерная ОН-группа и, следовательно, только один восстанавливающий (редуцирующий) конец.
При полимеризации глюкозы снижается растворимость образующейся молекулы гликогена и, следовательно, её влияние на осмотическое давление в клетке. Это обстоятельство объясняет, почему в клетке депонируется гликоген, а не свободная глюкоза.
После приёма пищи, богатой углеводами, запас гликогена в печени может составлять примерно 4 %-5 % от её массы. В мышцах запасается около 1 % гликогена, однако масса мышечной ткани значительно больше и поэтому общее количество гликогена в мышцах в 2 раза больше, чем в печени. Гликоген может синтезироваться во многих клетках, например в нейронах, макрофагах, клетках жировой ткани, но содержание его в этих тканях незначительно. В организме может содержаться до 450 г гликогена.
Запасы углеводов в организме нормального человека (массой 70 кг) после приёма пищи. В таблице приведены средние показатели.
| Углевод | Процентное содержание и масса |
|---|---|
| Гликоген печени | 4 % = 72 г |
| Мышечный гликоген | 0,7 % = 245 г |
| Внеклеточная глюкоза | 0,1 % = 10 г |
| Итого | 327 г |
Следует подчеркнуть, что синтез и распад гликогена в клетке осуществляется разными метаболическими путями. В частности считалось, что гликогенфосфорилаза (фосфорилаза а) катализирует как распад, так и синтез гликогена потому что в опытах in vitro, было доказано что гликогенфосфорилазная реакция обратима. Однако в дальнейшем было установлено, что в клетке (in vivo) фосфорилаза а катализирует только распад гликогена, синтез гликогена осуществляется совершенно другим ферментом. Оба эти процесса (синтез и распад) регулируют содержание глюкозы в крови и создают резерв глюкозы для интенсивной мышечной работы.
Распад гликогена печени служит в основном для поддержания уровня глюкозы в крови в постабсорбтивном периоде. Поэтому содержание гликогена в печени изменяется в зависимости от ритма питания. При длительном голодании оно снижается почти до нуля. Гликоген мышц служит резервом глюкозы — источника энергии при мышечном сокращении. Мышечный гликоген не используется для поддержания уровня глюкозы в крови. Как уже упоминалось ранее, в клетках мышц нет фермента глюкозо-6-фосфатазы, и образование свободной глюкозы невозможно. Расход гликогена в мышцах зависит в основном от физической нагрузки.
Гликогеногенез[править | править код]
Гликоген синтезируется в период пищеварения (через 1-2 ч после приёма углеводной пищи). Следует отметить, что синтез гликогена из глюкозы, как и любой анаболический процесс, является эндергоническим, то есть требующим затрат энергии.
Глюкоза, поступающая в клетку, фосфорилируется при участии АТФ. Затем глюкозо-6-фосфат в ходе обратимой реакции превращается в глюкозо-1-фосфат под действием фермента фосфоглюкомутазы. Глюкозо-1-фосфат по термодинамическому состоянию мог бы служить субстратом для синтеза гликогена. Но в силу обратимости реакции глюкозо-6-фосфат ↔ глюкозо-1-фосфат синтез гликогена из глюкозо-1-фосфата и его распад оказались бы также обратимыми и поэтому неконтролируемыми. Чтобы синтез гликогена был термодинамически необратимым, необходима дополнительная стадия образования УДФ-глюкозы из УТФ и глюкозо-1-фосфата. Фермент, катализирующий эту реакцию, назван по обратной реакции: УДФ-глюкопирофосфорилаза. Однако в клетке обратная реакция не протекает, потому что образовавшийся в ходе прямой реакции пирофосфат очень быстро расщепляется пирофосфатазой на 2 молекулы фосфата.
Реакция образования УДФ-глюкозы обусловливает необратимость всей серии реакций, протекающих при синтезе гликогена. Этим же объясняется невозможность протекания распада гликогена путём простого обращения процесса его синтеза.
Образованная УДФ-глюкоза далее используется как донор остатка глюкозы при синтезе гликогена. Эту реакцию катализирует фермент гликогенсинтаза (глюкозилтрансфераза). Поскольку в данной реакции не используется АТФ, фермент называют синтазой, а не синтетазой. Нуклеотидная часть УДФ-глюкозы играет существенную роль в действии гликоген синтазы, выполняя функцию «рукоятки», при помощи которой фермент располагает глюкозу в полисахаридной цепи в нужном положении. Кроме того, нуклеотидная часть УДФ-глюкозы, по-видимому, необходима для узнавания субстрата при катализе.
Так как гликоген в клетке никогда не расщепляется полностью, синтез гликогена осуществляется путём удлинения уже имеющейся молекулы полисахарида, называемой «затравка», или «праймер». К «затравке» последовательно присоединяются молекулы глюкозы. Строением молекулы «затравки» как бы предопределяется тип связи, который возникает в реакции трансгликозилирования. Таким образом, синтезируется полисахарид, аналогичный по строению с «затравочным». В состав «затравки» может входить белок гликогенин, в котором к ОН-группе одного из тирозиновых остатков присоединена олигосахаридная цепочка (примерно 8 остатков глюкозы). Глюкозные остатки переносятся гликогенсинтазой на нередуцирующий конец олигосахарида и связываются α-1,4-гликозидными связями. По окончании синтеза гликогенин остаётся включённым в гранулу гликогена.
Разветвлённая структура гликогена образуется при участии амило-1,4 → 1,6-глюкозилтрансферазы, называемой ферментом «ветвления» (от англ. branching enzyme). Как только гликогенсинтаза удлиняет линейный участок примерно до 11 глюкозных остатков, фермент ветвления переносит её концевой блок, содержащий 6-7 остатков, на внутренний остаток глюкозы этой или другой цепи. В точке ветвления концевой остаток глюкозы олигосахарида соединяется с г
нарушения углеводного обмена | Что делать, если нарушился углеводный обмен?
Нарушения углеводного обмена1. Нарушения гидролиза и всасывания углеводов
Всасывание углеводов нарушается при недостаточности амилолитических ферментов желудочно-кишечного тракта (амилаза панкреатического сока и др.). При этом поступающие с пищей углеводы не расщепляются до моносахаридов и не всасываются. Развивается углеводное голодание.
Всасывание углеводов страдает также при нарушении фосфорилирования глюкозы в кишечной стенке, возникающем при воспалении кишечника, при отравлении ядами, блокирующими фермент гексокиназу (флоридзин, монойодацетат). Не происходит фосфорилирования глюкозы в кишечной стенке и она не поступает в кровь.
Всасывание углеводов особенно легко нарушается у детей грудного возраста, у которых еще не вполне сформировались пищеварительные ферменты и ферменты, обеспечивающие фосфорилирование и дефосфорилирование.
Причины нарушения углеводного обмена, вследствие нарушения гидролиза и всасывания углеводов:
— гипоксия
— нарушение функций печени — нарушение образования гликогена из молочной кислоты — ацидоз (гиперлакцидемия).
— гиповитаминоз В1.
2. Нарушения синтеза и расщепления гликогена
Синтез гликогена может изменяться в сторону патологического усиления или снижения.
Усиление распада гликогена происходит при возбуждении центральной нервной системы. Импульсы по симпатическим путям идут к депо гликогена (печень, мышцы) и активируют гликогенолиз и мобилизацию гликогена. Кроме того, в результате возбуждения центральной нервной системы повышается функция гипофиза, мозгового слоя надпочечников, щитовидной железы, гормоны которых стимулируют распад гликогена.
Повышение распада гликогена при одновременном увеличении потребления мышцами глюкозы происходит при тяжелой мышечной работе.
Снижение синтеза гликогена происходит при воспалительных процессах в печени — гепатитах, в ходе которых нарушается ее гликоген-образовательная функция.
При недостатке гликогена тканевая энергетика переключается на жировой и белковый обмены. Образование энергии за счет окисления жира требует много кислорода; в противном случае в избытке накапливаются кетоновые тела и наступает интоксикация. Образование же энергии за счет белков ведет к потере пластического материала.
Гликогеноз — нарушение обмена гликогена, сопровождающееся патологическим накоплением гликогена в органах.
Болезнь Гирке — гликогеноз, обусловленный врожденным недостатком глюкозо-6-фосфатазы — фермента, содержащегося в клетках печени и почек. Глюкозо-6-фосфата-за отщепляет свободную глюкозу от глюкозо-6-фосфата, что делает возможным трансмембранный переход глюкозы из клеток этих органов в кровь. При недостаточности глюкозо-6-фосфатазы глюкоза задерживается внутри клеток. Развивается гипогликемия. В почках и печени накапливается гликоген, что ведет к увеличению этих органов. Происходит перераспределение гликогена внутри клетки в сторону значительного накопления его в ядре. Возрастает содержание в крови молочной кислоты, в которую усиленно переходит глюкозо-6-фосфат. Развивается ацидоз. Организм страдает от углеводного голодания.
Больные дети, как правило, рано умирают.
Гликогеноз при врожденном дефиците α-глюкозидазы. Этот фермент отщепляет глюкозные остатки от молекул гликогена и расщепляет мальтозу. Он содержится в лизосомах и разобщен с фосфорилазой цитоплазмы. При отсутствии α-глюкозидазы в лизосомах накапливается гликоген, который оттесняет цитоплазму, заполняет всю клетку и разрушает ее. Содержание глюкозы в крови нормальное. Гликоген накапливается в печени, почках, сердце. Обмен веществ в миокарде нарушается, сердце увеличивается в размерах. Больные дети рано умирают от сердечной недостаточности.
3. Нарушения промежуточного обмена углеводов
К нарушению промежуточного обмена углеводов могут привести:
1. Гипоксические состояния (например, при недостаточности дыхания или кровообращения, при анемиях и др.), анаэробная фаза превращения углеводов преобладает над аэробной фазой. Происходит избыточное накопление в тканях и крови молочной и пировиноградной кислот. Содержание молочной кислоты в крови возрастает в несколько раз. Возникает ацидоз. Нарушаются ферментативные процессы. Снижается образование АТФ.
2. Расстройства функции печени, где в норме часть молочной кислоты ресинтезируется в глюкозу и гликоген. При поражении печени этот ресинтез нарушается. Развиваются гиперлакцидемия и ацидоз.
3. Гиповитаминоз В1. Нарушается окисление пировиноградной кислоты, так как витамин B1 входит в состав кофермента, участвующего в этом процессе. Пировиноградная кислота накапливается в избытке и частично переходит в молочную кислоту, содержание которой также возрастает. При нарушении окисления пировиноградной кислоты снижается синтез ацетилхолина и нарушается передача нервных импульсов. Уменьшается образование из пировиноградной кислоты ацетилкоэнзима А. Пировиноградная кислота является фармакологическим ядом для нервных окончаний. При увеличении ее концентрации в 2-3 раза возникают нарушения чувствительности, невриты, параличи и др.
При гиповитаминозе B1 нарушается также и пентозофосфатный путь обмена углеводов, в частности образование рибозы.
4. Гипергликемия
Гипергликемия — повышение уровня сахара крови выше нормального. В зависимости от этиологических факторов различают следующие виды гипергликемий:
1. Алиментарная гипергликемия. Развивается при приеме больших количеств сахара. Этот вид гипергликемии используют для оценки состояния углеводного обмена (так называемая сахарная нагрузка). У здорового человека после одномоментного приема 100-150 г сахара содержание глюкозы в крови нарастает, достигая максимума — 1,5-1,7 г/л (150-170 мг%) через 30-45 мин. Затем уровень сахара крови начинает падать и через 2 ч снижается до нормы (0,8-1,2 г/л), а через 3 ч оказывается даже несколько сниженным.
2. Эмоциональная гипергликемия. При резком преобладании в коре головного мозга раздражительного процесса над тормозным возбуждение иррадиирует на нижележащие отделы центральной нервной системы. Поток импульсов по симпатическим путям, направляясь к печени, усиливает в ней распад гликогена и тормозит переход углеводов в жир. Одновременно возбуждение воздействует через гипоталамические центры и симпатическую нервную систему на надпочечники. Происходит выброс в кровь больших количеств адреналина, стимулирующего гликогенолиз.
3. Гормональные гипергликемии. Возникают при нарушении функции эндокринных желез, гормоны которых участвуют в регуляции углеводного обмена. Например, гипергликемия развивается при повышении продукции глюкагона — гормона α-клеток островков Лангерганса поджелудочной железы, который, активируя фосфорилазу печени, способствует гликогенолизу. Сходным действием обладает адреналин. К гипергликемии ведет избыток глюкокортикоидов (стимулируют глюконеогенез и тормозят гексокиназу) и соматотропного гормона гипофиза (тормозит синтез гликогена, способствует образованию ингибитора гексокиназы и активирует инсулиназу печени).
4. Гипергликемии при некоторых видах наркоза. При эфирном и морфинном наркозах происходит возбуждение симпатических центров и выход адреналина из надпочечников; при хлороформном наркозе к этому присоединяется нарушение гликогенообразовательной функции печени.
5. Гипергликемия при недостаточности инсулина является наиболее стойкой и выраженной. Ее воспроизводят в эксперименте путем удаления поджелудочной железы. Однако при этом дефицит инсулина сочетается с тяжелым расстройством пищеварения. Поэтому более совершенной экспериментальной моделью инсулиновой недостаточности является недостаточность, вызванная введением аллоксана (C4h3N2O4), который блокирует SH-группы. В β-клетках островков Лангерганса поджелудочной железы, где запасы SH-групп невелики, быстро наступает их дефицит и инсулин становится неактивным.
Экспериментальную недостаточность инсулина можно вызвать дитизоном, блокирующим цинк в β-клетках островков Лангерганса, что ведет к нарушению образования гранул из молекул инсулина и его депонирования. Кроме того, в β-клетках образуется дитизонат цинка, который повреждает молекулы инсулина.
Недостаточность инсулина может быть панкреатической и внепанкреатической. Оба эти вида инсулиновой недостаточности могут вызвать сахарный диабет (diabetes mellitus).
6. Панкреатическая инсулиновая недостаточность
Этот тип недостаточности развивается при разрушении поджелудочной железы опухолями, туберкулезным или сифилитическим процессом, при острых воспалительно-дегенеративных процессах в поджелудочной железе — панкреатитах. В этих случаях нарушаются все функции поджелудочной железы, в том числе и способность вырабатывать инсулин. После панкреатита в 16-18% случаев развивается инсулиновая недостаточность в связи с избыточным разрастанием соединительной ткани, которая как бы «замуровывает» β-клетки, что нарушает их снабжение кислородом.
К инсулиновой недостаточности ведет местная гипоксия островков Лангерганса (атеросклероз, спазм сосудов), где в норме очень интенсивное кровообращение. При этом дисульфидные группы в инсулине переходят в сульфгидрильные и он становится неактивным (не оказывает гипогликемического эффекта).
Предполагают, что причиной инсулиновой недостаточности может послужить образование в организме при нарушении пуринового обмена аллоксана, близкого по структуре к мочевой кислоте (уреид мезоксалевой кислоты).
Инсулярный аппарат может истощаться после предварительного повышения функции, например при излишнем употреблении в пищу легкоусвояемых углеводов, вызывающих гипергликемию, при переедании.
В развитии панкреатической инсулиновой недостаточности важная роль принадлежит исходной наследственной неполноценности инсулярного аппарата.
7. Внепанкреатическая инсулиновая недостаточность
Этот тип недостаточности может развиться при повышенной активности инсулиназы — фермента, расщепляющего инсулин и образующегося в печени к началу полового созревания.
К недостаточности инсулина могут привести хронические воспалительные процессы, при которых в кровь поступает много протеолитических ферментов, разрушающих инсулин.
Избыток гидрокортизона, тормозящего гексокиназу, снижает действие инсулина. Активность инсулина снижается при избытке в крови неэстерифицированных жирных кислот, которые оказывают на него непосредственное тормозящее влияние.
Причиной недостаточности инсулина может послужить чрезмерно прочная его связь с переносящими белками в крови. Инсулин, связанный с белком, не активен в печени и мышцах, но оказывает обычно действие на жировую ткань (так называемый диабет тучных).
В ряде случаев при сахарном диабете содержание инсулина в крови нормально или даже повышено. Предполагают, что диабет при этом обусловлен присутствием в крови антагониста инсулина, однако природа этого антагониста не установлена.
Образование в организме антител против инсулина ведет к разрушению этого гормона.
Нарушения углеводного обмена при недостаточности инсулина.
Углеводный обмен при сахарном диабете характеризуется следующими особенностями:
1. резко снижен синтез глюкокиназы, которая при диабете почти полностью исчезает из печени, что ведет к уменьшению образования глюкозо-6-фосфата в клетках печени. Этот момент наряду со сниженным синтезом гликогенсинтетазы обусловливает резкое замедление синтеза гликогена. Происходит обеднение печени гликогеном. При недостатке глюкозо-6-фосфата тормозится пентозофосфатный цикл;
2. активность глюкозо-6-фосфатазы резко возрастает, поэтому глюкозо-6-фосфат дефосфорилируется и поступает в кровь в виде глюкозы;
3. тормозится переход глюкозы в жир;
4. понижается прохождение глюкозы через клеточные мембраны, она плохо усваивается тканями;
5. резко ускоряется глюконеогенез — образование глюкозы из лактата, пирувата, аминокислот жирных кислот и других продуктов неуглеводного обмена. Ускорение глюконеогенеза при сахарном диабете обусловлено отсутствием подавляющего влияния (супрессии) инсулина на ферменты, обеспечивающие глюконеогенез в клетках печени и почек: пируваткарбоксилазу, глюкозо-6-фосфатазу и др.
Таким образом, при сахарном диабете имеют место избыточная продукция и недостаточное использование глюкозы тканями, вследствие чего возникает гипергликемия. Содержание сахара в крови при тяжелых формах может достигать 4-5 г/л (400-500 мг%) и выше. При этом резко возрастает осмотическое давление крови, что ведет к обезвоживанию клеток организма. В связи с обезвоживанием глубоко нарушаются функции центральной нервной системы (гиперосмолярная кома).
Сахарная кривая при диабете по сравнению с таковой у здоровых значительно растянута во времени. Значение гипергликемии в патогенезе заболевания двояко. Она играет адаптивную роль, так как при ней тормозится распад гликогена и частично усиливается его синтез. При гипергликемии глюкоза лучше проникает в ткани и они не испытывают резкого недостатка углеводов. Гипергликемия имеет и отрицательное значение. При ней повышается концентрация глюко- и мукопротеидов, которые легко выпадают в соединительной ткани, способствуя образованию гиалина. Поэтому для сахарного диабета характерно раннее поражение сосудов атеросклерозом. Атеросклеротический процесс захватывает коронарные сосуды сердца (коронарная недостаточность), сосуды почек (гломерулонефриты) и др.
В пожилом возрасте сахарный диабет может сочетаться с гипертонической болезнью.
При повышении содержания сахара в крови до 1,6-2,0 г/л (160-200 мг%) и выше он начинает переходить в окончательную мочу — возникает глюкозурия.
Глюкозурия. В норме глюкоза содержится в провизорной моче. В канальцах она реабсорбируется в виде глюкозофосфата, для образования которого необходима гексокиназа, и после дефосфорилирования поступает в кровь. Таким образом, в окончательной моче сахара в нормальных условиях не содержится. При диабете процессы фосфорилирования и дефосфорилирования глюкозы в канальцах почек не справляются с избытком глюкозы в первичной моче. Развивается глюкозурия. При тяжелых формах сахарного диабета содержание сахара в моче может достигать 8-10%. Осмотическое давление мочи повышено; в связи с этим в окончательную мочу переходит много воды. Суточный диурез возрастает до 5-10 л и более (полиурия). Развивается обезвоживание организма и как следствие его — усиленная жажда (полидипсия).
Карта симптомов предназначена исключительно для образовательных целей. Не занимайтесь самолечением; по всем вопросам, касающимся определения заболевания и способов его лечения, обращайтесь к врачу. EUROLAB не несет ответственности за последствия, вызванные использованием размещенной на портале информации.
Нарушение углеводного обмена — диагностика и лечение в медицинском центре «Андреевские больницы
У каждого человека в норме уровень содержания глюкозы в крови должен быть от 3,3 до 5,5 ммоль/л. Конечно, глюкоза — очень важная постоянная гомеостаза. При расстройствах углеводного обмена (гипогликемия) в организме происходят необратимые изменения, которые связаны с деятельностью центральной нервной системы.
Понижение глюкозы в крови до 2.2 ммоль/л может спровоцировать судороги и нарушения сознания, человек может впасть гликемическую кому. При незначительном отклонении от нормы больной будет испытывать недомогание, а также снизится его работоспособность.
Причины нарушения углеводного обмена
Основными причинами нарушений процессов, связанных с углеводным обменом, могут стать:
- Нарушение фосфорилирования глюкозы в стенке кишечника (обычно это происходит в том случае, если воспаляется кишечная стенка, при отравлениях флоридзином и монойодацетагом).
- Нарушение нервно-гормональной регуляции.
- Нарушение углеводной функции печени.
- Нарушение нейрогормональной регуляции углеводного обмена.
Симптомы нарушения углеводного обмена
При нарушении разных видов углеводного обмена наблюдается снижение глюкокиназы. Возрастает активность глюко-фосфатазы, следовательно, глюкофосфат поступает в кровь в виде глюкозы. Через мембраны клеток глюкоза практически не проходит, вследствие чего она не способна усваиваться тканями. Ускоряется глюконеогенез (образование глюкозы из пирувата, лактата, амиокислот жирных веществ и др.).
Человек при пониженном уровне глюкозы в крови чувствует общую слабость, быстро утомляется, ему тяжело выполнять обычную ежедневную работу. При сильных отклонениях от нормы начинаются судороги, помутнения сознания. Самый страшный симптом этого заболевания – гликемическая кома.
Диагностика нарушения углеводного обмена
Чтобы правильно диагностировать заболевание, вам необходимо обратиться к врачу, который предложит вам пройти следующие анализы и обследования:
- В первую очередь нужно сдать анализ крови.
- Затем биохимический анализ крови.
- Сделать глюкозотолерантный тест.
- Липидный профиль.
- Гликированный гемоглобин.
- Определить уровень секреции инсулина, а также С-пептида.
- Провести иммунологические анализы.
- Проверить, расположены ли вы к возникновению развития нарушений углеродного обмена вследствие наследственности.
- Диагностика нефропатии.
- ЭКГ и УЗИ.
- Сканирование ультразвуком сосудов.
Врач, который специализируется на нарушениях углеводного обмена, – эндокринолог.
Лечение нарушений углеводного обмена
Для восстановления углеводного обмена можно воспользоваться медикаментозным лечением – препаратами, которые снижают сахар в крови. Это бигуаниды, ингибиторы альфа-глюкозидаза. Однако препараты не принесут пользы, если вы не будете соблюдать правильный режим жизни. Сюда входят: правильное питание, физические нагрузки, сахароснижающая терапия.
Профилактика нарушений углеводного обмена
В связи с нарушением обмена веществ могут развиться довольно сложные и серьезные заболевания, поэтому необходимо предпринять все меры для того, чтобы нарушения не начали развиваться. В первую очередь необходимо сбалансированно и правильно питаться. Это основной залог здоровья. Также существует множество витаминных препаратов, биологических пищевых добавок. Если вы – сладкоежка, от продуктов, содержащих много глюкозы, придется отказаться. Оптимальное употребление воды – 2 л в день.
Заболевания связанные с нарушениями углеводного обмена
Заболевания, связанные с нарушениями углеводного обмена, возникают при избытке либо недостатке углеводов в организме человека, что может быть вызвано наследственными и приобретенными факторами. Дисбаланс углеводов приводит к нарушению обмена веществ. Механизм заболевания прост: при нормальном уровне содержания глюкозы в крови человек чувствует себя замечательно, при значительных отклонениях от нормы – заболевает.Жизненно необходимые вещества Все микроэлементы, поступающие к нам с пищей, условно можно разделить на 4 группы: воду, углеводы, жиры и белки. Углеводы важны для слаженной работы всех органов человека, особенно, центральной нервной системы, печени и сердца. Эти вещества регулируют все процессы обмена жиров, белков и витаминов в организме. Без них невозможен синтез РНК и ДНК. Углеводы обеспечивают энергетическое питание всех органов, а главное, мозга. Попадая в организм, углеводы расщепляются на глюкозу, галактозу и фруктозу, после чего микроэлементы поступают в кровь. Если в организм поступает достаточное количество углеводов, их запас откладывается в мышцах и печени в виде гликогена, который еще называют животным крахмалом. Если человек потребляет углеводы с избытком, они трансформируются в жиры.
Симптомы нарушений углеводного обмена

Самыми частыми видами нарушений считаются гипергликемия, характеризующаяся повышенным уровнем глюкозы в крови, и гипогликемия, при которой наблюдается дефицит углеводов. Гипергликемия развивается в случае избытка углеводов в питании, к примеру, если человек долгое время злоупотребляет сладостями. Течение болезни часто переходит в сахарный диабет. Гипергликемия проявляется у людей с увеличенной щитовидной железой, почечной или печеночной недостаточностью, а также при некоторых других гормональных заболеваниях. Признаками избытка углеводов являются высокий уровень глюкозы в крови, ожирение и сахарный диабет. При эмоциональной гипергликемии возрастание глюкозы у человека происходит, когда он в состоянии стресса, гнева или другого возбуждения психики. Алиментарная гипергликемия появляется при избыточном потреблении сахара, а гормональная – из-за неправильного функционирования эндокринной системы.
Причинами развития гипогликемии становятся малоуглеводные диеты, голодание и проблемы пищеварительного тракта. Болезнь возникает, если у человека происходит недостаточное расщепление и всасывание углеводов.
При потреблении сладостей или повышении инсулина в крови у больных диабетом может развиться внезапная гипогликемия. Усиленные физические нагрузки на работе и в спорте, чрезмерно расходующие энергию и запасы гликогена, также способны привести к заболеванию. У истощенных алкогольной зависимостью людей гипогликемию может вызвать прием спиртного, если они не получают при этом достаточное количество углеводов. Острый приступ может вызвать также употребление некоторых лекарств.
Выделения из сосков груди
Дисгормональная мастопатия
Фиброзно-кистозная мастопатия с преобладанием фиброзного компонента
Мастопатия с преобладанием кистозного компонента
Увеличение лимфоузлов при мастопатии
Двусторонняя мастопатия
Симптомы острой гипогликемии проявляются в общей слабости, мелком дрожании рук и ног, сонливости. У человека бледнеют кожные покровы и слизистые, он испытывает острое чувство голода, возникает холодный пот, замирание сердца и учащенное сердцебиение. Могут проявляться нервозность, тревожность и страх.
Нарушения при углеводном гидролизе и всасывании
Такие нарушения возникают при недостаточной или избыточной активности поджелудочной железы. Именно амилолитические ферменты отвечают за расщепление углеводов до моносахаридов и обусловливают их всасывание. Нарушения обмена могут вызвать также недостаточность витамина «В», гипоксия и болезни печени. Нарушение синтеза и расщепления гликогена: Гликоген, который накапливается в печени, является своеобразным резервом. Он начинает расщепление до глюкозы при возникновении потребности в энергии в случае, если поступающих с пищей углеводов недостаточно. При последующих приемах пищи запас восполняется. Распад гликогена увеличивается в случаях перевозбуждения ЦНС и тяжелых физических нагрузках. Снижение расщепления происходит при наличии воспалительных процессов в печени. Недостаточное количество гликогена вызывает расход белков и жиров. При перерасходе сжигаемых жиров, особенно при недостатке кислорода, возникает избыточное образование кетонов. Усиленное сгорание белков вызывает потерю мышечной массы, волос и белковый дефицит. Наследственные заболевания: Обмен углеводов может быть нарушенным вследствие врожденных недостатков организма при искажениях работы ферментных аппаратов:
• гликогеноз, при котором гликоген интенсивно накапливается в органах и тканях;
• болезнь Гирке, т.е. врожденный недостаток фермента клеток печени и почек.
Нарушения промежуточного обмена
Есть несколько заболеваний, которые считаются разновидностями нарушений промежуточного углеводного обмена. Рассмотрим некоторые из них:
• гиперлакцидемия и ацидоз, характеризующиеся расстройствами функций печени;
• состояния гипоксии, при котором возникает избыточное концентрирование пировиноградной и молочной кислот в тканях и крови;
• переизбыток витамина «В1», при котором накапливание пировиноградной кислоты становится очень ядовитым для нервных отростков, в результате чего люди теряют чувствительность, может возникнуть неврит или паралич. Гипергликемии вызывают у людей повышение в крови уровня глюкозы и ведут к возникновению сахарного диабета. Инсулинорезистентность: Для питания клетки глюкозой очень важен инсулин. Если рецепторы клетки не воспринимают инсулин, возникает инсулинорезистентность, при которой глюкоза не способна из крови проникнуть в клетки. Чтобы глюкоза туда попала, организм вынужден все время поддерживать высокую концентрацию инсулина. Чем больше уровень глюкозы, тем больше требуется инсулина.
Углеводы и сахарный диабет
Независимо от причины болезни, организм при диабете не в состоянии полностью использовать сахар из продуктов, накапливать его в печени и мышечной ткани. Оставшаяся глюкоза циркулирует в организме, вступает в реакции, пагубно влияя на работу органов. При повышении ее концентрации образуются кетоновые тела, отравляющие все органы, в особенности, мозг. Больные сахарным диабетом мучаются от жажды и сухости в ротовой полости, частого мочеиспускания, слабости, утомляемости, сонливости. Некоторые пациенты постоянно чувствуют голод и страдают от повышенного аппетита и зуда во всем теле. В результате у них возникают ранки, которые долго не заживают. При первом типе сахарного диабета человек может резко похудеть, а при втором – быстро полнеет. Инсулинозависимые диабеты развиваются, как правило, очень быстро или даже внезапно, а инсулинонезависимые – постепенно с умеренно выраженными симптомами. При неблагоприятном течении диабетической болезни возможно развитие сердечно-сосудистых заболеваний, атеросклероза ног, снижение зрения. Может появиться нейропатия (утрата чувствительности, судороги в руках или ногах), сухость и шелушение кожи, заболевание почек или печени, язвенные болезни стоп, инфекционные гнойничковые и грибковые проявления. Самое страшное последствие диабета – это кома. Увеличение и понижение содержания глюкозы приводят как к неприятным для человека кратковременным последствиям, так и к пожизненным хроническим заболеваниям тереотоксическому кризу. А критические по содержанию повышение или понижение сахара могут вызвать даже летальный исход.
Вхождение в фазу полового созревания и начало первой менструации каждая женщина переживает по-своему, но есть и то, что объединяет всех представительниц прекрасного пола

242
Нарушение углеводного обмена — причины появления симптома, способы лечения
Общие сведения
Углеводный обмен отвечает за процесс усвоения углеводов в организме, их расщепление с образованием промежуточных и конечных продуктов, а также новообразование из соединений, не являющихся углеводами, или превращение простых углеводов в более сложные. Основная роль углеводов определяется их энергетической функцией.
Глюкоза крови является непосредственным источником энергии в организме. Быстрота ее распада и окисления, а также возможность быстрого извлечения из депо обеспечивают экстренную мобилизацию энергетических ресурсов при стремительно нарастающих затратах энергии в случаях эмоционального возбуждения, при интенсивных мышечных нагрузках.
При снижении уровня глюкозы в крови развиваются:
-
Судороги;
-
бред;
-
потеря сознания;
-
вегетативные реакции (усиленное потоотделение, изменение просвета кожных сосудов).
Это состояние получило название «гипогликемическая кома». Введение в кровь глюкозы быстро устраняет данные расстройства.
Метаболизм углеводов в организме человека состоит из следующих процессов:
-
Расщепление в пищеварительном тракте поступающих с пищей поли- и дисахаридов до моносахаридов, дальнейшее всасывание моносахаридов из кишечника вкровь.
-
Синтез и распад гликогена в тканях (гликогенез и гликогенолиз).
-
Гликолиз (распад глюкозы).
-
Анаэробный путь прямого окисления глюкозы (пентозный цикл).
-
Взаимопревращение гексоз.
-
Анаэробный метаболизм пирувата.
-
Глюконеогенез — образование углеводов из неуглеводных продуктов.
Нарушения углеводного обмена
Всасывание углеводов нарушается при недостаточности амилолитических ферментов желудочно-кишечного тракта (амилаза панкреатического сока). При этом поступающие с пищей углеводы не расщепляются до моносахаридов и не всасываются. В результате у пациента развивается углеводное голодание.
Всасывание углеводов страдает также при нарушении фосфорилирования глюкозы в кишечной стенке, возникающем при воспалении кишечника, при отравлении ядами, блокирующими фермент гексокиназу (флоридзин, монойодацетат). Не происходит фосфорилирования глюкозы в кишечной стенке и она не поступает в кровь.
Всасывание углеводов особенно легко нарушается у детей грудного возраста, у которых еще не вполне сформировались пищеварительные ферменты и ферменты, обеспечивающие фосфорилирование и дефосфорилирование.
Причины нарушения углеводного обмена, вследствие нарушения гидролиза и всасывания углеводов:
-
Гипоксия
-
нарушение функций печени — нарушение образования гликогена из молочной кислоты — ацидоз (гиперлакцидемия).
-
гиповитаминоз В1.
Нарушение синтеза и расщепления гликогена
Синтез гликогена может изменяться в сторону патологического усиления или снижения. Усиление распада гликогена происходит при возбуждении центральной нервной системы. Импульсы по симпатическим путям идут к депо гликогена (печень, мышцы) и активируют гликогенолиз и мобилизацию гликогена. Кроме того, в результате возбуждения центральной нервной системы повышается функция гипофиза, мозгового слоя надпочечников, щитовидной железы, гормоны которых стимулируют распад гликогена.
Повышение распада гликогена при одновременном увеличении потребления мышцами глюкозы происходит при тяжелой мышечной работе. Снижение синтеза гликогена происходит при воспалительных процессах в печени: гепатитах, в ходе которых нарушается ее гликоген-образовательная функция.
При недостатке гликогена тканевая энергетика переключается на жировой и белковый обмены. Образование энергии за счет окисления жира требует много кислорода; в противном случае в избытке накапливаются кетоновые тела и наступает интоксикация. Образование же энергии за счет белков ведет к потере пластического материала. Гликогеноз это нарушение обмена гликогена, сопровождающееся патологическим накоплением гликогена в органах.
Болезнь Гирке гликогеноз, обусловленный врожденным недостатком глюкозо-6-фосфатазы — фермента, содержащегося в клетках печени и почек.
Гликогеноз при врожденном дефиците α-глюкозидазы. Этот фермент отщепляет глюкозные остатки от молекул гликогена и расщепляет мальтозу. Он содержится в лизосомах и разобщен с фосфорилазой цитоплазмы.
При отсутствии α-глюкозидазы в лизосомах накапливается гликоген, который оттесняет цитоплазму, заполняет всю клетку и разрушает ее. Содержание глюкозы в крови нормальное. Гликоген накапливается в печени, почках, сердце. Обмен веществ в миокарде нарушается, сердце увеличивается в размерах. Больные дети рано умирают от сердечной недостаточности.
Нарушения промежуточного обмена углеводов
К нарушению промежуточного обмена углеводов могут привести:
Гипоксические состояния (например, при недостаточности дыхания или кровообращения, при анемиях), анаэробная фаза превращения углеводов преобладает над аэробной фазой. Происходит избыточное накопление в тканях и крови молочной и пировиноградной кислот. Содержание молочной кислоты в крови возрастает в несколько раз. Возникает ацидоз. Нарушаются ферментативные процессы. Снижается образование АТФ.
Расстройства функции печени, где в норме часть молочной кислоты ресинтезируется в глюкозу и гликоген. При поражении печени этот ресинтез нарушается. Развиваются гиперлакцидемия и ацидоз.
Гиповитаминоз В1. Нарушается окисление пировиноградной кислоты, так как витамин B1 входит в состав кофермента, участвующего в этом процессе. Пировиноградная кислота накапливается в избытке и частично переходит в молочную кислоту, содержание которой также возрастает. При нарушении окисления пировиноградной кислоты снижается синтез ацетилхолина и нарушается передача нервных импульсов. Уменьшается образование из пировиноградной кислоты ацетилкоэнзима А. Пировиноградная кислота является фармакологическим ядом для нервных окончаний. При увеличении ее концентрации в 2-3 раза возникают нарушения чувствительности, невриты, параличи и др.
При гиповитаминозе B1 нарушается также и пентозофосфатный путь обмена углеводов, в частности образование рибозы.
Гипергликемия
Гипергликемия это повышение уровня сахара крови выше нормального. В зависимости от этиологических факторов различают следующие виды гипергликемий:
Алиментарная гипергликемия. Развивается при приеме больших количеств сахара. Этот вид гипергликемии используют для оценки состояния углеводного обмена (так называемая сахарная нагрузка). У здорового человека после одномоментного приема 100-150 г сахара содержание глюкозы в крови нарастает, достигая максимума — 1,5-1,7 г/л (150-170 мг%) через 30-45 мин. Затем уровень сахара крови начинает падать и через 2 ч снижается до нормы (0,8-1,2 г/л), а через 3 ч оказывается даже несколько сниженным.
Эмоциональная гипергликемия. При резком преобладании в коре головного мозга раздражительного процесса над тормозным возбуждение иррадиирует на нижележащие отделы центральной нервной системы. Поток импульсов по симпатическим путям, направляясь к печени, усиливает в ней распад гликогена и тормозит переход углеводов в жир. Одновременно возбуждение воздействует через гипоталамические центры и симпатическую нервную систему на надпочечники. Происходит выброс в кровь больших количеств адреналина, стимулирующего гликогенолиз.
Гормональные гипергликемии. Возникают при нарушении функции эндокринных желез, гормоны которых участвуют в регуляции углеводного обмена. Например, гипергликемия развивается при повышении продукции глюкагона — гормона α-клеток островков Лангерганса поджелудочной железы, который, активируя фосфорилазу печени, способствует гликогенолизу. Сходным действием обладает адреналин. К гипергликемии ведет избыток глюкокортикоидов (стимулируют глюконеогенез и тормозят гексокиназу) и соматотропного гормона гипофиза (тормозит синтез гликогена, способствует образованию ингибитора гексокиназы и активирует инсулиназу печени).
Гипергликемии при некоторых видах наркоза. При эфирном и морфинном наркозах происходит возбуждение симпатических центров и выход адреналина из надпочечников; при хлороформном наркозе к этому присоединяется нарушение гликогенообразовательной функции печени.
Гипергликемия при недостаточности инсулина является наиболее стойкой и выраженной. Ее воспроизводят в эксперименте путем удаления поджелудочной железы. Однако при этом дефицит инсулина сочетается с тяжелым расстройством пищеварения. Поэтому более совершенной экспериментальной моделью инсулиновой недостаточности является недостаточность, вызванная введением аллоксана (C4h3N2O4), который блокирует SH-группы. В β-клетках островков Лангерганса поджелудочной железы, где запасы SH-групп невелики, быстро наступает их дефицит и инсулин становится неактивным.
Экспериментальную недостаточность инсулина можно вызвать дитизоном, блокирующим цинк в β-клетках островков Лангерганса, что ведет к нарушению образования гранул из молекул инсулина и его депонирования. Кроме того, в β-клетках образуется дитизонат цинка, который повреждает молекулы инсулина.
Недостаточность инсулина может быть панкреатической и внепанкреатической. Оба эти вида инсулиновой недостаточности могут вызвать сахарный диабет.
Панкреатическая инсулиновая недостаточность
Этот тип недостаточности развивается при разрушении поджелудочной железы:
В этих случаях нарушаются все функции поджелудочной железы, в том числе и способность вырабатывать инсулин. После панкреатита в 16-18% случаев развивается инсулиновая недостаточность в связи с избыточным разрастанием соединительной ткани, которая нарушает снабжение клеток кислородом.
К инсулиновой недостаточности ведет местная гипоксия островков Лангерганса (атеросклероз, спазм сосудов), где в норме очень интенсивное кровообращение. При этом дисульфидные группы в инсулине переходят в сульфгидрильные и он не оказывает гипогликемического эффекта). Предполагают, что причиной инсулиновой недостаточности может послужить образование в организме при нарушении пуринового обмена аллоксана, близкого по структуре к мочевой кислоте.
Инсулярный аппарат может истощаться после предварительного повышения функции, например при излишнем употреблении в пищу легкоусвояемых углеводов, вызывающих гипергликемию, при переедании. В развитии панкреатической инсулиновой недостаточности важная роль принадлежит исходной наследственной неполноценности инсулярного аппарата.
Внепанкреатическая инсулиновая недостаточность
Этот тип недостаточности может развиться при повышенной активности инсулиназы: фермента, расщепляющего инсулин и образующегося в печени к началу полового созревания.
К недостаточности инсулина могут привести хронические воспалительные процессы, при которых в кровь поступает много протеолитических ферментов, разрушающих инсулин.
Избыток гидрокортизона, тормозящего гексокиназу, снижает действие инсулина. Активность инсулина снижается при избытке в крови неэстерифицированных жирных кислот, которые оказывают на него непосредственное тормозящее влияние.
Причиной недостаточности инсулина может послужить чрезмерно прочная его связь с переносящими белками в крови. Инсулин, связанный с белком, не активен в печени и мышцах, но оказывает обычно действие на жировую ткань.
В ряде случаев при сахарном диабете содержание инсулина в крови нормально или даже повышено. Предполагают, что диабет при этом обусловлен присутствием в крови антагониста инсулина, однако природа этого антагониста не установлена. Образование в организме антител против инсулина ведет к разрушению этого гормона.
Сахарный диабет
Углеводный обмен при сахарном диабете характеризуется следующими особенностями:
-
Резко снижен синтез глюкокиназы, которая при диабете почти полностью исчезает из печени, что ведет к уменьшению образования глюкозо-6-фосфата в клетках печени. Этот момент наряду со сниженным синтезом гликогенсинтетазы обусловливает резкое замедление синтеза гликогена. Происходит обеднение печени гликогеном. При недостатке глюкозо-6-фосфата тормозится пентозофосфатный цикл;
-
Активность глюкозо-6-фосфатазы резко возрастает, поэтому глюкозо-6-фосфат дефосфорилируется и поступает в кровь в виде глюкозы;
-
Тормозится переход глюкозы в жир;
-
Понижается прохождение глюкозы через клеточные мембраны, она плохо усваивается тканями;
-
Резко ускоряется глюконеогенез — образование глюкозы из лактата, пирувата, аминокислот жирных кислот и других продуктов неуглеводного обмена. Ускорение глюконеогенеза при сахарном диабете обусловлено отсутствием подавляющего влияния (супрессии) инсулина на ферменты, обеспечивающие глюконеогенез в клетках печени и почек: пируваткарбоксилазу, глюкозо-6-фосфатазу.
Таким образом, при сахарном диабете имеют место избыточная продукция и недостаточное использование глюкозы тканями, вследствие чего возникает гипергликемия. Содержание сахара в крови при тяжелых формах может достигать 4-5 г/л (400-500 мг%) и выше. При этом резко возрастает осмотическое давление крови, что ведет к обезвоживанию клеток организма. В связи с обезвоживанием глубоко нарушаются функции центральной нервной системы (гиперосмолярная кома).
Сахарная кривая при диабете по сравнению с таковой у здоровых значительно растянута во времени. Значение гипергликемии в патогенезе заболевания двояко. Она играет адаптивную роль, так как при ней тормозится распад гликогена и частично усиливается его синтез. При гипергликемии глюкоза лучше проникает в ткани и они не испытывают резкого недостатка углеводов. Гипергликемия имеет и отрицательное значение.
При ней повышается концентрация глюко- и мукопротеидов, которые легко выпадают в соединительной ткани, способствуя образованию гиалина. Поэтому для сахарного диабета характерно раннее поражение сосудов атеросклерозом. Атеросклеротический процесс захватывает коронарные сосуды сердца (коронарная недостаточность), сосуды почек (гломерулонефриты). В пожилом возрасте сахарный диабет может сочетаться с гипертонической болезнью.
Глюкозурия
В норме глюкоза содержится в провизорной моче. В канальцах она реабсорбируется в виде глюкозофосфата, для образования которого необходима гексокиназа, и после дефосфорилирования поступает в кровь. Таким образом, в окончательной моче сахара в нормальных условиях не содержится.
При диабете процессы фосфорилирования и дефосфорилирования глюкозы в канальцах почек не справляются с избытком глюкозы в первичной моче. Развивается глюкозурия. При тяжелых формах сахарного диабета содержание сахара в моче может достигать 8-10%. Осмотическое давление мочи повышено; в связи с этим в окончательную мочу переходит много воды.
Суточный диурез возрастает до 5-10 л и более (полиурия). Развивается обезвоживание организм, развивается усиленная жажда (полидипсия). При нарушении углеводного обмена следует обратиться к эндокринологу за профессиональной помощью. Врач подберет необходимое медикаментозное лечение и разработает индивидуальную диету.
|
|
При некоторых состояниях можно наблюдать повышение содержания глюкозы в крови – гипергликемию, а также понижение концентрации глюкозы – гипогликемию. Гипергликемия является довольно частым симптомом различных заболеваний, прежде всего связанных с поражением эндокринной системы. Сахарный диабет. В регуляции гликолиза и глюконеогенеза большую роль играет инсулин. При недостаточности содержания инсулина возникает заболевание, которое носит название «сахарный диабет»: повышается концентрация глюкозы в крови (гипергликемия), появляется глюкоза в моче (глюкозурия) и уменьшается содержание гликогена в печени. Мышечная ткань при этом утрачивает способность утилизировать глюкозу крови. В печени при общем снижении интенсивности биосинтетических процессов: биосинтеза белков, синтеза жирных кислот из продуктов распада глюкозы – наблюдается усиленный синтез ферментов глюконеогенеза. При введении инсулина больным диабетом происходит коррекция метаболических сдвигов: нормализуется проницаемость мембран мышечных клеток для глюкозы, восстанавливается соотношение между гликолизом и глюко-неогенезом. Инсулин контролирует эти процессы на генетическом уровне как индуктор синтеза ключевых ферментов гликолиза: гексокиназы, фос-фофруктокиназы и пируваткиназы. Инсулин также индуцирует синтез гли-когенсинтазы. Одновременно инсулин действует как репрессор синтеза ключевых ферментов глюконеогенеза. Следует отметить, что индукторами синтеза ферментов глюконеогенеза служат глюкокортикоиды. В связи с этим при инсулярной недостаточности и сохранении или даже повышении секреции кортикостероидов (в частности, при диабете) устранение влияния инсулина приводит к резкому повышению синтеза и концентрации ферментов глюконеогенеза, особенно фосфоенолпируват-карбоксикиназы, определяющей возможность и скорость глюконеогенеза в печени и почках. Развитие гипергликемии при диабете можно рассматривать также как результат возбуждения метаболических центров в ЦНС импульсами с хе-морецепторов клеток, испытывающих энергетический голод в связи с недостаточным поступлением глюкозы в клетки ряда тканей. Роль системы фруктозо-2,6-бисфосфата в регуляции метаболизма углеводов, а также нарушения ее функционирования при сахарном диабете см. главу 16. Гипергликемия может возникнуть не только при заболевании поджелудочной железы, но и в результате расстройства функции других эндокринных желез, участвующих в регуляции углеводного обмена. Так, гипергликемия может наблюдаться при гипофизарных заболеваниях, опухолях коркового вещества надпочечников, гиперфункции щитовидной железы. Иногда гипергликемия появляется во время беременности. Наконец, гипергликемия возможна при органических поражениях ЦНС, расстройствах мозгового кровообращения, болезнях печени воспалительного или дегенеративного характера. Поддержание постоянства уровня глюкозы в крови, как отмечалось,– важнейшая функция печени, резервные возможности которой в этом отношении весьма велики. Поэтому гипергликемия, обусловленная нарушением функции печени, выявляется обычно при тяжелых ее поражениях. Большой клинический интерес представляет изучение реактивности организма на сахарную нагрузку у здорового и больного человека. В связи с этим в клинике довольно часто исследуют изменения во времени уровня глюкозы в крови, обычно после приема per os 50 г или 100 г глюкозы, растворенной в теплой воде,– так называемая сахарная нагрузка. При оценке построенных гликемических кривых обращают внимание на время максимального подъема, высоту этого подъема и время возврата концентрации глюкозы к исходному уровню. Для оценки гликемических кривых введено несколько показателей, из которых наиболее важное значение имеет коэффициент Бодуэна: где А – уровень глюкозы в крови натощак; В – максимальное содержание глюкозы в крови после нагрузки глюкозой. В норме этот коэффициент составляет около 50%. Значения, превышающие 80%, свидетельствуют о серьезном нарушении обмена углеводов. Гипогликемия. Нередко гипогликемия связана с понижением функций тех эндокринных желез, повышение функций которых приводит, как отмечалось, к гипергликемии. В частности, гипогликемию можно наблюдать при гипофизарной кахексии, аддисоновой болезни, гипотиреозе. Резкое снижение уровня глюкозы в крови отмечается при аденомах поджелудочной железы вследствие повышенной продукции инсулина β-клетками панкреатических островков. Кроме того, гипогликемия может быть вызвана голоданием, продолжительной физической работой, приемом β-ганглиоблока-торов. Низкий уровень глюкозы в крови иногда отмечается при беременности, лактации. Гипогликемия может возникнуть при введении больным сахарным диабетом больших доз инсулина. Как правило, она сопровождает почечную глюкозурию, возникающую вследствие снижения «почечного порога» для глюкозы. Глюкозурия. Обычно присутствие глюкозы в моче (глюкозурия) является результатом нарушения углеводного обмена вследствие патологических изменений в поджелудочной железе (сахарный диабет, острый панкреатит и т.д.). Реже встречается глюкозурия почечного происхождения, связанная с недостаточностью резорбции глюкозы в почечных канальцах. Как временное явление глюкозурия может возникнуть при некоторых острых инфекционных и нервных заболеваниях, после приступов эпилепсии, сотрясения мозга. Отравления морфином, стрихнином, хлороформом, фосфором также обычно сопровождаются глюкозурией. Наконец, необходимо помнить о глюкозурии алиментарного происхождения, глюкозурии беременных и глюкозурии при нервных стрессовых состояниях (эмоциональная глюкозурия). Изменение углеводного обмена при гипоксических состояниях. Отставание скорости окисления пирувата от интенсивности гликолиза наблюдается чаще всего при гипоксических состояниях, обусловленных различными нарушениями кровообращения или дыхания, высотной болезнью, анемией, понижением активности системы тканевых окислительных ферментов при некоторых инфекциях и интоксикациях, гипо- и авитаминозах, а также в результате относительной гипоксии при чрезмерной мышечной работе. При усилении гликолиза происходит накопление пирувата и лактата в крови, что сопровождается обычно изменением кислотно-основного равновесия, уменьшением щелочных резервов крови. Увеличение содержания лактата и пирувата в крови может наблюдаться также при поражениях паренхимы печени (поздние стадии гепатита, цирроз печени и т.п.) в результате торможения процессов глюконеогенеза в печени. Гликогенозы. Ряд наследственных болезней связан с нарушением обмена гликогена. Эти болезни получили название гликогенозов. Они возникают в связи с дефицитом или полным отсутствием ферментов, катализирующих процессы распада или синтеза гликогена, и характеризуются избыточным его накоплением в различных органах и тканях (табл. 10.2). Гликогеноз I типа (болезнь Гирке) встречается наиболее часто, обусловлен наследственным дефектом синтеза фермента глюкозо-6-фосфатазы в печени и почках. Болезнь наследуется по аутосомно-рецессивному типу. Патологические симптомы появляются уже на первом году жизни ребенка: увеличена печень, нередко увеличены почки. В результате гипогликемии появляются судороги, задержка роста, возможен ацидоз. В крови – повышенное количество лактата и пирувата. Введение адреналина или глюка-гона вызывает значительную гиперлактатацидемию, но не гипергликемию, так как глюкозо-6-фосфатаза в печени отсутствует и образования свободной глюкозы не происходит. Предыдущая страница | Следующая страница СОДЕРЖАНИЕ |
Нарушение обмена веществ: симптомы, причины, признаки
Обмен веществ, осуществляемый в организме человека, представляет собой череду сменяющих друг друга химических реакций. Постоянно происходящее превращение энергии и различных веществ является основой нормальной жизнедеятельности организма.
О нарушении обмена веществ смело может заявлять любой врач, к которому обратился пациент, поскольку все болезни в той или иной мере протекают с нарушениями метаболизма.
Нарушение обмена веществ в организме может быть белкового, углеводного, жирового, минерального и др. характера, но деление это является условным и основополагается на превалирующем патогенетическом процессе – все виды обмена взаимосвязаны между собой и существенно влияют друг на друга.
Патогенетическая основа нарушений обмена веществ – это изменение гармоничного взаимодействия веществ, участвующих в обмене, избыток или недостаток этих веществ, а также нарушения реакций превращения, приводящих к накоплению промежуточных продуктов и диспропорциональному образованию конечных продуктов обмена.
Причины нарушения обмена веществ разнообразны, ведущую роль среди которых играют наследственность и патологии органов и систем, регулирующих обменные процессы.
Нарушения белкового обмена
Белки, как известно, являются основным строительным материалом для организма человека и играют ведущую роль в осуществлении его жизнедеятельности. Все без исключения патологические процессы протекают с нарушением белкового обмена, который возможен на любом из этапов его превращения в организме:
- Нарушения процессов всасывания белков, которые приводят к алиментарной недостаточности (дистрофия тканей кишечника, голодание, несбалансированный состав пищи по аминокислотной составляющей).
- Нарушение процессов синтезирования белков приобретенного и наследственного характера, приводящее к изменению количества синтезированного белка или к образованию белка с измененной молекулярной структурой (гормональные изменения, дисфункция нервной и иммунной системы, геномные ошибки).
- Нарушения обмена аминокислот, приводящее к дисбалансу процессов трансаминирования (образования) и окислительного дезаминирования (разрушения) аминокислот (беременность, лечение сульфаниламидами, голодание, тяжелые заболевания печени, панкреатит, инфаркт миокарда, гипоксия, голодание, травмы).
- Нарушения терминальных стадий белкового обмена, приводящих к накоплению азотистых продуктов распада и замедлению выведения их из организма (заболевания печени и почек, гипоксия, лейкозы, геномные ошибки).
- Нарушения белкового состава крови, приводящее к изменению их общего количества или дисбалансу соотношения их фракций (практически все патологические состояния, врожденные аномалии образования протеинов, голодание, кровопотеря, потеря белков с мочой).
Признаки нарушения белкового обмена
Симптомы нарушения обмена веществ белкового характера проявляются как при избытке данного нутриента, так и при его недостатке:
| Избыток белка | Дефицит белка |
|
|
Заболевания, возникающие при нарушении белкового обмена веществ
| Избыток белка | Дефицит белка |
| 1. Подагра | 1. Квашиокор |
|
|
| 2. Ожирение | 2. Алиментарная дистрофия |
|
|
Нарушения углеводного обмена
Углеводы осуществляют важнейшую энергетическую функцию и питают клетки мозга. Именно углеводы моментально компенсируют потерю энергии при различных нагрузках и стрессовых ситуациях. Организм человека сильно реагирует как на увеличение уровня глюкозы, так и на падение глюкозы крови, а заболевания, к которым приводят нарушения обмена веществ углеводного характера, зачастую сопровождают человека пожизненно. Более того, критические значения сахара крови могут обернуться летальным исходом.
Нарушения углеводного обмена возможны по следующим типам:
- Нарушение гидролиза (переваривания) углеводов и их всасывания, которое в конечном итоге приводит к углеводному голоданию организма (ферментативная недостаточность, детский возраст, воспаление тонкого кишечника, отравление ядами, гипоксия, дисфункция печени, гиповитаминоз В1).
- Нарушение синтезирования гликогена – повышенный распад или уменьшение его синтеза, приводящее к получению энергии за счет белка и интоксикации организма (перевозбуждение ЦНС, тяжелый физический труд, гепатиты).
- Нарушение обмена гликогена, при котором происходит патологическое накопление гликогена в тканях (врожденная ферментативная недостаточность).
- Нарушения промежуточного углеводного обмена, следствием которого является ацидоз и нарушение ферментативных процессов (гипоксия, гиповитаминоз В1, печеночная недостаточность).
- Повышение уровня глюкозы в крови, которое протекает в нескольких вариантах – алиментарная гипергликемия на фоне употребления большого количества сахара, гормональная гипергликемия при эндокринной патологии, эмоциональная гипергликемия на фоне сильных эмоциональных переживаний, панкреатическая и внепанкреатическая инсулинодефицитная гипергликемия, приводящая к сахарному диабету, гипергликемия на фоне некоторых видов наркоза (эфир, морфин, хлороформ).
Признаки нарушения углеводного обмена
Симптомы нарушения обмена веществ углеводного характера имеют место при недостатке и избытке сахаров:
| Избыток углеводов | Дефицит углеводов |
|
|
Заболевания, возникающие при нарушении углеводного обмена
| Избыток углеводов | Дефицит углеводов |
| 1. Сахарный диабет | 1. Гипогликемия |
|
|
| 2. Ожирение | 2. Болезнь Гирке |
|
|
Нарушения жирового обмена
Жиры играют не менее важную функцию в организме, чем другие нутриенты. Жировую основу имеют все гормоны человека – благодаря жирам поддерживается внутренний гомеостаз. Присутствуют жиры и в нервной ткани, обеспечивая стабильность клеточных структур и нормальную передачу нервных импульсов.
Нарушения жирового обмена может происходить вследствие:
- Недостаточности всасывания жиров в тонком кишечнике (дисфункция поджелудочной железы, недостаток желчных кислот, энтериты, гиповитаминозы, панкреатит).
- Пониженной активности липопротеинлипазы (гиперлипопротеинемия I и V типа).
- Ослабления функции гипофиза, щитовидной железы и половых желез.
- Поражения вегетативных центров гипоталамо-гипофизарной системы и коры надпочечников (гипофизарная кахексия, аддисонова болезнь).
- Изменения трофической функции нервной системы (липодистрофия, липоматоз).
- Повышенного образования кетоновых тел (кетоз).
- Действия ионизирующего излучения.
- Переедания, при котором общая калорийность пищи превалирует над энергетическими затратами.
Признаки нарушения жирового обмена
Симптомы нарушения обмена веществ жирового характера клинически проявляются при недостаточности и избытке липидов:
| Избыток жиров | Дефицит жиров |
|
|
Заболевания, возникающие при нарушении жирового обмена веществ
| Избыток жиров | Дефицит жиров |
| 1. Жировой гепатоз | 1. Истощение нервной системы |
|
|
| 2. Атеросклероз | 2. Половая дисфункция |
|
|
Нарушения водного обмена
Вода – незаменимая и важнейшая жидкость гомеостаза, составляющая чуть больше половины массы тела взрослого человека. Нормальный водный баланс означает примерно одинаковое количество (около 2,5 литра) поступившей в организм и выделившейся из организма воды.
Нарушение водного обмена может протекать в виде обезвоживания и патологической задержки жидкости в организме. Оба состояния опасны и серьезно нарушают здоровье человека: так, при обезвоживании возникает сгущение крови, страдают все органы и ткани, особенно ЦНС и ЖКТ, при отеках нарушается функция выделительной системы, уменьшается сердечный выброс и повышается давление.
| Обезвоживание | Задержка воды в организме |
При недостаточном поступлении в организм жидкости:
| При водном отравлении: |
При недостатке электролитов:
| При отеках:
|
| При гипервентиляции легких- гипервентиляционный синдром у детей | |
При полиурии:
|
Нарушение минерального обмена
Минералы являются структурными составляющим клеток и присутствуют в ферментах, витаминах, гормонах, пигментах. Это биокатализаторы большинства физиологических реакций и стабилизаторы кислотно-основного состояния организма.
Минеральный обмен в той или иной степени нарушен практически у восьмидесяти процентов населения. Причин данного нарушения много: стрессы, ускоренный темп жизни в мегаполисах, неблагоприятная окружающая среда, увлечение диетами, несбалансированное питание, нервозность, вредные привычки. Дисбаланс минерального состава приводит к нарушениям обмена нутриентов, гиповитаминозам и ферментопатиям, ослаблению иммунитета и поражению органов и тканей.
Нарушения минерального обмена проявляются следующими симптомами:
- выпадение волос
- ломкость ногтей
- угри и прыщи
- бессонница
- падение зрения
- снижение иммунитета
- аллергические реакции
- снижение иммунитета
- расстройства стула
- снижение либидо
Нарушение минерального обмена может происходить по каждому микро- или макроэлементу, наиболее распространены следующие патологические состояния:
- Кальциноз – нарушение обмена кальция. В основе патологии лежит отложение солей кальция в клетках или межклеточном веществе. Это может привести к функциональным нарушениям тех органов и структур организма, где происходит отложение кальция.
- Болезнь Вильсона – нарушение обмена меди. Увеличивается содержание меди в клетках, особенно в гепатоцитах и базальных ядрах мозга, и происходит дистрофия пораженных структур.
- Гиперкалиемия – увеличение уровня калия в крови. Часто возникает при поражении коры надпочечников и приводит к нарушениям функции сердечно-сосудистой системы.
Распространены и нарушения обмена веществ, связанные с дефицитом иди избытком определенных витаминов в организме (см. авитаминоз и гиповитаминоз — симптомы, причины). Гиповитаминозы и автиминозы часто диагностируются у детей, гипервитаминозы – более редкие патологии, характерные для людей, бездумно употребляющих витамины или не соблюдающих дозировки применения.
Лечение нарушения обмена веществ, особенно неосложненного, не имеющего врожденного характера, связанного с алиментарным фактором, может быть проведено всего лишь коррекцией рациона и режима питания. Однако диагностировать нарушения обмена веществ в начале своего развития сложно. Зато легко предотвратить подобные состояния, ведя здоровый образ жизни и следуя принципам здорового питания!