Клинические рекомендации по диагностике и лечению системного амилоидоза. Клиническая фармакология и терапия
Л.В. Лысенко (Козловская), В.В. Рамеев, С.В. Моисеев, О.В. Благова, Э.И. Богданов, Г.Е. Гендлин, Д.А. Гришина, А.Я. Гудкова, Е.В. Захарова, О.Е. Зиновьева, О.М. Моисеева, С.С. Никитин, В.А. Парфенов, Н.А. Супонева, С.Н. Терещенко
- DOI
- 10.32756/ 0869-5490-2020-1-13-24
- Количество просмотров
- 13085
В клинических рекомендациях, подготовленных специалистами различного профиля, рассматриваются методы диагностики и лечениясистемного амилоидоза, в том числе АА (вто-ричный амилоидоз при хронических воспалительных заболеваниях, включая ревматоидныйартрит, анкилозирующий спондилит, аутовоспалительные заболевания, хроническиенагноения, злокачественные опухоли и др. ), AL (амилоидоз при плазмоклеточных дискразиях – идиопатический, при миеломной болезни и макроглобулинемии Вальденстрема) иATTR (транстиретиновый; семейные формыполиневропатического, кардиопатического идругого амилоидоза, системный старческийамилоидоз). Диагноз амилоидоза, которыйможно заподозрить на основании клиническихданных, необходимо подтвердить при гистологическом исследовании (окрашивание препаратов ткани конго-красным с последующей микроскопией в поляризованном свете). Чтобы замедлить или приостановить прогрессирование амилоидоза любого типа, необходимо добиться уменьшения количества (или, если возможно, удаления) белков-предшественников путем лечения хронического воспаленияпри АА-амилоидозе или подавления пролиферации клона плазматических клеток для уменьшения продукции легких цепей иммуно-глобулинов при AL-амилоидозе. Для замедления прогресирования ATTR-амилоидоза упациентов с полиневропатией применяют тафамидис, который ингибирует диссоциацию мутантного транстиретина и снижает его амилоидогенность.
), AL (амилоидоз при плазмоклеточных дискразиях – идиопатический, при миеломной болезни и макроглобулинемии Вальденстрема) иATTR (транстиретиновый; семейные формыполиневропатического, кардиопатического идругого амилоидоза, системный старческийамилоидоз). Диагноз амилоидоза, которыйможно заподозрить на основании клиническихданных, необходимо подтвердить при гистологическом исследовании (окрашивание препаратов ткани конго-красным с последующей микроскопией в поляризованном свете). Чтобы замедлить или приостановить прогрессирование амилоидоза любого типа, необходимо добиться уменьшения количества (или, если возможно, удаления) белков-предшественников путем лечения хронического воспаленияпри АА-амилоидозе или подавления пролиферации клона плазматических клеток для уменьшения продукции легких цепей иммуно-глобулинов при AL-амилоидозе. Для замедления прогресирования ATTR-амилоидоза упациентов с полиневропатией применяют тафамидис, который ингибирует диссоциацию мутантного транстиретина и снижает его амилоидогенность.
Определение, классификация, группы риска и принципы диагностики
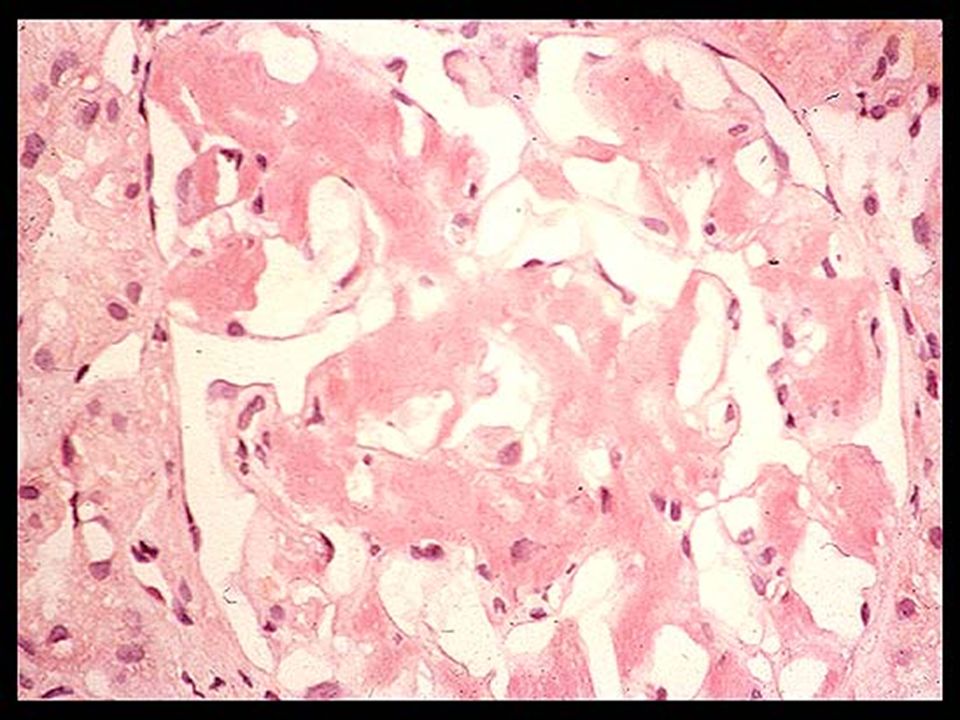
Амилоидоз – группа заболеваний, отличительным признаком которых является отложение в тканях и органах фибриллярного гликопротеида амилоида. Специфическое свойство амилоида, отличающее его от других фибриллярных белков стромы, – способность к двойному лучепреломлению, что проявляется свечением в поляризованном свете предварительно окрашенных конгокрасным препаратов амилоида с изменением красного цвета конгофильных амилоидных отложений на яблочно-зеленый (дихроизм).
В основе амилоидогенеза лежит синтез большого количества нестабильных белковпредшественников, которые
агрегируются с образованием амилоидной фибриллы. Клю чевое значение имеет амилоидогенность основного
белка-предшественника амилоида, специфичного для каждой формы амилоидоза (в настоящее время известно более 30
таких белков), обозначение которого положено в основу современной классификации заболевания (ВОЗ, 2016 г.
| Белок амилоида | Белок-Белок-предшественник | Клиническая форма амилоидоза |
|---|---|---|
| АА | SSA-белок | Вторичный амилоидоз при хронических воспалительных заболеваниях, в том числе периодической болезни и синдроме Макла-Уэллса |
| AL | λ, κ-легкие цепи иммуноглобулинов | Амилоидоз при плазмоклеточных дискразиях – идиопатический, при миеломной болезни и макроглобулинемии Вальденстрема |
| ATTR | Транстиретин | Семейные формы полиневропатического, кардиопатического и др. амилоидоза, системный старческий
амилоидоз амилоидоза, системный старческий
амилоидоз |
| Аβ2М | β2-микроглобулин | Диализный амилоидоз |
| AGel | Гелсолин | Финская семейная амилоидная полиневропатия |
| AApoAI | Аполипопротеин А-I | Амилоидная полиневропатия (III тип по van Allen, 1956 г.) |
| Фибриноген | Амилоидная нефропатия | |
| Aβ2 | β-белок | Болезнь Альцгеймера, синдром Дауна, наследственные кровоизлияния в мозг с амилоидозом |
| APrPScr | Прионовый белок | Болезнь Крейтцфельда-Якоба, болезнь Герстманна-Штраусслера-Шейнкера |
| AANF | Предсердный натрийуретический фактор | Изолированный амилоидоз предсердий |
| AIAPP | Амилин | Изолированный амилоидоз в островках Лангерганса при сахарном диабете 2 типа, инсулиноме |
| ACal | Прокальцитонин | При медуллярном раке щитовидной железы |
| ACys | Цистатин С | Наследственные кровоизлияния в мозг с амилоидозом (Исландия) |
АА-амилоидоз чаще всего развивается при ревматоидном артрите, серонегативных спондилоартропатиях,
аутовоспалительных наследственных периодических лихорадках, в том числе периодической болезни (семейной
средиземноморской лихорадке), а также при хронических нагноениях, туберкулезе.
Клинические формы AL-амилоидоза обусловлены единым этиологическим фактором – В-лимфоцитарной дискразией,
характеризующейся формированием аномального клона плазматических или В-клеток в костном мозге, которые
продуцируют аномальные иммуноглобулины, обладающие амилоидогенностью (легкие цепи моноклонального
иммуноглобулина, чаще λ, реже κ-типа). При первичном AL-амилоидозе плазмоклеточная дискразия относительно более
доброкачественная, в то время как при В-гемобластозах (множественной миеломе, болезни Вальденстрема и др.) она
обладает признаками злокачественной опухоли. Аномальный амилоидогенный клон плазматических клеток может
формироваться также из плазмоцитов, локализующихся вне костного мозга, что может привести к развитию локального
амилоидоза.
ATTR-амилоидоз является необратимо прогрессирующим заболеванием с высокой степенью инвалидизации вследствие тяжелого поражения сердца, периферической и/или автономной полиневропатии. Пациенты обычно умирают в течение 10-12 лет от первых проявлений. Развитие ATTR-амилоидоза обусловлено мутациями в молекуле транстиретина или возрастным нарушением секреции тетрамеров транстиретина печенью. В обоих случаях происходит распад тетрамеров транстиретина до мономеров, обладающих выраженной конформационной нестабильностью.
Рекомендации:
- Скрининг АА-амилоидоза следует проводить в следующих группах риска: серопозитивные и серонегативные
хронические полиартриты (ревматоидный артрит, анкилозирующий спондилоартрит, ювенильный хронический артрит,
псориатический артрит, синдром Рейтера и др.

- Риск АА-амилоидоза у больных с хроническими воспалительными заболеваниями повышается при персистирующем
увеличении уровней маркеров острой фазы воспаления (С-реактивный белок, SAA), наличии анемии хронических
заболеваний (с повышением уровня ферритина крови), особенно в сочетании с суставным синдромом (синовитом)
[4,6-12]. Дина мический контроль за уровнем этих показателей необходим также при мониторировании течения
диагностированного АА-амилоидоза. Для оценки риска развития или прогрессирования АА-амилоидоза в условиях
преимущественного аутовоспаления или с целью выявления субклинической активации воспаления можно определять
сывороточный маркер нейтрофильной активности S100A12 (кальгранулин) [4,13-15].

- Диагностика аутовоспалительных заболеваний предполагает, в первую очередь, проведение генетического исследования на мутации генов MEFV (пирин), NLRP3 (криопирин), TRAPS (рецептор к фактору некроза опухоли альфа), мевалонаткиназы [4,16-25].
- Высокая частота олигосекреторных моноклональных гаммапатий у лиц старше 50 лет требует скринингового обследования этой группы лиц на предмет моноклональных гаммапатий. Наиболее чувствительным и недорогим турбидиметрическим методом для скрининговой диагностики являет Freelite-метод количественной оценки уровня свободных легких цепей иммуноглобулинов. Все больные с плазмоклеточными дискразиями и лимфопролиферативными заболеваниями входят в группу риска AL-амилоидоза [26-34].
- У пациентов с морфологически подтвержденным амилоидозом диагностика AL-амилоидоза предполагает проведение
иммунохимического исследования с применением высокочувствительных методов – иммунофиксации сыворотки и
суточной мочи, количественного определения свободных легких цепей иммуноглобулинов (Freelite) [26-35].

- Помимо выявления моноклональной гаммапатии, диагностика плазмоклеточной дискразии предполагает выявление и оценку количества плазмоцитов костного мозга, а также их структурных особенностей. Применение цитогенетического исследования и иммунофенотипирования плазмоцитов важно для уточнения клональности и злокачественности аберрантного клона плазматических клеток, в особенности в редких случаях неинформативности иммунохимического исследования крови и суточной мочи [26,33-34,36,37].
- Важное значение в диагностике плазмоклеточных дискразий имеют также иммуногистохимические методы выявления патологического клона плазматических клеток. Это особенно важно для диагностики, типирования и лечения локального варианта ALамилоидоза [35].
- ATTR-амилоидоз следует подозревать у пациентов с полиневропатией, необъяснимым чередованием запоров и
диареи, синдромом карпального канала, особенно при наличии полиневропатии, синдрома карпального канала,
кардиомиопатии у родственников.
 Важными симптомами являются геморрагии, фестончатый край зрачка, потеря
массы тела, снижение зрения [38-47].
Важными симптомами являются геморрагии, фестончатый край зрачка, потеря
массы тела, снижение зрения [38-47]. - Диагностика амилоидоза основывается на результатах морфологического исследования [1-2,39,48].
- При системном амилоидозе для диагностики амилоидного поражения органа нет необходимости проводить его биопсию у больных с ранее верифицированным диагнозом амилоидоза по результатам биопсии другого органа. Однако точная диагностика возможна только с помощью морфологического исследования [1,48].
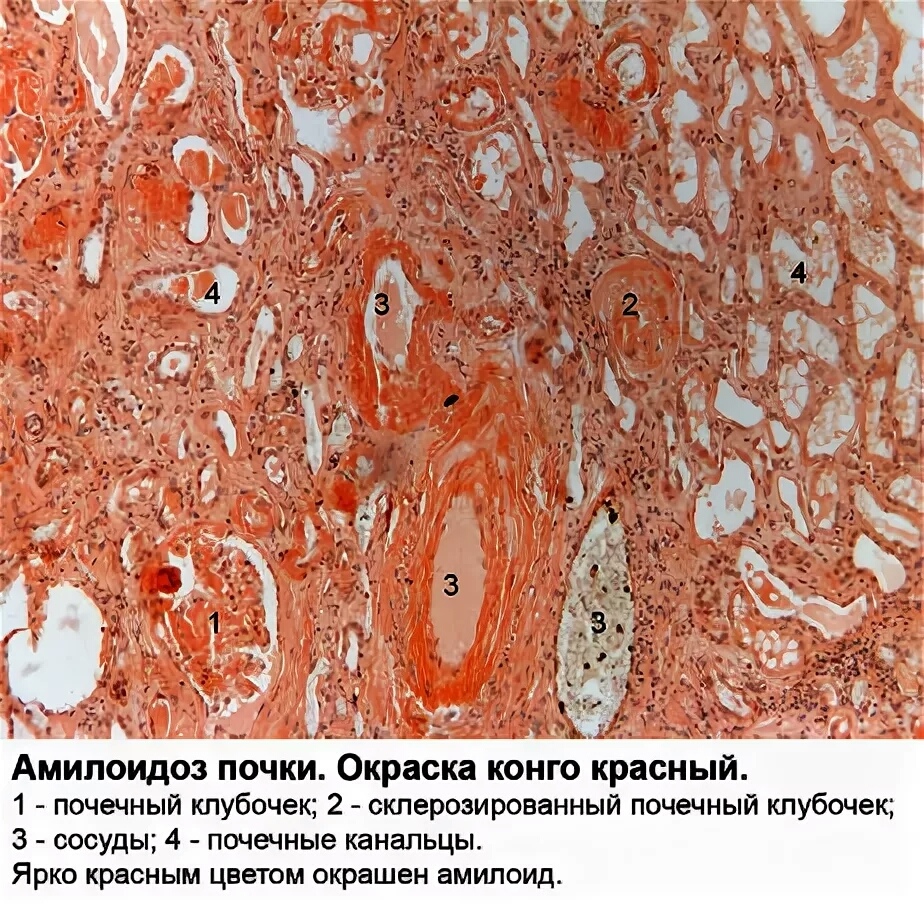
- С целью выявления амилоида необходимо окрашивание препаратов ткани красителем конго-красный с последующей
микроскопией в поляризованном свете. Окончательный диагноз амилоидоза устанавливают при выявлении
конгофильных масс, обладающих способностью к яблочно-зеленому или желтоватому свечению в поляризованном
свете [1,39,48]. Для более точной диагностики амилоидоза применяют также метод окраски тиофлафином Т,
который дает светло-зеленое свечение амилоида [1,2].

- При системном амилоидозе информативна биопсия прямой или двенадцатиперстной кишки (с захватом подслизистого слоя). ATTR-амилоид отличается слабой конгофилией. По этой причине выявить этот тип амилоида нередко удается только при повторных биопсиях из разных органов – аспирационной биопсии подкожной жировой клетчатки, биопсии слюнных желез губ и др. Наиболее эффективна биопсия пораженного органа [1-2,39,48]. У пациентов с синдромом запястного канала исследованию на амилоид необходимо подвергать ткань, удаленную при оперативной декомпрессии запястного канала.
- Не рекомендуется проводить биопсию подкожной жировой клетчатки у больных инсулинозависимым сахарным диабетом, так как в местах иньекций инсулин может агрегировать и формировать амилоидные депозиты [48].
- Для дифференциальной диагностики АА-амилоидоза от AL- и ATTR-амилоидоза используют окрасочные методы при
тщательном учете клинических предпосылок разных типов амилоидоза [48,49].

- Наиболее эффективным методом типирования является иммуногистохимическое исследование. Поскольку некоторые антисыворотки могут давать перекрестные реакции с разными типами амилоида, исследование целесообразно проводить с панелью антисывороток. Для неспециализированных терапевтических и нефрологических стационаров рекомендуется применение панели антисывороток к SAA, разным типам тяжелых цепей иммуноглобулинов, легким цепям иммуноглобулинов λ и κ, транстиретину. Важно также использовать антисыворотки к фибриногену [36,50].
- Для диагностики ATTR-амилоидоза необходимо генетическое исследование на наличие мутации гена транстиретина [39].
Клинические проявления
Для вторичного АА-амилоидоза характерно более раннее начало, чем для AL-амилоидоза (средний возраст больных
составляет около 40 и 65 лет, соответственно). ATTR-амилоидоз, несмотря на наследственную природу,
характеризуется низкой пенетрантностью и также проявляется обычно после 35 лет.
Поражение почек – ведущий клинический признак АА- и AL-амилоидоза, наблюдающийся практически у всех больных. Поражение почек встречается и у больных с многими формами семейного амилоидоза (AFib, ALys, AGel и др.). При ATTR-амилоидозе нефропатия отмечается лишь у 20-23% больных. Клинически амилоидная нефропатия характеризуется неуклонно прогрессирующим течением с последовательной сменой стадий: протеинурия, нефротический синдром, хроническая почечная недостаточность (ХПН). Иногда возможно развитие ХПН без предшествующего нефротического синдрома.
Поражение сердца развивается у подавляющего большинства больных AL-амилоидозом и у 50-60% пациентов с
АTTR-амилоидозом, но не характерно для АА-амилоидоза (рис. 1). При эхокардиографии у больных амилоидозом сердца
наблюдается утолщение межжелудочковой перегородки и стенки левого желудочка (чаще симметричное), которое не
сопровождается электрокардиографическими признаками гипертрофии миокарда. У части больных отмечается снижение
вольтажа зубцов на ЭКГ, хотя отсутствие этого признака не исключает диагноз амилоидоза сердца. Нарушение
диастолической функции левого желудочка (рестриктивный тип) приводит к развитию сердечной недостаточности,
которая быстро прогрессирует, плохо поддается лечению и почти у 50% пациентов оказывается причиной смерти. Кроме
того, у больных амилоидозом сердца часто наблюдаются различные аритмии и нарушения проводимости.
У части больных отмечается снижение
вольтажа зубцов на ЭКГ, хотя отсутствие этого признака не исключает диагноз амилоидоза сердца. Нарушение
диастолической функции левого желудочка (рестриктивный тип) приводит к развитию сердечной недостаточности,
которая быстро прогрессирует, плохо поддается лечению и почти у 50% пациентов оказывается причиной смерти. Кроме
того, у больных амилоидозом сердца часто наблюдаются различные аритмии и нарушения проводимости.
При AL-амилоидозе и особенно ATTR-амилоидозе часто встречается ортостатическая артериальная гипотензия – вариант
сосудистой недостаточности, при которой сосуды теряют способность поддерживать нормальное артериальное давление
в условиях ортостатических нагрузок. Она проявляется ощущением дурноты и потемнением в глазах в ортостазе в
сочетании с резким снижением АД. Обычно этот симптом связан с дисфункцией автономной нервной системы (амилоидоз
нервных сплетений сосудов). Тяжелая ортостатическая гипотензия сопровождается обмороками, а иногда приводит к
развитию острого нарушения мозгового кровообращения.
Она проявляется ощущением дурноты и потемнением в глазах в ортостазе в
сочетании с резким снижением АД. Обычно этот симптом связан с дисфункцией автономной нервной системы (амилоидоз
нервных сплетений сосудов). Тяжелая ортостатическая гипотензия сопровождается обмороками, а иногда приводит к
развитию острого нарушения мозгового кровообращения.
Поражение желудочно-кишечного тракта может проявляться, особенно при AL-амилоидозе, тяжелой диареей или динамической непроходимостью, которые чаще связаны с нарушениями моторики кишечника вследствие дисфункции автономных нервных сплетений. Иногда выявляют изъязвления или перфорацию стенок с возможным кровотечением. При поражении пищевода возможна дисфагия.
Поражение печени при АА- и AL-типах амилоидоза наблюдают практически в 100% случаев. Функция печени чаще остается сохранной, редким признаком амилоидоза печени является внутрипеченочная портальная гипертензия. При некоторых вариантах семейного ALys-амилоидоза описаны тяжелые спонтанные внутрипеченочные кровотечения.
При некоторых вариантах семейного ALys-амилоидоза описаны тяжелые спонтанные внутрипеченочные кровотечения.
Увеличение селезенки, обусловленное амилоидным поражением, отмечается у большинства больных и обычно сопутствует увеличению печени.
Поражение нервной системы, представленное симптомами периферической соматической и автономной невропатии, отмечают у 17-35% больных AL-амилоидозом и практически у всех пациентов с наследственной амилоидной полиневропатией разных типов (ATTR, AApoA1 и др.). В большинстве случаев развивается дистальная симметричная полиневропатия с неуклонно прогрессирующим течением, различные дисфункции автономной нервной системы. Реже выявляют двусторонний синдром запястного канала, обусловленный сдавлением срединного нерва депозитами амилоида.
Поражение кожи наблюдают почти у 40% больных AL-амилоидозом. Помимо параорбитальных геморрагий описаны также
папулы, бляшки, узелки, пузырьковые высыпания, склеродермоподобная индурация кожи.
Амилоидные отложения в мышцах чаще встречаются при AL-амилоидозе. Макроглоссия – патогномоничный симптом AL-амилоидоза, развивающийся примерно у 20% пациентов.
Редким проявлением амилоидоза, описанным при AL- и, в особенности, АTTR-типах, бывает поражение глаз (сухой кератоконъюнктивит, вторичная глаукома, помутнение стекловидного тела, дисфункции зрачка).
Клиническая картина других типов амилоидоза варьируется в зависимости от основной локализации и распространенности амилоидных депозитов, которые иногда могут быть значительными и напоминать проявления AL-амилоидоза.
Рекомендации:
- Наиболее типичное проявление амилоидоза почек – изолированная протеинурия более 0,5 г/сут, чаще
нефротического уровня. Иногда при множественной миеломе важное значение приобретает иммунохимическое
электрофоретическое исследование мочи для отличия альбуминурии в рамках амилоидоза и протеинурии
переполнения (наличие в моче белка БенсДжонса, реакция термопреципитации белка Бенс-Джонса не обладает
достаточной информативностью).
 Для установления связи протеинурии с амилоидозом необходимо также исключить
протеинурию, связанную с диабетической нефропатией и гипертонической почкой [4,5,29,48,51-56].
Для установления связи протеинурии с амилоидозом необходимо также исключить
протеинурию, связанную с диабетической нефропатией и гипертонической почкой [4,5,29,48,51-56]. - На амилоидоз сердца указывает утолщение межжелудочковой перегородки и/или задней стенки левого желудочка более 12 мм при эхокардиографии, особенно в сочетании с низкоамплитудной ЭКГ. Дифференциальный диагноз проводят с гипертрофией левого желудочка, которая может быть следствием артериальной гипертонии, аортальных пороков, гипертрофической кардиомиопатии и других причин [29,37-39,42,48,51-53,57-62].
- Характерное проявление амилоидоза сердца – низкая амплитуда желудочковых комплексов на ЭКГ (менее 5 мм в
отведениях от конечностей). Пато логические Q-зубцы у больных амилоидозом нередко являются псевдоинфарктными
(вследствие электрически нейтральных отложений амилоида, имитирующих рубцовые изменения), однако при
амилоидозе коронарных артерий возможно развитие и истинного инфаркта миокарда [29,37-39,42,48,51-53,56-62].

- При амилоидозе сердца наблюдается рестриктивное нарушение диастолической функции левого желудочка, фракция выброса часто остается нормальной, или степень ее снижения не соответствует тяжести сердечной недостаточности [29,37-39,42,48,51-53,5662].
- Всем больным с амилоидозом сердца необходимо проведение стандартной эхокардиографии с допплерометрической оценкой трансмитрального крово тока, при наличии технической возможности оправдано также проведение тканевой допплерометрии миокарда для более точной оценки внутрисердечной гемодинамики. В стандарт обследования больных амилоидозом сердца входят также ЭКГ и суточное мониторирование АД и ЭКГ [1,2,29,37-39,42,48,5153,56-62].
- Магнитно-резонансная томография (МРТ) с контрастированием гадолинием с высокой вероятностью выявляет
инфильтративный характер поражения миокарда и имеет особое диагностическое значение при “изолированном»
поражении сердца [48,56,6062].

- Амилоидную инфильтрацию сердца позволяет выявить также сцинтиграфия миокарда с пирофосфатом технеция, особенно при наличии трудностей в морфологической диагностике ATTR-амилоидоза, для которого характерна слабая конгофилия пораженных тканей. Интенсивное накопление радиоактивного препарата в миокарде (2+/3+) в сочетании с утолщением миокарда неясной этиологии указывает на высоко вероятный ATTR-амилоидоз, если у пациента исключен диагноз AL-амилоидоза (рис. 1) [39,42,58-59,62].
- Диагноз амилоидоза сердца может быть подтвержден при биопсии миокарда. Однако проведение этого исследования обычно не требуется при наличии типичных эхокардиографических изменений у пациентов с амилоидозом, установленным при биопсии другого органа, например, почки или слизистой оболочки прямой или двенадцатиперстной кишки.
- Диагностика периферической амилоидной полиневропатии основывается на клинической оценке неврологических
проявлений: обычно выявляют различные нарушения чувствительности, в частности температурной и болевой.
 Из-за
поражения преимущественно мелких немиелинизированных волокон электромиография и исследование скорости
проведения нервного импульса обычно неинформативны для ранней диагностики амилоидной полиневропатии [38,39].
Доминирование жалоб, связанных с поражением нервной системы, является отличительной чертой ATTR-амилоидоза.
Из-за
поражения преимущественно мелких немиелинизированных волокон электромиография и исследование скорости
проведения нервного импульса обычно неинформативны для ранней диагностики амилоидной полиневропатии [38,39].
Доминирование жалоб, связанных с поражением нервной системы, является отличительной чертой ATTR-амилоидоза.
- Электромиография наряду с другими нейрофизиологическими методами (количественное сенсорное тестирование,
конфокальная микроскопия нервов роговицы, оценка состояния интраэпидермальных нервных волокон в биоптате
кожи) может использоваться для оценки характера (признаки аксонального и/или аксонально-демиелинизирующего
типа поражения двигательных и чувствительных волокон нервов конечностей) и тяжести неврологических
нарушений. Электромиография в сочетании с ультразвуковым исследованием периферических нервов позволяет
объективизировать их повреждение в анатомически узких каналах (туннельные невропатии) [38,39].

- Признаками I стадии амилоидной полиневропатии являются незначительные нарушения чувствительности по полиневропатическому типу, более выраженные в ногах, пациент сохраняет способность к самостоятельной ходьбе. При II стадии полиневропатии из-за нарастания чувствительных и присоединения двигательных нарушений в виде нижнего периферического преимущественно дистального парапареза походка пациента нарушается, требуется опора на трость или костыли. На III стадии тяжелые двигательные нарушения приковывают пациента к постели, передвижение возможно только на инвалидной коляске [38,39,46].
- Поражение вегетативной нервной системы чаще всего проявляется ортостатической гипотензией разной степени
тяжести. Однако систолическое артериальное давление менее 90 мм рт. ст. может быть обусловлено низким
сердечным выбросом у больных с сердечной недостаточностью или гиповолемией при тяжелом нефротическом
синдроме.
 Другие частые проявления поражения вегетативной нервной системы – моторная диарея, дисфункция
мочевого пузыря, половой сферы, гипогидроз [1,2,38,51]. Наряду с моторной диареей причиной значительного (на
9-18 кг) снижения массы тела могут быть нарушения трофики мышц [38,39].
Другие частые проявления поражения вегетативной нервной системы – моторная диарея, дисфункция
мочевого пузыря, половой сферы, гипогидроз [1,2,38,51]. Наряду с моторной диареей причиной значительного (на
9-18 кг) снижения массы тела могут быть нарушения трофики мышц [38,39]. - Двусторонний синдром запястного канала наиболее характерен для ATTR-, β2М- и AL-амилоидоза и проявляется интенсивными болями и парестезиями в IIII пальцах кистей с постепенной атрофией мышц тенара [38,39].
- МРТ головного мозга с контрастным усилением проводят при наличии клинических признаков поражения центральной нервной системы [38,39].
- Основным признаком амилоидоза печени является ее увеличение, наиболее специфична гепатомегалия более 15 см
по данным компьютерной томографии. У больных амилоидозом печени обычно выявляют также холестаз (повышение
активности щелочной фосфатазы и/или g-глютамилтранспептидазы в 1,5 раза по сравнению с верхней границей
нормы).
 Ложная диагностика амилоидоза печени возможна у больных с тяжелой застойной правожелудочковой
недостаточностью [2,4,48,51].
Ложная диагностика амилоидоза печени возможна у больных с тяжелой застойной правожелудочковой
недостаточностью [2,4,48,51]. - Для выявления амилоидоза печени, селезенки и почек всем пациентам проводят ультразвуковое исследование этих органов, в некоторых случаях необходимо проведение компьютерной томографии брюшной полости [2,48].
- Диарея вследствие инфильтрации амилоидом стенки желудочно-кишечного тракта возникает редко, такую диарею трудно дифференцировать от моторной диареи в рамках поражения вегетативной нервной системы. Наиболее надежно вовлечение желудочнокишечного тракта при амилоидозе устанавливают по результатам морфологического исследования. Одна ко обнаружение амилоида только в стенках сосудов желудочно-кишечного тракте не является критерием его поражения, необходимо обнаружение амилоидных депозитов в интерстиции подслизистого слоя кишечника [1-2,5,48,52].
- Нодулярный легочный и трахеобронхиальный амилоидоз за редким исключением – это проявление локального
AL-амилоидоза.
 Для системного AL-амилоидоза характерно обнаружение диффузного интерстициального легочного
амилоидоза. В связи с редкостью дыхательной недостаточности необходимости в морфологической верификации
легочного амилоидоза обычно не возникает. Наиболее информативным методом диагностики амилоидоза легких
является компьютерная томография [1,2,48]. У больных локальным трахеобронхиальным AL-амилоидозом важными
методами мониторирования течения заболевания являются ларингоскопия и бронхоскопия [27,48].
Для системного AL-амилоидоза характерно обнаружение диффузного интерстициального легочного
амилоидоза. В связи с редкостью дыхательной недостаточности необходимости в морфологической верификации
легочного амилоидоза обычно не возникает. Наиболее информативным методом диагностики амилоидоза легких
является компьютерная томография [1,2,48]. У больных локальным трахеобронхиальным AL-амилоидозом важными
методами мониторирования течения заболевания являются ларингоскопия и бронхоскопия [27,48]. - На амилоидоз плевры указывает рецидивирующий плевральный выпот, который не зависит от эффективности лечения
отечного синдрома, обусловленного сердечной недостаточностью или нефротическим синдромом. При амилоидном
поражении плевры жидкость, полученная во время пункции плевральной полости, нередко содержит примесь крови.
При амилоидозе плевры эвакуация плеврального выпота, как правило, малоэффективна из-за быстрого его
накопления [1,2,48].

- Поражение мягких тканей характерно для AL-амилоидоза. Макроглоссия с инфильтрацией дна ротовой полости и периорбитальная пурпура (и кожные геморрагии на теле) патогномоничны для этого типа амилоидоза. Возможны также псевдогипертрофия скелетных мышц с развитием мышечной слабости, лимфаденопатия, амилоидоз височной артерии [1,2,39,48,52].
- Признаками прогрессирования амилоидоза сердца являются дальнейшее утолщение миокарда (на 2 мм и более),
увеличение функционального класса сердечной недостаточности, снижение фракции выброса левого желудочка на
10% и более. Показатели тяжести амилоидоза сердца – увеличение уровня NTproBNP (особенно более 1800 нг/л) и
тропонинов (тропонин Т более 0,025 нг/мл). Критериями прогрессирования амилоидоза почек считают увеличение
протеинурии (на 50% от исходного уровня, как правило на 1 г/сут и более) и сывороточного уровня креатинина
(на 25% и более от исходного). Информативным критерием прогрессирования амилоидоза печени является
увеличение активности щелочной фосфатазы на 50% от исходной.
 Прогрес сирование полиневропатии
объективизируют на основании результатов стимуляционной электромиографии и других нейрофизиологических и
нейровизуализационных методов обследования (см. выше). Важным показателем тяжести больных AL-амилоидозом
является разница в содержании свободных легких цепей иммуноглобулинов более 180 мг/л, установленная методом
Freelite [2,38,51,48,60,61,64].
Прогрес сирование полиневропатии
объективизируют на основании результатов стимуляционной электромиографии и других нейрофизиологических и
нейровизуализационных методов обследования (см. выше). Важным показателем тяжести больных AL-амилоидозом
является разница в содержании свободных легких цепей иммуноглобулинов более 180 мг/л, установленная методом
Freelite [2,38,51,48,60,61,64].
Лечение системного амилоидоза
Целью терапии любого типа амилоидоза служит уменьшение количества (или, если возможно, удаление)
белков-предшественников для того, чтобы замедлить или приостановить прогрессирование болезни. Неблаго приятный
прогноз при естественном течении амилоидоза оправдывает применение агрессивных методов лечения. Клиническое
улучшение, достигаемое с помощью лечения, включает стабилизацию или восстановление функции жизненно важных
органов, а также предотвращение функциональных нарушений с увеличением продолжительности жизни больных. Лечение
амилоидоза должно включать симптоматические методы, направленные на уменьшение выраженности сердечной
недостаточности, аритмии, отечного синдрома, коррекцию артериальной гипотензии и др.
Лечение
амилоидоза должно включать симптоматические методы, направленные на уменьшение выраженности сердечной
недостаточности, аритмии, отечного синдрома, коррекцию артериальной гипотензии и др.
Лечение АА-амилоидоза
Цель терапии АА-амилоидоза – подавление продукции белка-предшественника SAA (вплоть до устойчивой нормализации), что достигается активным лечением хронического воспаления (в том числе субклинического). Это позволяет уменьшить клинические проявления и предотвратить прогрессирование амилоидной нефропатии и существенно улучшить прогноз.
Рекомендации:
- Основной стратегией лечения АА-амилоидоза является эффективное подавление воспаления. Лечение должно
проводиться вне зависимости от клинической активности воспалительного заболевания до нормализации уровня
маркеров острой фазы воспаления – С-реактивного белка (предпочтительно применение высокочувствительного
метода измерения) и/или SAA [10-13,63,66-77].

- Больным ревматоидным артритом и серонегативными спондилоартропатиями необходима постоянная пожизненная базисная терапия. Предпочтение отдают генно-инженерным биологическим препаратам, в том числе ингибиторам фактора некроза опухоли-α, интерлейкина-6, ритуксимабу. После оценки эффективности и безопасности базисной терапии оправдано присоединение терапии колхицином в дозе 2 мг/сут [10-13,63,66-77].
- Препаратом выбора при периодической болезни и тяжелой рецидивирующей подагре является колхицин в дозе 2
мг/сут. Начальная доза препарата составляет 0,5 мг/сут, затем ее постепенно увеличивают до целевой под
контролем клинического анализа крови и сывороточного уровня креатинина. Для предупреждения осмотической
диареи, обусловленной колхицином, возможно временное назначение ферментных препаратов. Дозу колхицина
снижают до 1 мг/сут у больных с хронической болезнью почек 4-5 стадии [1,2,4,69]. При неэффективности
колхицина показано назначение ингибиторов интерлейкина-1, в частности канакинумаба.

- При криопиринопатиях, TRAPS препаратами выбора являются ингибиторы интерлейкина-1, к которым присоединяют колхицин [18,19,74-77].
- При хронических нагноениях важное значение имеет хирургическое лечение. В дальнейшем или одновременно проводят лечение димексидом (5-10 г/сут в разведении большим количеством соков – томатного, гранатового и др.). Препарат предпочтителен при легочных нагноениях [1-2,4,6,31].
Лечение АL-амилоидоза
При AL-амилоидозе, как и при множественной миеломе, целью лечения служит подавление пролиферации клона
плазматических клеток для уменьшения продукции легких цепей иммуноглобулинов. В отличие от множественной
миеломы, принципиальной задачей лечения AL-амилоидоза является по возможности полная элиминация патологического
клона. В связи с быстрым прогрессированием заболевания важное значение имеет применение быстродействующих схем
лечения на основе бортезомиба. По мере достижения ремиссии у некоторых больных применяют высокодозную
химиотерапию с поддержкой аутологичными стволовыми клетками. При строгом подборе больных с исключением
противопоказаний к этой терапии эффект достигают у 60% больных. У больных с клиническими симптомами амилоидоза
сердца, ортостатической гипотензией, диареей, желудочно-кишечными кровотечениями в анамнезе, а также у лиц
старше 70 лет с амилоидным поражением двух и более систем организма проведение высокодозной химиотерапии не
рекомендуется. Тяжелый агранулоцитоз и другие осложнения существенно ограничивают ее применение. Проводят также
лечение талидомидом или леналидомидом. Колхицин при AL-амилоидозе не эффективен.
По мере достижения ремиссии у некоторых больных применяют высокодозную
химиотерапию с поддержкой аутологичными стволовыми клетками. При строгом подборе больных с исключением
противопоказаний к этой терапии эффект достигают у 60% больных. У больных с клиническими симптомами амилоидоза
сердца, ортостатической гипотензией, диареей, желудочно-кишечными кровотечениями в анамнезе, а также у лиц
старше 70 лет с амилоидным поражением двух и более систем организма проведение высокодозной химиотерапии не
рекомендуется. Тяжелый агранулоцитоз и другие осложнения существенно ограничивают ее применение. Проводят также
лечение талидомидом или леналидомидом. Колхицин при AL-амилоидозе не эффективен.
Рекомендации:
- Основной стратегией лечения АL-амилоидоза является элиминация амилоидогенного клона плазматических клеток
костного мозга. После достижения гематологической ремиссии проводят противорецидивное лечение в течение не
менее 12 месяцев.
 В этот период при отсутствии противопоказаний возможна высокодозная химиотерапия с
поддержкой аутологичными стволовыми клетками, которая позволяет достичь длительной ремиссии
[2,26,37,56,57,65,78,79].
В этот период при отсутствии противопоказаний возможна высокодозная химиотерапия с
поддержкой аутологичными стволовыми клетками, которая позволяет достичь длительной ремиссии
[2,26,37,56,57,65,78,79]. - Полный гематологический ответ диагностируют на основании исчезновения моноклональных амилоидогенных иммуноглобулинов по данным иммунофиксации крови и суточной мочи, количественного определения свободных легких цепей иммуноглобулинов методом Freelite (нормальный уровень легких цепей κ – менее 19,4 мг/л, λ – менее 26,3 мг/л, нормальное соотношение легких цепей в пределах 0,261,65). При снижении уровня свободных легких цепей на 50% от исходного диагностируют частичный ответ, критерием очень хорошего частичного ответа является разница между содержанием двух типов легких цепей иммуноглобулинов менее 40 мг/л [37,60,61,64].
- Клинический эффект терапии в первую очередь оценивают по динамике кардиологических и ренальных показателей.
 Особо выделяют NT-proBNP-ответ (снижение уровня маркера на 30% и более или на 300 нг/л и более у пациентов с
исходным уровнем более 650 нг/л). С клиническим эффектом лечения больше коррелирует почечный ответ (снижение
протеинурии на 75% и более, повышение сывороточного креатинина не более 25% от исходного). Ответ со стороны
других органов не обладает существенной прогностической информативностью. Эффективность лечения амилоидоза
печени оценивают по снижению активности щелочной фосфатазы (на 50% и более) и уменьшению размеров печени
(краниокаудальный размер по данным КТ должен уменьшиться на 30% в течение года после достижения
гематологической ремиссии). Эффективность лечения амилоидной полиневропатии определяют, главным образом, по
результатам клинического неврологического осмот ра. Уменьшение амилоидных депозитов в мягких тканях может
быть оценено по данным компьютерной томографии или МРТ. Эффективным методом оценки общего содержания
амилоида в тканях служит сцинтиграфия с радиоактивным амилоидным Ркомпонентом [2,26,37,57,60,61,64].
Особо выделяют NT-proBNP-ответ (снижение уровня маркера на 30% и более или на 300 нг/л и более у пациентов с
исходным уровнем более 650 нг/л). С клиническим эффектом лечения больше коррелирует почечный ответ (снижение
протеинурии на 75% и более, повышение сывороточного креатинина не более 25% от исходного). Ответ со стороны
других органов не обладает существенной прогностической информативностью. Эффективность лечения амилоидоза
печени оценивают по снижению активности щелочной фосфатазы (на 50% и более) и уменьшению размеров печени
(краниокаудальный размер по данным КТ должен уменьшиться на 30% в течение года после достижения
гематологической ремиссии). Эффективность лечения амилоидной полиневропатии определяют, главным образом, по
результатам клинического неврологического осмот ра. Уменьшение амилоидных депозитов в мягких тканях может
быть оценено по данным компьютерной томографии или МРТ. Эффективным методом оценки общего содержания
амилоида в тканях служит сцинтиграфия с радиоактивным амилоидным Ркомпонентом [2,26,37,57,60,61,64].
- Учитывая возможность достижения быстрого гематологического ответа, терапией первой линии, особенно у больных
с высоким риском быстрого прогрессирования, считают комбинированные схемы на основе бортезомиба, например,
трехкомпонентная схема: бортезомиб 1,3 мг/м2 внутривенно или подкожно (1, 5, 8 и 11-й дни цикла), мелфалан
0,15 мг/кг внутрь (с 1-го по 4-й день) и дексаметазон 20 мг/сут внутрь (1, 5, 8 и 11-й дни). Для большей
безопасности предпочтительно подкожное введение бортезомиба. Если в дальнейшем планируется высокодозная
химиотерапия с поддержкой аутологичными стволовыми клетками мелфалан в составе трехкомпонентной схемы
заменяют на циклофосфамид (400 мг внутривенно капельно в 1, 8, 12-й дни), который не вызывает истощение пула
стволовых клеток в костном мозге. Курсы химиотерапии на основе бортезомиба проводят каждые 4 недели (всего 8
курсов). Одновременно назначают омепразол, низкомолекулярные гепарины (для профилактики тромбозов при
применении высоких доз дексаметазона), при наличии показаний – антибиотики, противогрибковые препараты,
ацикловир [65,78,79].

- Не менее эффективна схема терапии мелфаланом (внутрь 0,15 мг/кг с 1-го по 4-й день) и дексаметазоном (внутрь 20 мг/сут в дни 1-4, 9-12 и 17-21) каждые 4-6 недель. Основным недостатком этой схемы является медленное формирование гематологического ответа, что делает ее менее перспективной у больных с высоким риском быстрого прогрессирования амилоидоза. Одновременно назначают омепразол, низкомолекулярные гепарины (для профилактики тромбозов при применении высоких доз дексаметазона), при наличии показаний – антибиотики, противогрибковые препараты, ацикловир [1,2,37,56,57,65,78,79].
- У тяжелых больных с декомпенсированной сердечной недостаточностью может применяться схема терапии мелфаланом (внутрь 0,15 мг/кг с 1-го по 4-й дни) и преднизолоном (0,8 мг/кг с 1-го по 7-й день). Однако эффективность этой схемы ограничена [1,2,56,57,65,78,79].
Лечение ATTR-амилоидоза
До недавнего времени единственным методом лечения ATTR-амилоидоза была трансплантация печени, секретирующей
нормальный транстиретин. Поскольку 98% всего сывороточного транстиретина синтезируется печенью, это позволяло
прервать продукцию мутантного транстиретина. Трансплантация печени существенно замедляет прогрессирование
ATTR-амилоидоза, а 20летняя выживаемость больных после трансплантации составляла 55,3% [36]. Однако уже
имеющиеся массы амилоида способны выступать в роли ядра нуклеации для новых депозитов амилоида на основе
нормального транстиретина (амилоидускоряющая субстанция). В настоящее время у больных с ранними стадиями
ATTRамилоидной полиневропатии апробированы консервативные методы стабилизации тетрамерной структуры мутантного
транстиретина и, следовательно, подавления его амилоидогенности. Один из таких препаратов – тафамидис замедлял
на 52% (р=0,027) прогрессиро вание неврологических нарушений у больных ATTRамилоидозом, сохраняя функцию
периферических соматических и автономных нервных волокон [12]. В клиническом исследовании III фазы лечение
тафамидисом по сравнению с плацебо у больных с ATTR-амилоидозом сердца вызывало снижение общей смертности и
частоты госпитализаций по сердечно-сосудистым причинам и задерживало ухудшение функциональной активности [81].
Поскольку 98% всего сывороточного транстиретина синтезируется печенью, это позволяло
прервать продукцию мутантного транстиретина. Трансплантация печени существенно замедляет прогрессирование
ATTR-амилоидоза, а 20летняя выживаемость больных после трансплантации составляла 55,3% [36]. Однако уже
имеющиеся массы амилоида способны выступать в роли ядра нуклеации для новых депозитов амилоида на основе
нормального транстиретина (амилоидускоряющая субстанция). В настоящее время у больных с ранними стадиями
ATTRамилоидной полиневропатии апробированы консервативные методы стабилизации тетрамерной структуры мутантного
транстиретина и, следовательно, подавления его амилоидогенности. Один из таких препаратов – тафамидис замедлял
на 52% (р=0,027) прогрессиро вание неврологических нарушений у больных ATTRамилоидозом, сохраняя функцию
периферических соматических и автономных нервных волокон [12]. В клиническом исследовании III фазы лечение
тафамидисом по сравнению с плацебо у больных с ATTR-амилоидозом сердца вызывало снижение общей смертности и
частоты госпитализаций по сердечно-сосудистым причинам и задерживало ухудшение функциональной активности [81]. В
Российской Федерации применение тафамидиса зарегистрировано только для лечения ATTR-амилоидоза с периферической
полиневропатией.
В
Российской Федерации применение тафамидиса зарегистрировано только для лечения ATTR-амилоидоза с периферической
полиневропатией.
В качестве стабилизатора транстиретина изучается также дифлюнизал из группы нестероидных противовоспалительных препаратов, однако его эффективность показана только в экспериментальных условиях.
Рекомендации:
- Трансплантация печени остается одним из методов лечения ATTR-амилоидоза. Наилучших показателей выживаемости удается достичь у больных моложе 50 лет с небольшой длительностью заболевания, нормальным индексом массы тела и мутацией Val30Met. Эффективность трансплантации печени существенно ниже у больных с III стадией полиневропатии, ортостатической гипотензией, хронической сердечной недостаточностью, удлинением комплекса QRS бо лее 120 мс и утолщением межжелудочковой перегородки [2,38-40,43-46].
- Больным ATTR-амилоидозом с периферической невропатией рекомендуется пожизненный прием тафамидиса в дозе 20
мг/сут внутрь, который обладает хорошим профилем безопасности [38-40,43-46,80].

Заместительная почечная терапия
Рекомендации:
- Поскольку ХПН служит одной из основных причин смерти больных системным амилоидозом, проведение гемодиализа
или постоянного амбулаторного перитонеального диализа позволяет улучшить прогноз этих пациентов.
Выживаемость больных амилоидозом при проведении гемодиализа, независимо от его типа, сопоставима с
выживаемостью больных другими системными заболеваниями и сахарным диабетом. При этом хорошую и
удовлетворительную реабилитацию отмечают у 60% пациентов с АА- и AL-типами амилоидоза. Основной причиной
смерти больных амилоидозом при проведении гемодиализа являются сердечно-сосудистые осложнения. Амбула торный
перитонеальный диализ имеет некоторые преимущества перед гемодиализом, учитывая отсутствие необходимости в
постоянном сосудистом доступе и меньший риск артериальной гипотензии во время процедуры диализа. У больных
AL-амилоидозом во время процедуры возможно удаление легких цепей иммуноглобулинов [1-4,6,28,48].

- Трансплантация почки эффективна при системном амилоидозе: 5-летняя выживаемость больных и трансплантата составляет 65% и 62%, соответственно, и сопоставима с таковыми в других группах больных с ХПН. Трансплантация почки показана больным с медленным прогрессированием амилоидоза без поражения сердца и желудочно-кишечного тракта. Амилоидоз в трансплантированной почке возникает, по разным данным, примерно у 30% больных, однако он служит причиной потери трансплантата всего у 2-3% пациентов [1-4,6,28,48].
Симптоматическая терапия
Рекомендации:
- Больным амилоидозом противопоказаны сердечные гликозиды и недигидропиридиновые антагонисты кальция
(верапамил, дилтиазем), которые могут накапливаться в амилоиде, в то время как β-адреноблокаторы и
ингибиторы АПФ следует применять осторожно. Основа лечения застойной сердечной недостаточности при
амилоидозе сердца – петлевые диуретики, хотя ортостатическая гипотензия может ограничивать применение этих
препаратов, как и β-адреноблокаторов и ингибиторов АПФ [1,2,31,45,49,52,58].

- При наличии желудочковых тахиаритмий, сопровождавющихся высоким риском внезапной сердечной смерти, показана установка искусственного кардиовертера-дефибриллятора, а при синдроме слабости синусового узла и атрио-вентрикулярной блокаде – имплантация искусственного водителя ритма [2,38,39,45,52,53,58].
- Для лечения ортостатической гипотензии могут быть использованы минералокортикостероиды или глюкокортикостероиды, хотя их применение может привести к декомпенсации сердечной недостаточности. Возможно назначение α-адреномиметика мидодрина (Гутрон), однако его применение требует осторожности [1,2,39,42,45,52,58].
- Для контроля кишечной моторики высокую эффективность показали пролонгированные препараты соматостатина (октреотид-лонг 20 мг один раз в месяц) [1,2,38,39,49].
- При деструкции стекловидного тела у больных ATTR-амилоидозом может потребоваться витрэктомия. При наличии
неконтролируемой глаукомы проводят трабекулэктомию [39].

- Для купирования невропатической боли у пациентов с амилоидной невропатией рекомендовано использование адъювантных анальгетиков (антиконвульсанты и антидепрессанты) [39].
причины, симптомы, диагностика, лечение в НКЦ ОАО «РЖД», с филиалом ЦКБ № 1
Амилоидоз почек — заболевание нарушения обмена веществ, в результате чего в тканях образуется субстанция — амилоид, которая нарушает функций органов.
Причины амилоидоза почек:
Данная болезнь, как правило, возникает после длительного хронического воспаления (туберкулеза, сифилиса), при ревматоидном артрите, хронических нагноениях (остеомиелит), опухолях и других заболеваниях.
Амилоидные субстанции часто откладываются в почках, нервной системе, сердце и кишечнике. Первичную форму болезни врачи связывают именно с наследственными причинами.
Если вам поставлен диагноз амилоидоз почек, лечение следует начинать незамедлительно.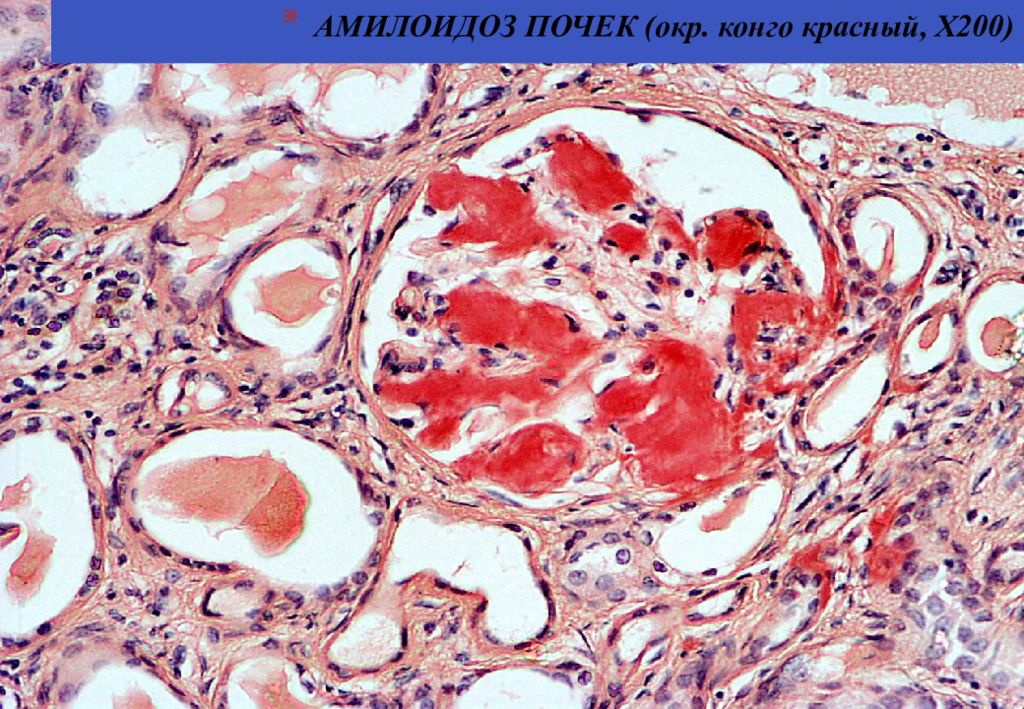 Это позволит избежать осложнений, в том числе и на сердце, так как накопление амилоида в сердечных тканях приводит к развитию сердечной недостаточности. Происходит увеличение размеров сердца, поражение клапанов, сердце не справляется с привычными нагрузками, происходит застой крови в легких, в результате чего отеки и дыхательная недостаточность увеличиваются.
Это позволит избежать осложнений, в том числе и на сердце, так как накопление амилоида в сердечных тканях приводит к развитию сердечной недостаточности. Происходит увеличение размеров сердца, поражение клапанов, сердце не справляется с привычными нагрузками, происходит застой крови в легких, в результате чего отеки и дыхательная недостаточность увеличиваются.
Симптомы и диагностика амилоидоза:
Амилоидоз, согласно медицинской статистике, встречается часто. Больше всего при данном заболевании поражаются почки. Локализованные формы амилоидоза кожи или мочевого пузыря могут протекать бессимптомно долгое время. Заболевание затем проявляется в виде отеков, общей слабости, развития почечной недостаточности, перепадами артериального давления, иногда диареей. В ряде случаев больные жалуются на одышку и аритмию, нарушения чувствительности нервных окончаний.
При диагностике в моче пациента обнаруживается белок. Длительная потеря белка в сочетании с другими факторов приводят к развитию гипопротеинемии (снижению белка в крови) и связанного с ней отека.
Биопсия почки, слизистой оболочки прямой кишки, либо ткани десны сегодня является самым достоверным методом диагностики.
В нефрологическом отделении нашей клиники можно пройти всестороннее обследование, в том числе биопсию почки.
Амилоидоз почек. Лечение
Специалисты нашей больницы проводят диагностику и лечение амилоидоза. Основная цель лечения амилоидоза почек — сокращение выработки патологического белка и защита организма от его влияния.
После постановки пациенту точного диагноза «амилоидоз почек», проводится системное лечение. Мы накопили богатый опыт по профилактике и лечению пациентов с такими диагнозами, как амилоидоз кожи, мочевого пузыря, и т.д.
Врачи индивидуально подберут тип лечения: диетические программы, препараты с учётом сопутствующей патологии. Лечение амилоидоза почек проводится совместно со специалистами-кардиологами, гастроэнтерологами и неврологами.
Для получения подробной информации и записи на прием обращайтесь к нам по телефону контакт-центра: (495) 925-02-02 (круглосуточно).
Лечение амилоидоза почек — врачи, лечащие заболевание
Нефрологи Москвы — последние отзывы
Врач очень квалифицированный. Заболевание ребёнка оказалось совсем не её сферой, но при этом даже в других направлениях медицины она хорошо разбирается. Она выслушала наши симптомы, посмотрела документы, послушала внутренние органы, провела пальпацию желудка и дала рекомендации. Мы так же получили направления на дальнейшие обследования.
На модерации, 11 июня 2021
Доктор внимательный, небезразличный и очень грамотный. Она хорошо разбирается в том, чем занимается. Врач меня проконсультировала.
Она хорошо разбирается в том, чем занимается. Врач меня проконсультировала.
Аноним, 28 мая 2021
Внимательный доктор, который пытается разобраться в вопросе пациента. Я приходил не с острыми проблемами. На первом приеме он меня расспросил и назначил анализы.
Анатолий, 21 мая 2021
Замечательный, отзывчивый, знающий и внимательный врач. Она мягкий человек. У неё всегда много пациентов. У меня большие проблемы, поэтому я постоянно у неё наблюдаюсь. Доктор всегда выслушивает, меняет лекарства и предлагает что-то новое. Врач держит меня на плову.
В этой клиники всегда чисто и хорошо берут кровь из вены.
Она мягкий человек. У неё всегда много пациентов. У меня большие проблемы, поэтому я постоянно у неё наблюдаюсь. Доктор всегда выслушивает, меняет лекарства и предлагает что-то новое. Врач держит меня на плову.
В этой клиники всегда чисто и хорошо берут кровь из вены.
Евгения, 08 июня 2021
Если Вам дорого своё здоровье, ни за что не ходите к этому врачу!! У мужа был обычный баланопостит, а после назначенного лечения этим доктором, сейчас у него эрозивно-язвенный!! Когда он пришёл к другому врачу, тот чуть ли не в шоке был!
Аноним, 30 мая 2021
Доктор очень чуткий, профессиональный и понимающий. Она внимательно обследовала ребёнка, изучила все результаты исследований, поставила диагноз и назначила таблетки. Мы очень довольны посещением.
Она внимательно обследовала ребёнка, изучила все результаты исследований, поставила диагноз и назначила таблетки. Мы очень довольны посещением.
Тимур, 29 мая 2021
Наталия Ивановна очень позитивный, хороший, добрый врач с оптимистическим настроем. Она просмотрела результаты анализов, всё по полочкам разложила и назначила лечение. Мы обратимся к ней повторно!
Замира, 27 мая 2021
Очень внимательный, общительный и не пафосный доктор. Она мне все подробно и доступным языком рассказала. Я не первый раз к ней обращаюсь.
Она мне все подробно и доступным языком рассказала. Я не первый раз к ней обращаюсь.
Татьяна, 27 мая 2021
Очень приятный и спокойный доктор. Она нас до конца выслушала и ответила на вопросы. Мы довольны лечением, которое нам прописала врач. Я хочу к ней привести свою дочь.
Кристина, 25 мая 2021
Доктор опытный, пунктуальный и тактичный.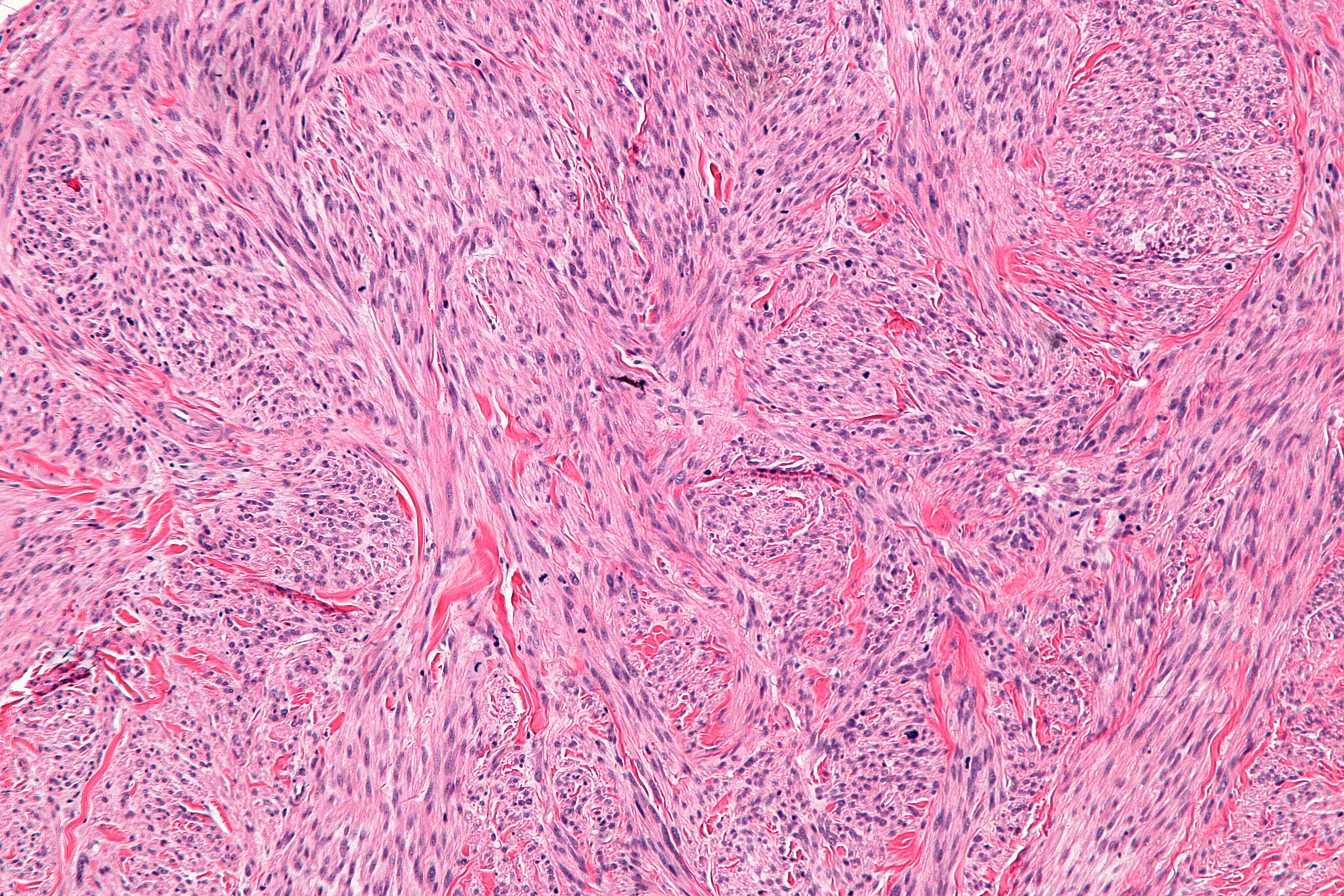 Она провела полный осмотр. Если будут вопросы, то обратимся ещё раз к врачу на прием.
Она провела полный осмотр. Если будут вопросы, то обратимся ещё раз к врачу на прием.
Алексей, 25 мая 2021
Показать 10 отзывов из 1198симптомы, диагностика и лечение в Москве «Диамед»
Амилоидоз почек — тяжелое заболевание, которое отличается очаговым поражением внутренних органов вследствие нарушения белкового обмена. Основная особенность заболевания заключается в выработке специфического вещества известного как амилоид. Амилоид не только оседает в тканях внутренних органов, но и нарушает их функциональность и жизнедеятельность. Несмотря на то, что ведущие ученые уже более века изучают амилоидоз, заболевание до сегодняшнего дня остается неизлечимым.
Классификация заболевания почек
Различают первичный и вторичный амилоидоз почек. Первичный амилоидоз характеризуется как заболевание, возникающее в результате неправильного сцепления иммуноглобулинов, которые оседают не только в органах, но и на стенках сосудов, а также поражают состав крови. Более того первичный амилоидоз сложно подается диагностическим процедурам, поскольку имеет большое количество общих симптомов с другими серьезными заболеваниями.
Первичный амилоидоз характеризуется как заболевание, возникающее в результате неправильного сцепления иммуноглобулинов, которые оседают не только в органах, но и на стенках сосудов, а также поражают состав крови. Более того первичный амилоидоз сложно подается диагностическим процедурам, поскольку имеет большое количество общих симптомов с другими серьезными заболеваниями.
Вторичный амилоидоз развивается в результате хронических инфекций и таких заболеваний как приобретенный остеомиелит, спондилоартрит, колит, заболевания онкологического характера, склероз, ревматоидный артрит и туберкулез. Вторичный амилоидоз может развиться в старческом возрасте, а также как генетически обусловленный фактор.
Всем формам заболевания свойственно:
- возникать и продолжать развиваться преимущественно в период раннего детства;
- протекать с периодическим обострением;
- наличие болевых приступов;
- безрезультативное лечение;
- поражение только почек.

Четыре стадии заболевания:
- Латентная стадия заболевания характеризуется бессимптомным протеканием. Наблюдается лишь отечность и признаки склероза. Стадия может длиться примерно 6 лет. В течение последних 2 лет есть вероятность появления первых признаков основной болезни (туберкулез, артрит, злокачественная опухоль).
- Альбуминурическая стадия заболевания обусловлена появлением амилоид на стенках сосудов. На этой стадии у больного развивается склероз, лимфостаз, а также почки увеличиваются в размерах. Стадия длится примерно 12 лет.
- Отечная стадия. На этой стадии амилоиды полностью поражают нефрон. Основные внутренние органы увеличиваются, отмечается глубокий склероз, выраженная отечность и артериальная гипертензия, наблюдаются признаки очагового поражения кишечного тракта. Стадия длится не более 7 лет.
- Азотемическая стадия – наблюдается сморщенная, деформированная почка, имеющая высокую плотность и рубцы. У больного выражена почечная недостаточность, страдает низким артериальным давлением.

Симптомы амилоидоза почек
Первые симптоматические проявления заболевания почек протекают при наиболее ранней форме развития амилоидоза. Самый ранний и достоверный показатель развития заболевания является анализ мочи. У больного в моче содержится высокий процент белков.
Основные общие признаки при амилоидозе почек – это слабость всего организма, анемия, резкое снижение иммунитета, частая простуда, дисфункция сердечно-сосудистой системы, диарея. Наиболее характерными признаками амилоидоза почек является отечность, а также увеличение внутренних органов.
На поздних этапах заболевания больной чаще всего обращается за медицинской помощью в связи с артериальной гипертонией и с такими серьезными осложнениями как анурия и тромбозы почечных вен.
Сегодня большинство исследований указывают на такие комбинированные симптомы протекания амилоидоза почек как:
- почечная недостаточность, слабовыраженная фильтрация почек;
- нарушения в работе желудочно-кишечного тракта, а также неправильное всасывание питательных веществ;
- поражение системы нервной деятельности;
- аритмия и сердечная недостаточность.

Методы диагностики амилоидоза почек
Одним из самых распространенных и достоверных диагностирующих методов амилоидоза является анализ крови, поскольку при заболевании резко увеличивается содержание тромбоцитов, снижается количество гемоглобина и белков, а в сыворотке повышается уровень печеночного фермента.
Следующий метод – электрокардиограмма, у больного с амилоидозом почек импульсы отличаются заниженным ритмом.
Очень часто диагноз устанавливается специалистами при помощи биопсии, которая позволяет безошибочно определить количество амилоид в органах и сосудах.
Наиболее информативным методом является микроскопия. Нередко используется рентгенологический метод исследования внутренних органов.
Основные этапы протекания амилоидоза почек:
- Самый ранний этап болезни характеризуется увеличением холестерина в крови и первыми признаками легкого отека.
- Второй этап отличается сильными отеками, которые проявляются вследствие простудных заболеваний как пневмония, тяжелая форма ОРВИ, инфекционная ангина и малярия.

- Третий этап – кахексический период обусловлен снижением иммунитета, а также крайним истощением организма. Развивается хроническая почечная недостаточность, наблюдается уремия, отечность сохраняется.
Стоит отметить, что развитие заболевания амилоидоз остановить невозможно, единственный вариант – это замедлить процесс.
Методы лечения заболевания
Специалисты рекомендуют пациентам периодически проходить санаторно-курортное лечение, как можно чаще выезжать на природу, а также принимать большое количество витаминов. Очень важно при амилоидозе почек исключить из рациона пищу, содержащую белки, а также отказаться от употребления соли, что поможет снять отечность.
Что касается строго медикаментозного лечения, то для снижения аутоиммунного фактора назначаются препараты антигистаминного характера. Обычно к таким препаратам относятся супрастин, а также димедрол. Лечение не обходится и без антибактериальных и противовоспалительных препаратов, особенно отличающихся иммунодепрессивным действием. Чтобы выраженность отеков снизилась, врачи прописывают диуретические препараты, а для поднятия гемоглобина в крови назначают глюкозу, которая проникает в организм посредством капельных вливаний.
Чтобы выраженность отеков снизилась, врачи прописывают диуретические препараты, а для поднятия гемоглобина в крови назначают глюкозу, которая проникает в организм посредством капельных вливаний.
Общие методы лечения для всех форм и стадий заболевания:
- здоровый образ жизни, без стрессовых ситуаций;
- отсутствие физических нагрузок;
- отказ от вредных привычек.
Важно заметить, что лечение назначается в зависимости от стадии заболевания, степени поражения органов, выраженности и сложности его протекания, возрастных особенностей больного и общей картины анамнеза.
Больные с почечной недостаточностью часто подвергаются хирургическим процедурам в связи с трансплантацией почки и удалении пораженного участка. Несмотря на то, что заболевание амилоидоз не относится к онкологической группе заболеваний, в некоторых случаях, врачи назначают курсы химиотерапии, а также прибегают к применению сильного лекарственного препарата колхицина. А также для поддержания здоровья пациента нередко назначают высокую дозу стероидов.
Стоит отметить, что своевременная диагностика и лечение заболевания позволит снизить разрушающее воздействие амилоидоза на внутренние органы, а также позволит улучшить состояние в кратчайшие сроки.
Протекание заболевания и прогноз
Специалисты утверждают, что в основном причиной смертельного исхода больных является хроническая почечная недостаточность, которая наступает в результате реактивного амилоидоза, характеризующий как воспалительный инфекционный процесс. А также существуют сведения, что больные при вспышке реактивного амилоидоза умирают в результате инфекционного заболевания кишечника и диареи.
Статистические данные указывают, что даже при своевременном обнаружении и лечении заболевания средняя выживаемость пациентов с почечной недостаточностью составляет не более полтора года с момента обследования. На сегодняшний день ведущие специалисты продлевают жизнь больным посредством пересадки костного мозга, а также проводят хирургические процедуры по пересадке почки.
#диагностика #урология проблемы с почкамисовременные методы диагностики и лечения uMEDp
В статье дан обзор современных представлений о классификации, патогенезе, клинических проявлениях, диагностике и подходах к лечению системного амилоидоза. Наиболее подробно обсуждены проблемы первичного AL-, вторичного АА- и диализного А-бета-2-М-амилоидоза.
Таблица. Классификация амилоидоза
Термин «амилоидоз» объединяет заболевания, которые характеризуются внеклеточным отложением специфического нерастворимого фибриллярного белка амилоида. Немецкий патолог Рудольф Вирхов в 1853 г. предложил термин «амилоид» для обозначения вещества, откладывающегося в органах больных «сальной болезнью» (как называли амилоидоз в начале XIX века) при туберкулезе, сифилисе, лепре. Это вещество он ошибочно посчитал крахмалоподобным из-за характерной реакции с иодом. В настоящее время установлено, что полисахариды составляют не более 4% от массы амилоида, однако термины «амилоид» и «амилоидоз» закрепились.
Эпидемиология амилоидоза
Распространенность амилоидоза до настоящего времени изучена недостаточно. По данным S.Y. Tan и соавт. (1995) [1], реактивный АА-амилоидоз, один из наиболее частых вариантов амилоидоза, развивается у 5% больных с хроническими воспалительными заболеваниями в Европе; по данным других источников, АА-амилоидоз осложняет течение ревматоидного артрита в 6–10% случаев. В среднем доля АА-амилоидной нефропатии в структуре заболеваний почек в Европе составляет 2,5–2,8%, а в структуре болезней, приведших к хронической почечной недостаточности (ХПН), – 1% (в соответствии с данными Европейской ассоциации диализа и трансплантации).
В США частота амилоидоза варьирует от 5,1 до 12,8 случаев на 100 тыс. населения в год [2]. Эти данные касаются преимущественно распространенности первичного AL-амилоидоза, или амилоидоза в рамках миеломной болезни и других В-гемобластозов. В странах третьего мира, по мнению S.Y. Tan (1995), смертность от AL-амилоидоза составляет 1 на 2000 населения (0,05%). По-видимому, представленные данные о распространенности различных вариантов амилоидоза в целом могут быть экстраполированы и на другие страны.
Морфология амилоидоза
Основу тканевых отложений амилоида составляют амилоидные фибриллы – особые белковые структуры диаметром 5–10 нм и длиной до 800 нм, состоящие из 2 и более параллельных разнонаправленных (антипараллельных) филаментов, образующих кросс-бета-складчатую конформацию. Именно она определяет специфическое оптическое свойство амилоида – способность к двойному лучепреломлению. При микроскопии окрашенных конго красным препаратов в поляризованном свете амилоид изменяет красный цвет окраски на яблочно-зеленое свечение. Обнаружение этого свойства положено в основу диагностики амилоидоза.
Структурные и химико-физические особенности амилоида определяются основным белком-предшественником, содержание которого в фибрилле достигает 80% и является специфичным признаком для каждого типа амилоидоза.
Характеристика основных типов амилоидоза
В группу АА-амилоидоза входят реактивный (вторичный) амилоидоз, амилоидоз при периодической болезни, криопиринопатиях (преимущественно при синдроме Макла – Уэллса – семейной периодической лихорадке в сочетании с глухотой и крапивницей). Наиболее частыми причинами вторичного амилоидоза в настоящее время служат ревматоидный артрит (30–50%), хронические гнойно-деструктивные болезни (остеомиелит, бронхоэктатическая болезнь), воспалительные заболевания кишечника (язвенный колит, болезнь Крона), туберкулез, опухоли (чаще лимфогранулематоз и рак почки) [3].
АА-амилоид образуется из сывороточного белка-предшественника SAA – острофазового белка, в норме синтезируемого гепатоцитами, нейтрофилами и фибробластами в следовых количествах. Его концентрация значительно возрастает под воздействием интерлейкинов 1 и 6, фактора некроза опухоли в ответ на воспаление, опухолевый рост. Повышение содержания SAA в крови играет основную роль в патогенезе АА-амилоидоза.
Однако для развития амилоидоза недостаточно только высокой концентрации SAA, необходимо также наличие у белка-предшественника амилоидогенности. Развитие амилоидоза у человека связывают с депозицией SAA1; в настоящее время известно 5 изотипов SAA1, из которых наибольшую амилоидогенность приписывают изотипам 1.1 и 1.5 [4]. Конечный этап амилоидогенеза – образование фибрилл амилоида из белка-предшественника – осуществляется при неполном расщеплении протеазами моноцитов-макрофагов. Стабилизация амилоидной фибриллы и резкое снижение растворимости этого макромолекулярного комплекса во многом обусловлены взаимодействием с полисахаридами интерстиция. При АА-амилоидозе амилоид обнаруживают в различных органах, однако клиническая картина и прогноз обусловлены поражением почек.
AL-амилоидоз включает в себя первичный (идиопатический) амилоидоз и амилоидоз, ассоциированный с миеломной болезнью, развивающийся у 7–10% больных с множественной миеломой. По современным представлениям, первичный AL-амилоидоз и миеломную болезнь (как ассоциированную, так и не ассоциированную с амилоидозом) рассматривают в рамках единой В-лимфоцитарной дискразии, которая характеризуется пролиферацией аномального клона плазматических клеток или В-клеток в костном мозге с избыточной продукцией моноклонального иммуноглобулина, обладающего амилоидогенностью. Белком-предшественником при AL-амилоидозе считают моноклональные легкие цепи иммуноглобулинов (ЛЦИ), из названия которых происходит аббревиатура L [3]. AL-амилоидоз – это генерализованный процесс с преимущественным поражением сердца, почек, желудочно-кишечного тракта (ЖКТ), нервной системы и кожи.
К ATTR-амилоидозу относят семейную амилоидную полиневропатию, наследуемую по аутосомно-доминантному типу, и системный старческий амилоидоз. Белком-предшественником при этой форме амилоидоза служит транстиретин – компонент фракции преальбумина, синтезируемый печенью и выполняющий функции транспортного белка тироксина и ретинола. Установлено, что АTTR-амилоидоз бывает результатом мутации в гене, кодирующем синтез транстиретина, что приводит к замене аминокислот в молекуле TTR. В результате повышается амилоидогенность белка-предшественника и облегчается его полимеризация в амилоидные фибриллы. В настоящее время известно множество вариантных транстиретинов, чем и обусловлено разнообразие клинических форм наследственной невропатии [5]. Эта группа заболеваний характеризуется прогрессирующей периферической и вегетативной невропатией, которая сочетается с поражением сердца, почек и других органов различной степени.
Системный старческий амилоидоз развивается после 70 лет в результате возрастных изменений структуры нормального транстиретина, усиливающих его амилоидогенность. К органам-мишеням старческого амилоидоза относят сердце, сосуды головного мозга и аорту.
К семейным формам амилоидоза относятся также более редкие AGel-, AFib-, ALys-амилоидозы, при которых амилоидогенностью обладают мутантные формы соответственно гелсолина, фибриногена, лизоцима. При этих вариантах амилоидоза также отмечается преимущественное поражение почек, однако для гелсолинового амилоидоза характерно сочетание нефропатии с сетчатой дистрофией роговицы и периферической невропатией (преимущественно поражаются черепно-мозговые нервы).
В настоящее время известно более 20 амилоидогенных белков-предшественников и, соответственно, клинических вариантов амилоидоза. Так, А-бета-амилоид является морфологической основой болезни Альцгеймера, AIAPP-амилоид – сахарного диабета 2 типа и др. [3].
В нефрологической практике большое значение имеет А-бета-2-М-амилоидоз (ассоциированный с хроническим гемодиализом). Белком-предшественником при этой форме амилоидоза служит бета-2-микроглобулин, который в норме присутствует в крови, моче, спинномозговой и синовиальной жидкостях. При нормальной функции почек его концентрация в крови составляет 1–2 мг/л. Этот белок фильтруется в клубочках почек и метаболизируется после реабсорбции в проксимальных канальцах. У пациентов с ХПН концентрация этого белка в крови возрастает, коррелируя с содержанием креатинина, однако максимальных значений (в 20–70 раз превышающих норму) она достигает через несколько лет проведения регулярного гемодиализа. Бета-2-микроглобулин плохо удаляется при проведении стандартного гемодиализа, что неизбежно приводит к развитию амилоидоза [3]. Первые депозиты бета-2-М-амилоида обнаруживают в синовиальной оболочке суставов уже через 1–2 года заместительной почечной терапии, клинические симптомы появляются через 7 и более лет терапии [3]. У больных старше 60 лет диализный амилоидоз развивается быстрее. Кроме высокой концентрации белка-предшественника, в патогенезе диализного амилоидоза существенную роль играют и другие факторы. Амилоидогенность бета-2-микроглобулина возрастает при модификациях, обусловленных взаимодействием с продуктами неполного гликирования, а также при окислении бета-2-микроглобулина и ацидификации среды [3]. Одним из основных источников этих модификаций являются компоненты диализата, в том числе бактериальный липополисахарид; гликирование бета-2-микроглобулина возможно также при контакте с целлюлозными диализными мембранами. Таким образом, профилактика диализного амилоидоза во многом связана с отказом от целлюлозных диализных мембран и тщательностью контроля качества применяемого диализата. Модифицированный бета-2-микроглобулин является мощным индуктором образования цитокинов (интерлейкины 1 и 6, фактор некроза опухоли альфа). Результатом активации цитокинового каскада является тяжелое синовиальное воспаление с привлечением макрофагов [3]. Макрофагальное воспаление определяет высокий деструктивный потенциал воспаления в синовии с развитием костных эрозий и кист, рост которых обусловливает развитие переломов костей. Было установлено, что бета-2-микроглобулин обладает высокой коллагенсвязывающей активностью, возрастающей по мере увеличения его концентрации в крови. Кроме того, выявлена связь бета-2-микроглобулина с гликозоаминогликанами хряща. Этими фактами можно объяснить преимущественное отложение фибрилл амилоида в суставных тканях. Таким образом, при А-бета-2-М-амилоидозе отмечают поражение костей и периартикулярных тканей, реже – сосудов.
Патогенез амилоидоза
Несмотря на различие в типах амилоидного белка, существует общность патогенеза различных клинических форм амилоидоза. Основной причиной развития болезни служит наличие определенного, нередко повышенного количества амилоидогенного предшественника. Как уже указывалось, появление или усиление амилоидогенности может быть обусловлено циркуляцией вариантов белков с повышенной общей гидрофобностью молекулы, нарушенным соотношением поверхностных молекулярных зарядов, что приводит к нестабильности белковой молекулы и способствует ее агрегации в амилоидную фибриллу. Эти механизмы особенно ярко прослеживаются на примере белков, в функцию которых заложена необходимость физиологического изменения конформации. Так, практически все аполипопротеины, вынужденные разворачивать свою вторичную структуру в процессе транслокации холестерина через стенку сосуда, участвуют в патогенезе различных форм амилоидоза. На последнем этапе амилоидогенеза происходит взаимодействие амилоидного белка с белками плазмы крови и гликозоаминогликанами тканей. Кроме структурных особенностей, имеют значение также физико-химические свойства межклеточного матрикса, где происходит сборка амилоидной фибриллы. В практике экспериментального амилоидоза хорошо известна способность суспензии амилоидных масс (амилоидускоряющая субстанция), полученной из тканей животных, пораженных амилоидом, провоцировать амилоидоз при введении здоровым животным. В клинической практике у больных ATTR-амилоидозом, несмотря на прекращение циркуляции патологического транстиретина после трансплантации здоровой печени, продолжается нарастание массы амилоидных депозитов в сердце за счет захвата нормального неизмененного транстиретина [6]. Многие формы амилоидоза можно объединить также по признаку возникновения в пожилом и старческом возрасте (AL, ATTR, AIAPP, AApoA1, AFib, ALys, AANF, A-бета), что указывает на наличие механизмов возрастной эволюции структуры определенных белков в сторону повышения амилоидогенности и позволяет рассматривать амилоидоз как одну из моделей старения организма.
Классификация амилоидоза
Объяснение многообразия клинических форм амилоидоза наличием многочисленных сывороточных белков-предшественников привело к созданию современной классификации амилоидоза, в основу которой положен биохимический тип белка-предшественника (табл.). Все типы амилоидоза обозначают аббревиатурой, в которой первая буква А означает «амилоидоз», а последующие – сокращенное название основных фибриллярных белков амилоида: А – амилоидный белок А, L – легкие цепи иммуноглобулинов, TTR – транстиретин, бета-2-М – бета2-микроглобулин и др. С клинической точки зрения целесообразно выделять локальные и системные, или генерализованные, формы амилоидоза. Среди последних основными считают АА-, AL-, АTTR- и А-бета-2-М-амилоидоз.
Симптомы амилоидоза почек
В клинической практике наибольшее значение имеют АА- и AL-типы системного амилоидоза, которые протекают с вовлечением в патологический процесс многих органов, однако чаще манифестируют симптомами моноорганного поражения. В дальнейшем развивается, как правило, столь характерный для этих типов амилоидоза полиморфизм клинических проявлений. АА- и AL-амилоидоз у мужчин отмечают в 1,8 раза чаще, чем у женщин. Для вторичного амилоидоза характерно более раннее начало, чем для первичного (средний возраст заболевших – около 40 и 65 лет соответственно). Среди многочисленных клинических проявлений АА- и AL-амилоидоза наряду с общими для обоих типов симптомами существуют характерные лишь для AL-типа признаки (периорбитальные геморрагии, макроглоссия, поражение кожи и др.) [7–9]. Кроме того, клинические проявления, напоминающие признаки первичного амилоидоза, возможны при АTTR- и А-бета-2-М-амилоидозе (синдром запястного канала и др.).
Поражение почек – ведущий клинический признак АА- и AL-амилоидоза. При АА-амилоидозе почки вовлечены в патологический процесс практически у всех больных, при AL-типе частота нефропатии также высока и приближается к 80%. Поражение почек наблюдают и при АTTR-амилоидозе, однако у большинства больных семейной амилоидной невропатией отмечают несоответствие между клиническими и морфологическими признаками нарушений почек.
Амилоид при АА- и AL-типах амилоидоза локализуется преимущественно в клубочках, однако у 10% больных первичным амилоидозом и у значительной части больных наследственной невропатией отмечают только отложения вне клубочков. Амилоид откладывается также в других почечных структурах: в базальной мембране канальцев (преимущественно дистальных и петли Генле), интерстиции, стенках сосудов.
Клинически амилоидная нефропатия манифестирует, как правило, изолированно протеинурией и характеризуется неуклонно прогрессирующим течением с последовательной сменой стадий: протеинурическая, нефротическая, ХПН. Только у 20% больных АА-амилоидозом ХПН развивается без предшествующего нефротического синдрома. При AL-амилоидозе стадийность течения амилоидной нефропатии проявляется менее отчетливо [9].
К особенностям амилоидоза почек относят редкость гематурии и лейкоцитурии («скудный» мочевой осадок), а также артериальной гипертонии, которую даже при ХПН отмечают лишь у 20% больных АА-амилоидозом и еще реже при AL-амилоидозе. Нефротический синдром и большие размеры почек сохраняются даже при развитии и прогрессировании ХПН.
Величина протеинурии не коррелирует с выраженностью амилоидных отложений в почках (при преимущественно сосудистом поражении протеинурия может быть минимальной) и зависит от степени деструкции подоцитов. Максимальную потерю белка обнаруживают через участки базальной мембраны, которые пропитаны амилоидом и лишены эпителиального покрытия.
Амилоидоз почек у большинства больных диагностируют на стадии нефротического синдрома, у 33% – на стадии ХПН. В редких случаях амилоидная нефропатия может проявляться остронефротическим синдромом и макрогематурией. Описаны также синдром Фанкони и тромбоз почечных вен.
Поражение сердца отмечают у подавляющего большинства больных AL-амилоидозом и у части пациентов с АTTR-амилоидозом, в то время как для АА-амилоидоза этот симптом не характерен. В результате замещения миокарда амилоидными массами развивается рестриктивная кардиомиопатия [10]. Клинически определяют кардиомегалию, рано развивается сердечная недостаточность (у 22% больных уже в дебюте болезни), которая быстро прогрессирует и почти у 50% пациентов, наряду с аритмиями, бывает причиной смерти. Особенностью сердечной недостаточности при первичном амилоидозе служит ее рефрактерность к терапии, в первую очередь сердечными гликозидами [11].
Нарушения ритма и проводимости при AL-амилоидозе многообразны: мерцательная аритмия, наджелудочковая тахикардия, синдром преждевременного возбуждения желудочков, различные блокады и синдром слабости синусового узла. Вследствие отложения амилоида в коронарных артериях возможно развитие инфаркта миокарда, обнаруживаемого на аутопсии у 6% больных. Амилоидные отложения в клапанных структурах симулируют картину клапанного порока. Основным признаком амилоидоза сердца на электрокардиограмме бывает снижение вольтажа зубцов комплекса QRS. Описан инфарктоподобный тип электрокардиограммы. Наиболее адекватным методом диагностики амилоидной кардиомиопатии считают эхокардиографию, с помощью которой можно диагностировать симметричное утолщение стенок желудочков, дилатацию предсердий, нарушения гемодинамики.
Серьезным патологическим признаком при AL-амилоидозе служит ортостатическая артериальная гипотония, которую наблюдают у 11% больных в момент постановки диагноза. Обычно этот симптом связан с автономной дисфункцией (поражение вегетативной нервной системы) и в тяжелых случаях сопровождается синкопальными состояниями. Артериальная гипотония бывает также у больных АА-амилоидозом, но в этом случае ее причиной служит надпочечниковая недостаточность вследствие отложения амилоида в надпочечниках [3].
Поражение дыхательной системы возникает при первичном амилоидозе примерно у 50% больных, а при вторичном – у 10–14%. В большинстве случаев оно протекает бессимптомно или со скудной клинической симптоматикой [12]. При AL-амилоидозе одним из ранних признаков болезни может быть охриплость или изменение тембра голоса вследствие отложения амилоида в голосовых связках, опережающего его появление в дистальных отделах дыхательных путей. В легких амилоид откладывается преимущественно в альвеолярных перегородках (что приводит к развитию кашля и одышки) и стенках сосудов. Описаны также ателектазы и инфильтраты в легких. Рентгенологическая картина не специфична, смерть от прогрессирующей дыхательной недостаточности наступает редко [13].
Поражение органов пищеварения наблюдают при амилоидозе в 70% случаев, причем у больных с AL- и АА-типами амилоидоза частота поражения тех или иных отделов ЖКТ различна [3]. У 25% больных первичным амилоидозом отмечают амилоидное поражение пищевода, проявляющееся преимущественно дисфагией, которая может быть одним из ранних симптомов заболевания. О поражении желудка и кишечника могут свидетельствовать изъязвления и перфорации их стенок с возможным кровотечением, а также препилорическая непроходимость желудка или механическая кишечная непроходимость из-за отложения амилоидных масс. У больных с преимущественным поражением толстой кишки возможно появление клинических симптомов, имитирующих язвенный колит. Наиболее частым желудочно-кишечным проявлением AL-амилоидоза, отмечаемым почти у 25% пациентов, бывает тяжелая моторная диарея с вторичным нарушением всасывания. Возможной причиной тяжелой диареи при этом, наряду с инфильтрацией кишечной стенки, и в том числе ворсин, амилоидом, у больных AL-амилоидозом служит автономная (вегетативная) дисфункция. Истинный синдром нарушенного всасывания развивается приблизительно у 4–5% больных. При АА-амилоидозе эти симптомы иногда также возможны, в том числе как единственное клиническое проявление амилоидоза.
Поражение печени при АА- и AL-амилоидозе наблюдают практически в 100% случаев, при этом обычно отмечают небольшое увеличение печени и 3–4-кратное повышение активности гамма-глутамилтранспептидазы и щелочной фосфатазы [14]. Увеличению печени обычно сопутствует небольшое увеличение селезенки. Тяжелое поражение печени с выраженной гепатомегалией и развернутыми признаками тяжелого холестаза отмечается значительно реже (у 15–25% больных) и более характерно для AL-амилоидоза. Несмотря на выраженную гепатомегалию, функция печени обычно остается сохранной. Редким признаком амилоидоза печени бывает внутрипеченочная портальная гипертензия, которая чаще сочетается с выраженной желтухой, холестазом, печеночной недостаточностью и свидетельствует о далеко зашедшем поражении печени с риском пищеводного кровотечения, печеночной комы. При некоторых вариантах семейного ALys-амилоидоза описаны тяжелые спонтанные внутрипеченочные кровотечения [15]. Редким проявлением амилоидоза селезенки бывает ее спонтанный разрыв.
Поражение нервной системы, представленное симптомами периферической невропатии и вегетативной дисфункции, отмечают у 17% больных AL-амилоидозом и у пациентов с семейной амилоидной невропатией разных типов (ATTR, AApoA1 и др.). Клиническая картина невропатии при всех типах амилоидоза практически одинакова, поскольку обусловлена сходными процессами: в первую очередь, дегенерацией миелиновой оболочки нервов, а также компрессией нервных стволов отложениями амилоида и ишемией в результате амилоидных депозитов в стенках сосудов [3].
В большинстве случаев возникает симметричная дистальная невропатия с неуклонным прогрессированием. В дебюте поражения нервной системы наблюдают, главным образом, сенсорные нарушения, в первую очередь болевой и температурной чувствительности, позже присоединяются нарушения вибрационной и позиционной чувствительности, двигательные нарушения. Ранними симптомами невропатии бывают парестезии или мучительные дизестезии (чувство онемения). Нижние конечности вовлекаются в патологический процесс чаще, чем верхние.
Автономные дисфункции часто манифестируют ортостатической артериальной гипотонией (см. выше), иногда с обморочными состояниями, диареей, нарушением функции мочевого пузыря, импотенцией у мужчин.
У 20% больных AL-амилоидозом и у большинства пациентов с амилоидозом на фоне проведения гемодиализа выявляют синдром запястного канала, обусловленный сдавлением срединного нерва в запястном канале амилоидом, откладывающимся в связках запястья [2, 8, 9]. Клинически этот синдром проявляется интенсивными болями и парестезиями в I–III пальцах кисти с постепенной атрофией мышц тенара. К особенностям синдрома запястного канала при диализном амилоидозе относят его преимущественное развитие на той руке, где сформирована фистула, а также усиление болей во время процедуры гемодиализа, возможно, в результате развития феномена обкрадывания, индуцированного фистулой, что приводит к ишемии срединного нерва.
Поражение кожи наблюдают почти у 40% больных первичным амилоидозом. Для него характерно разнообразие проявлений, наиболее частыми из которых бывают параорбитальные геморрагии (патогномоничны для AL-амилоидоза), возникающие при малейшем напряжении. Описаны также папулы, бляшки, узелки, пузырьковые высыпания. Нередко наблюдают индурацию кожи, аналогичную склеродермической. Редким вариантом поражения кожи при AL-амилоидозе служат нарушения пигментации (от выраженного усиления до тотального альбинизма), алопеция, трофические нарушения.
Поражение опорно-двигательного аппарата характерно для пациентов с диализным амилоидозом и редко (в 5–10% случаев) возникает у больных AL-амилоидозом (исключая костные изменения при миеломной болезни). При этом характер тканевого отложения амилоида сходен при обоих этих типах амилоидоза: амилоид откладывается в костях, суставном хряще, синовии, связках и мышцах [16, 17].
При диализном амилоидозе наиболее часто отмечают триаду признаков – плече-лопаточный периартрит, синдром запястного канала и поражение сухожильных влагалищ сгибателей кисти, приводящее к развитию сгибательных контрактур пальцев. Кроме них, характерно развитие кистозного поражения костей из-за отложения амилоида. Типичны амилоидные кисты в костях запястья и головках трубчатых костей. Со временем эти отложения увеличиваются в размерах, становясь причиной патологических переломов.
Частым признаком диализного амилоидоза бывает также деструктивная спондилоартропатия в результате амилоидного поражения межпозвонковых дисков, преимущественно в шейном отделе позвоночника.
Амилоидные отложения в мышцах чаще наблюдают при первичном амилоидозе. Они проявляются псевдогипертрофией или атрофией мышц, затрудняющими движения, мышечными болями. Макроглоссия, обусловленная выраженной инфильтрацией мышц амилоидом, – это патогномоничный симптом AL-амилоидоза, который встречается примерно у 20% пациентов и нередко сочетается с псевдогипертрофией других групп поперечно-полосатой мускулатуры. В тяжелых случаях макроглоссия не только затрудняет прием пищи и речь, но и приводит к обструкции дыхательных путей [3]. При АА-амилоидозе она не развивается.
Среди других органных поражений при амилоидозе известны поражение щитовидной железы с развитием клинической картины гипотиреоза (AL-амилоидоз), надпочечников с появлением симптомов их недостаточности (чаще при АА-амилоидозе), экзокринных желез, приводящее к возникновению сухого синдрома, лимфаденопатия. Редким проявлением, описанным при AL- и АTTR- амилоидозе, бывает поражение глаз.
Диагностика амилоидоза
Предполагаемый на основании клинических и лабораторных данных амилоидоз необходимо подтвердить морфологически обнаружением амилоида в биоптатах тканей.
При подозрении на AL-тип амилоидоза рекомендуют производить пункцию костного мозга. Подсчет плазматических клеток и окраска пунктата на амилоид позволяют не только диагностировать амилоидоз, но и дифференцировать первичный и ассоциированный с миеломой варианты AL-амилоидоза. Положительный результат исследования костного мозга на амилоид отмечают у 60% больных AL-амилоидозом.
Простой и безопасной диагностической процедурой считают аспирационную биопсию подкожной жировой клетчатки, при которой выявляют амилоид в 80% случаев AL-амилоидоза. К преимуществам этой процедуры, кроме информативности, относят также редкость развития кровотечений, что позволяет использовать этот метод у больных с нарушениями свертывания крови (больные первичным амилоидозом нередко имеют дефицит Х фактора свертывания, при котором могут развиться геморрагии [8]).
Наиболее часто для диагностики разных типов амилоидоза проводят биопсию слизистой оболочки прямой кишки, почки, печени. Биопсия слизистого и подслизистого слоев прямой кишки позволяет выявить амилоид у 70% больных, а биопсия почки – практически в 100% случаев. У пациентов с синдромом запястного канала исследованию на амилоид необходимо подвергать ткань, удаленную при операции декомпрессии запястного канала.
Биопсийный материал для выявления амилоида необходимо окрашивать конго красным с последующей микроскопией в поляризованном свете для выявления способности к двойному лучепреломлению. Современная морфологическая диагностика амилоидоза включает не только обнаружение, но и типирование амилоида, поскольку тип амилоида определяет терапевтическую тактику. Для типирования часто применяют пробу с перманганатом калия. При обработке окрашенных конго красным препаратов 5%-ным раствором перманганата калия АА-тип амилоида теряет окраску и утрачивает свойство двойного лучепреломления, тогда как AL-тип амилоида сохраняет их. Использование щелочного гуанидина позволяет более точно дифференцировать АА- и AL-амилоидоз.
Наиболее эффективным методом типирования амилоида служит иммуногистохимическое исследование с применением антисывороток к основным типам амилоидного белка (специфические антитела против АА-белка, легких цепей иммуноглобулинов, транстиретина и бета-2-микроглобулина) [3, 18].
Лечение амилоидоза
Согласно современным представлениям, целью терапии любого типа амилоидоза является уменьшение количества (или, если возможно, удаление) белков-предшественников для того, чтобы замедлить или приостановить прогрессирование болезни. Неблагоприятный прогноз при естественном течении амилоидоза оправдывает применение некоторых агрессивных лекарственных режимов или других радикальных мер. Клиническое улучшение, достигаемое с помощью этих видов лечения, включает стабилизацию или восстановление функции жизненно важных органов, а также предотвращение функциональных нарушений, что увеличивает продолжительность жизни больных. Морфологическим критерием эффективности лечения считают уменьшение отложений амилоида в тканях, что в настоящее время можно оценить, применяя радиоизотопную сцинтиграфию с сывороточным Р-компонентом амилоида. Кроме основных терапевтических режимов, лечение амилоидоза должно включать симптоматические методы, направленные на уменьшение выраженности застойной недостаточности кровообращения, аритмии, отечного синдрома, коррекцию артериальной гипер- и гипотонии.
Целью терапии вторичного амилоидоза служит подавление продукции белка-предшественника SAA [19, 20], что достигается лечением хронического воспаления, в том числе и хирургическим (секвестрэктомия при остеомиелите, удаление доли легкого при бронхоэктатической болезни, опухоли, туберкулезе).
Особое значение в настоящее время придают терапии ревматоидного артрита, учитывая его лидирующее положение среди причин вторичного амилоидоза. Базисная терапия ревматоидного артрита цитостатическими лекарственными средствами (метотрексатом, циклофосфамидом, хлорамбуцилом) или современными антицитокиновыми средствами (блокаторы эффектов фактора некроза опухоли альфа, интерлейкины 1 и 6, блокаторы СD20 В-лимфоцитов и др.), назначаемая на длительный срок (более 12 мес.), уменьшает риск развития амилоидоза. У пациентов с уже развившимся амилоидозом это лечение позволяет в большинстве случаев уменьшить клинические проявления амилоидной нефропатии. В результате подобной терапии отмечают снижение выраженности протеинурии, купирование нефротического синдрома, стабилизацию функции почек. У части пациентов удается предотвратить развитие ХПН или замедлить ее прогрессирование, что существенно улучшает прогноз. Об эффективности лечения свидетельствует также нормализация концентрации С-реактивного белка в крови.
Средством выбора для лечения АА-амилоидоза при периодической болезни служит колхицин. При его постоянном приеме можно полностью избежать рецидивирования приступов у большинства больных, предотвращая у них также развитие амилоидоза. При развившемся амилоидозе длительный, возможно пожизненный, прием колхицина в дозе 1,8–2 мг/сут приводит к ремиссии, выражающейся в ликвидации нефротического синдрома, уменьшении или исчезновении протеинурии у больных с нормальной функцией почек. При наличии ХПН начальную дозу лекарственных средств уменьшают в зависимости от величины клубочковой фильтрации, хотя в случае снижения концентрации креатинина в крови возможно повышение дозы до стандартной. Колхицин также предотвращает рецидив амилоидоза в трансплантированной почке. Больные хорошо переносят данное лекарственное средство. Если эффективность колхицина при амилоидозе в рамках периодической болезни не вызывает сомнений, то имеются лишь единичные работы, свидетельствующие о его успешном применении у больных вторичным амилоидозом. Кроме колхицина, при АА-амилоидозе применяют диметилсульфоксид, вызывающий резорбцию амилоидных отложений. Однако использование его в высоких дозах (не менее 10 г/сут), необходимых для успешного лечения, ограничено из-за крайне неприятного запаха.
При AL-амилоидозе, как и при миеломной болезни, лечение должно быть направлено на подавление пролиферации клона плазматических клеток для уменьшения продукции ЛЦИ. Наибольший опыт лечения накоплен для мелфалана в сочетании с преднизолоном [21]. Лечение продолжают 7-дневными курсами с интервалом 4–6 недель на протяжении 12–24 месяцев. Доза мелфалана составляет 0,15 мг/кг массы тела в сутки, преднизолона – 0,8 мг/кг массы тела в сутки. У больных с ХПН (скорость клубочковой фильтрации менее 40 мл/мин) дозу мелфалана уменьшают на 50%. Эта схема лечения характеризуется низким риском осложнений химиотерапии и может применяться у абсолютного большинства больных, даже при наличии тяжелых висцеральных проявлений амилоидоза. Однако эффект этой терапии достигается только у 18–30% больных.
В настоящее время разработан эффективный иммунохимический метод оценки ремиссии плазмоклеточной дискразии у больных амилоидозом – определение свободных ЛЦИ в сыворотке (Freelite). Ранее применявшиеся методы не позволяли отличить пул свободных ЛЦИ от пула связанных с иммуноглобулинами, что резко снижало чувствительность методов. Благодаря методу Freelite, который базируется на применении антител к скрытым эпитопам ЛЦИ, появилась возможность количественной оценки пула свободных ЛЦИ, впервые были сформулированы критерии нормальной продукции ЛЦИ. В настоящее время во всем мире метод Freelite стал стандартом оценки эффективности терапии и мониторирования течения болезни у больных амилоидозом [22, 23].
С целью повышения эффективности лечения широко применялись попытки лечения более агрессивными схемами химиотерапии с включением винкристина, доксорубицина, циклофосфана, мелфалана, дексаметазона в разных комбинациях. Наибольшая эффективность достигнута при химиотерапии с использованием высоких доз. Так, в 1996 г. были опубликованы предварительные результаты (R.L. Comenzo и соавт.) лечения 5 больных AL-амилоидозом внутривенными вливаниями мелфалана в дозе 200 мг/м² поверхности тела с последующим введением аутологичных стволовых клеток (CD34+) крови [24]. Аутологичные стволовые клетки получают методом лейкофереза крови больного после предварительной их мобилизации из костного мозга под влиянием введенного извне гранулоцитарного колониестимулирующего фактора. Однако тяжелый агранулоцитоз и другие осложнения этой терапии существенно ограничивают применение терапии сверхвысокими дозами мелфалана, в частности, у больных с недостаточностью кровообращения. В последние годы показана высокая эффективность при относительно удовлетворительной переносимости схемы «мелфалан (0,15 мг/кг 4 дня) в сочетании с дексаметазоном (20 мг/сут в 1–4-е и 9–12-е дни)» ежемесячными курсами [25]. В настоящее время эта схема стала первой линией терапии AL-амилоидоза. В качестве второй линии терапии обсуждаются схемы с включением бортезомиба и талидомида [26, 27]. Кардиотоксичность и нейротоксичность этих препаратов не позволяют рекомендовать их в качестве препаратов первой линии выбора, несмотря на высокую эффективность в отношении плазмоклеточной дискразии.
Основной целью лечения А-бета-2-М-амилоидоза является уменьшение поступления в ткани бета-2-микроглобулина. Поскольку способы подавления его продукции в настоящее время отсутствуют, необходимо увеличить клиренс бета-2-микроглобулина путем проведения современных методов очищения крови.
Широко распространено мнение о том, что наиболее эффективным методом выведения бета-2-микроглобулина является трансплантация почки. Эта точка зрения подкреплена высокой эффективностью трансплантации в отношении костных болей, характерных для диализного амилоидоза. В настоящее время установлено, что причиной костных болей, так же как и костных кист, является макрофагальное воспаление, характерное для этого типа амилоидоза. Быстрое исчезновение болей после трансплантации является следствием назначения стероидов и цитостатиков, необходимых для предотвращения отторжения трансплантата и одновременно подавляющих макрофагальное воспаление в зоне депозиции амилоида. На поздних этапах амилоидогенеза зависимость макрофагального воспаления от поставки бета-2-микроглобулина в ткани снижается, и улучшение клиренса этого белка после трансплантации не предупреждает дальнейшее прогрессирование костных кист и эрозий. Таким образом, трансплантация способна предотвратить прогрессирование диализного амилоидоза только на ранних, в основном доклинических, стадиях амилоидоза [28].
В этой связи в лечении диализного амилоидоза большое значение придают современным диализным технологиям увеличения клиренса бета-2-микроглобулина. При проведении стандартной процедуры гемодиализа с использованием низкопоточных мембран (диффузионная модель) клиренс бета-2-микроглобулина существенно ограничен, так как этот белок по своей массе (11 800 Да) приближается к классу так называемых средних молекул. Однако применение высокопоточных синтетических мембран и сочетание диффузионного механизма очищения крови с конвективным приводят к существенному повышению эффективности выведения бета-2-микроглобулина. Так, было показано, что лечение гемодиафильтрацией в режиме online (режим ГДФ ONLINE предусматривает использование в качестве замещающего раствора сверхчистого диализата, который готовится непосредственно в аппарате для гемодиализа) позволяет добиться значительного снижения постдиализного уровня бета-2-микроглобулина (на 70% и более) [29]. В этой связи наиболее предпочтительным методом гемодиализа с точки зрения профилактики и лечения диализного амилоидоза является высокоэффективная ГДФ ONLINE с использованием синтетических мембран и скоростью подачи замещающего раствора не менее 100 мл/мин. Пациенты, которые получали ГДФ ONLINE с объемом замещения не менее 24 л за 4 часа процедуры, имели достоверно более существенное (на 72,7%) снижение сывороточного уровня бета-2-микроглобулина по сравнению с пациентами, получавшими стандартный гемодиализ на низкопоточных мембранах (на 49,7%) [30].
Результаты недавно завершенного исследования CONTRAST (CONvective TRAnsport STudy), посвященного влиянию конвективного транспорта на сывороточный уровень бета-2-микроглобулина, свидетельствуют о том, что через 6 месяцев у пациентов, которым проводится гемодиафильтрация, уровень бета-2-микроглобулина в сыворотке достоверно ниже, чем у пациентов на низкопоточном гемодиализе [31].
Дальнейшие перспективы в развитии гемодиализа во многом связаны с технологическим усовершенствованием и широким распространением методики ГДФ ONLINE в клинической практике. В частности, усовершенствованная техника ГДФ ONLINE – MIXED ГДФ – позволяет существенно увеличить эффективность конвективного транспорта, в том числе перенос средних молекул, в безопасном для пациента режиме [32–34].
Большое значение имеет применение современных синтетических диализных мембран, которые способны адсорбировать значительные количества бета-2-микроглобулина, в результате чего концентрация этого белка в крови в течение процедуры гемодиализа может снижаться на 30–40% [29]. Разработаны также специальные сорбционные колонки с высокими показателями очищения крови от бета-2-микроглобулина, однако их широкое применение сдерживается высокой себестоимостью [35–37].
Поскольку важным компонентом диализного амилоидоза является макрофагальное воспаление, большое значение имеет использование высокоочищенных растворов для приготовления диализата. G. Lonnemann и другие исследователи сообщают о том, что применение ультрачистых диализных жидкостей во время лечения конвективными методами позволяет снизить частоту синдрома запястного канала на 50% [37, 38].
В качестве симптоматической терапии больным диализным амилоидозом может быть рекомендовано местное применение стероидных мазей при болях, в литературе обсуждаются также показания к применению стероидов внутрь и в инъекциях, однако их использование ограничено из-за тяжелой ренальной остеодистрофии. В этой связи представляется перспективным применение у таких больных современных препаратов, подавляющих эффекты фактора некроза опухоли, интерлейкина-1 и интерлейкина-6.
Средством выбора для лечения АTTR-амилоидоза служит трансплантация печени, при которой удается удалить источник синтеза амилоидогенного предшественника. Трансплантация печени существенно задерживает прогрессирование амилоидоза, в первую очередь нервной системы [39]. В то же время накопленные депозиты амилоида в тканях, в особенности в сердце, способны адсорбировать также и нормальный транстиретин и тем самым способствовать дальнейшему прогрессированию амилоидоза [6]. В этой связи в настоящее время широко обсуждаются возможности стабилизации нормального транстиретина и предотвращения его амилоидогенности с помощью фармакологических препаратов (diflunisal) [40].
Поскольку ХПН служит одной из основных причин смерти больных системным амилоидозом, проведение гемодиализа или постоянного амбулаторного перитонеального диализа позволяет улучшить прогноз этих пациентов, в частности, выживаемость этих больных связывают с уровнем бета-2-микроглобулина [41–43].
Выживаемость больных амилоидозом при проведении гемодиализа, независимо от типа амилоидоза, сопоставима с выживаемостью больных другими системными заболеваниями и сахарным диабетом. Постоянный амбулаторный перитонеальный диализ имеет некоторые преимущества перед гемодиализом, поскольку нет необходимости в постоянном сосудистом доступе, отсутствует артериальная гипотония во время процедуры диализа, а у больных с AL-типом амилоидоза во время процедуры возможно удаление легких цепей иммуноглобулинов.
Трансплантация почки одинаково эффективна при обоих типах системного амилоидоза. Пятилетняя выживаемость больных и трансплантата составляет 65 и 62% соответственно и сопоставима с таковыми показателями других групп больных с ХПН. Трансплантация почки показана больным с медленным прогрессированием амилоидоза без поражения сердца и ЖКТ. Амилоидоз в трансплантированной почке возникает, по разным данным, примерно у 30% больных, однако он служит причиной потери трансплантата всего у 2–3% пациентов.
Прогноз при амилоидозе
Амилоидоз характеризуется неуклонно прогрессирующим течением. Прогноз заболевания зависит от типа амилоида, степени вовлечения различных органов, главным образом сердца и почек, наличия и характера предрасполагающего заболевания.
Наиболее серьезен прогноз при AL-амилоидозе. По данным клиники Мейо, средняя продолжительность жизни больных этим типом амилоидоза составляет лишь 13,2 мес., 5-летняя выживаемость – 7%, 10-летняя – всего 1%. При этом самая низкая продолжительность жизни отмечена у пациентов с застойной недостаточностью кровообращения (6 мес.) и ортостатической артериальной гипотонией (8 мес.) [2, 44, 45]. Наиболее частыми причинами смерти больных с AL-типом амилоидоза бывают сердечная недостаточность и нарушения ритма сердца (48%), уремия (15%), сепсис и инфекции (8%). Несмотря на то что смерть от уремии отмечают значительно реже, чем от кардиальных причин, ХПН разной степени выраженности регистрируют более чем у 60% умерших.
Прогноз при АА-амилоидозе более благоприятен и зависит, главным образом, от характера предрасполагающего заболевания и возможности его контроля. Средняя продолжительность жизни больных с этим типом амилоидоза от момента верификации диагноза составляет 30–60 мес. (большая при вторичном амилоидозе, меньшая при амилоидозе в рамках периодической болезни). Эффективное лечение предрасполагающих заболеваний, в том числе полное излечение туберкулеза или хронических нагноений, не исключает возможности развития амилоидоза в дальнейшем, однако замедляет его прогрессирование, улучшая прогноз. Эффективная терапия ревматоидного артрита позволяет продлить течение амилоидной нефропатии, замедляя наступление ХПН. Основной причиной смерти больных АА-типом амилоидоза служит почечная недостаточность.
Достижения последних лет в изучении проблемы амилоидоза, позволившие сформулировать четкие критерии классификации клинических форм амилоидоза и подходы к лечению, дали возможность существенно улучшить прогноз больных разными типами амилоидоза.
Амилоидоз:Причины,Симптомы,Лечение | doc.ua
Виды
- Первичный амилоидоз часто вызван изменениями плазматических клеток при миеломной болезни, моноклональной гипергамма-глобулинемии или болезни Вальденстрема. Сложный белково-полисахаридный комплекс складывается из легких цепей Ig, а при вышеуказанных болезнях синтез таких цепей быстро увеличивается.
- Вторичный амилоидоз бывает после хронических воспалительных заболеваний (это могут быть: ревматоидный артрит и остеомиелит, бронхоэктатическая болезнь и малярия, туберкулез или лепра). В таком случае амилоид слагается из фибриллярного белка амилоида и сывороточного амилоидного белка (продуктов распада).
- Идиопатический амилоидоз. Обычно является врожденной ферментопатией. Различают некоторые формы семейного амилоидоза, например, амилоидоз кожи при средиземноморской лихорадке (пароксизмальный полисерозит, проявляющийся лихорадкой, болями в животе, также артритом, плевритом и высыпаниями по кожному покрову).
- Старческий или амилоидоз в преклонном возрасте.
- Диализный амилоидоз случается при проведении внепочечного очищения крови при выявленной почечной недостаточности.
Причины
Причины различного поражения органов человека – почек, кишечника или кожи – пока не известны науке. На окончательную постановку диагноза влияет электронная микроскопия.
Симптомы
Симптомы и протекание болезни различны и зависят от степени распространенности и локализации амилоидных отложений в органах, также от времени течения заболевания и наличия осложнений. Так, существует целый комплекс симптомов, которые связаны с поражением некоторых органов.
Амилоидоз симптомы:
- поражение некоторых отделов пищеварительной системы вызывает амилоидоз пищевода, для которого характерна дисфагия при глотании твердой или плотной сухой пищи, также бывает отрыжка;
- амилоидоз желудка часто протекает вместе с амилоидозом кишечника и некоторых других органов. Симптомами выступают диспепсические расстройства и чувство тяжести после приема пищи;
- амилоидоз кишечника – частое заболевание, которое выражается в дискомфорте и тяжести, бывает, выражается тупыми болями в животе, запорами и диареей. Изолированный опухолевидный амилоидоз кишечника протекает в виде опухоли с болями и непроходимостью кишечника, и узнают о нем часто прямо на операционном столе;
- амилоидоз печени возникает также часто. При таком виде болезни происходит уплотнение и увеличение печени, а посредством пальпации прощупываются ровные края, но безболезненно. Нечасто протекает болезнь с болями в правом подреберье или с диспепсическими явлениями, спленомегалией, желтухой или геморрагическим синдромом;
- амилоидоз поджелудочной железы проявляется при хроническом панкреатите, которому сопутствует тупая боль в левом подреберье и диспепсические явления;
- амилоидоз сердца приводит к отложению белково-полисахаридного комплекса в тканях сердца, что выражается позже в гипертрофии миокарда, нарушением его сокращений, в развитии хронической недостаточности кровообращения, аритмии и гипертензии;
- амилоидоз почек протекает при любой форме амилоидоза. Так, главный симптом амилоидоза почек – протеинурия, развивающаяся при любых его формах, но характерна вторичному заболеванию. Пациенты часто длительное время не имеют никаких жалоб. А позже, при появлении отечности, артериальной гипотензии и почечной недостаточности, также при тромбозах почечных вен, сопровождающихся болью и анурией, приводят больных амилоидозом почек в больницу на консультацию к врачу;
- также при амилоидозе поражаются и другие системы и органы человека. Нарушаются функции сердечно-сосудистой системы, высыпания в виде полупрозрачных узелков на коже, проявляется пурпура, различные отеки.
Диагностика
Диагностика амилоидоза проводится лабораторными исследованиями и другими специальными исследованиями органов человека.
При распознавании амилоидоза лабораторными исследованиями выявляют анемию в крови, лейкоцитоз, повышение СОЭ (скорость оседания эритроцитов), гипопротеинемию и гиперглобулинемию, гипонатриемию, гипопротромбинемию и гипокальциемию. При поражении печени проявляется гиперхолестеринемия, иногда гипербилирубинемия. Проводят оценку функций щитовидки, почек. Исследуют мочу, выявляя в осадке не только белок, но и лейкоциты и эритроциты, цилиндры. Увеличенное содержание амилоида в моче и крови определяет первичный амилоидоз. При выявлении признаков воспалительных заболеваний проявляется вторичный амилоидоз. Проводится копрологическое исследование с выявлением стеатореи и амилореи, креатореи.
Иные исследования для выявления амилоидоза – это эхокардиография, рентген, при котором:
- пищевод гипотоничен, а перистальтика ослаблена, при горизонтальном положении больного бариевая взвесь надолго задерживается в пищеводе – это амилоидоз пищевода;
- эвакуация содержимого из желудка, сглаженные складки слизистой оболочки, ослабленная перистальтика – амилоидоз желудка;
- наблюдается сглаженность рельефа слизистой оболочки кишки и развернутость кишечных петель, утолщение складок – амилоидоз кишечника.
Также проводится биопсия.
При поражениях ЖКТ наблюдают язвенную болезнь желудка и хронический гастрит.
Синдром запястного канала и периферическая полиневропатия, рестриктивная кардиомиопатия, нефротический синдром, обструкция мочевыводящих путей, острый канальцевый некроз, симметричный полиартрит, заболевания легких, токсическое воздействие на почки, болезнь Альцгеймера и деменция при множественных инфарктах мозга приводят к амилоидозу.
Лечение
Больным амилоидозом показаны:
- амбулаторный режим, если не наблюдается тяжелое состояние пациента;
- долгий прием сырой печени в течение двух лет по 100–120 грамм в сутки;
- ограничение употребления белка и соли в еде;
- лечение заболевания, симптомы которого похожи на амилоидоз. После излечения симптомы пропадают. Это вторичный амилоидоз;
- если амилоидоз кишечника проявляется диареей, то прописывают вяжущие средства, например, нитрат висмута основного или адсорбенты.
Хирургическое вмешательство при заболевании
Улучшение состояния человека возможно посредством спленэктомии, которая уменьшает количество амилоида, образуещегося в организме больного. При изолированном опухолевидном амилоидозе ЖКТ необходимо оперативное вмешательство.
При первичном амилоидозе необходимо частое и периодическое определение уровня амилоидных белков, чтобы оценить правильность и эффективность лечения заболевания. Также стоит обращать внимание и контролировать функции почек, чтобы наблюдать за лечением и эффективностью терапии.
При вторичном и диализном амилоидозах следует знать, что даже при проводимом лечении возникает хроническая почечная недостаточность, а также сердечная, поражаются суставы, возникает полиневропатия и интерстициальные заболевания легких.
Осложнениями амилоидоза можно считать: перфорацию язв, амилоидные язвы пищевода, также желудка, пищеводные и желудочно-кишечные кровотечения, стенозирование кишечника.
Возможна гипопротеинемия в тяжелой форме как следствие изменения процессов всасывания в кишечнике.
Течение и прогноз заболевания
Если развивается хроническая почечная недостаточность при первичном амилоидозе, то такие люди живут не больше года. Если сердечная недостаточность развита, таким пациентам жить остается не более четырех месяцев.
В общем, в среднем выживаемость держится в районе 12–14 месяцев, но по статистике женщины живут дольше мужчин.
При вторичном амилоидозе прогноз по выздоровлению и излечению от него немного лучше. Он также определяется посредством выявления основной болезни и возможностью ее лечения.
При семейном и диализном амилоидозах прогноз может быть разным. Хуже всего такая болезнь протекает у людей пожилого возраста.
СИСТЕМНЫЙ АМИЛОИДОЗ: диагноз, дифференциальный диагноз, лечение | #03/04
«Амилоидоз» — термин, объединяющий группу заболеваний, которые отличаются большим разнообразием клинических проявлений и характеризуются внеклеточным отложением нерастворимых патологических фибриллярных белков в органах и тканях. Впервые эта патология была описана в XVII в. Боне — саговая селезенка у больного с абсцессом печени. В середине XIX в. Вирхов применил ботанический термин «амилоид» (от греч. amylon — крахмал) для описания внеклеточного материала, обнаруженного в печени при аутопсии, так как полагал, что он близок по структуре к крахмалу. Впоследствии была установлена белковая природа отложений, однако термин «амилоид» сохранился до настоящего времени.
В 20-е гг. XX столетия Бенхольд предложил окрашивать амилоид конго-красным, затем был обнаружен эффект двойного лучепреломления в поляризованном свете — изменение кирпично-красной окраски на яблочно-зеленую. В 1959 г. Коген и Калкинс с помощью электронной микроскопии установили фибриллярную структуру амилоида.
Эволюцию претерпели и клинические представления об амилоидозе: Рокитанский в 1842 г. установил связь «сальной болезни» с туберкулезом, сифилисом, риккетсиозами; Уилкс в 1856 г. описал «жирные органы» у больного, не имевшего никаких сопутствующих заболеваний; Аткинсон в 1937 г. обнаружил амилоидоз у пациентов с миеломной болезнью. Выделены были старческие (Сойка, 1876) и наследственные (Андраде, 1952) формы заболевания, амилоидоз разделяли на генетический, первичный и вторичный, и, наконец, в 1993 г. была принята классификация ВОЗ, построенная на специфичности основного фибриллярного белка амилоида.
В нашей стране большой вклад в развитие представлений об амилоидозе внесли Е. М. Тареев, И. Е. Тареева, В. В. Серов. Огромная роль в изучении первичного и генетических вариантов амилоидоза и периодической болезни принадлежит О. М. Виноградовой, чьи монографии, изданные в 1973 и 1980 гг., не утратили своей актуальности и в наши дни.
В настоящее время амилоидоз принято клинически разделять на системные и локальные формы. Среди системных форм, в зависимости от состава фибриллярных отложений, выделяют четыре типа (табл. 1).
К локальным формам амилоидоза в настоящее время относят болезнь Альцгеймера (A-бета, фибриллы состоят из β-протеина, откладывающегося в головном мозге), амилоидоз островков поджелудочной железы, возможно, имеющий патогенетическую связь с диабетом 2 типа, амилоидоз, возникающий в эндокринных опухолях, амилоидные опухоли кожи, назофарингеальной области, мочевого пузыря и другие редкие виды.
AL-амилоидоз
Развитие AL-амилоидоза возможно при миеломной болезни, болезни Вальденстрема, В-клеточных лимфомах, и оно может быть идиопатическим при первичном амилоидозе. Все эти варианты объединены общим патогенезом, первичный амилоидоз представляет наибольшую трудность для распознавания в связи с отсутствием явных признаков гематологического заболевания, поэтому именно на данной форме стоит остановиться подробно.
При первичном амилоидозе, доброкачественной плазмоклеточной дискразии, родственной множественной миеломе, аномальные клоны плазматических клеток костного мозга продуцируют амилоидогенные иммуноглобулины. Некоторые аминокислоты в вариабельных участках легких цепей этих иммуноглобулинов занимают необычную позицию, что приводит к их нестабильности и обусловливает склонность к фибриллогенезу. У больных с первичным амилоидозом содержание плазматических клеток в костном мозге повышено до 5—10% (в норме их менее 4%, при миеломной болезни — более 12%), и они продуцируют определенный изотип легких цепей иммуноглобулинов, преобладающий при иммуногистохимическом окрашивании. Свободные моноклональные легкие цепи преобладающего лямбда- или (реже) каппа-изотипа определяются в крови и в моче, но содержание их ниже, чем при миеломной болезни.
Клиническая картина первичного амилоидоза многообразна и определяется преимущественным вовлечением в патологический процесс тех или иных органов — сердца, почек, нервной системы, желудочно-кишечного тракта, печени и др. Первыми симптомами являются слабость и потеря веса, но на этой стадии, до появления органных симптомов, диагноз устанавливается крайне редко.
Органами-мишенями при AL-амилоидозе чаще всего становятся почки и сердце. Поражение почек проявляется нефротическим синдромом, персистирующим и при наступлении ХПН, гематурия и артериальная гипертензия не характерны.
При отложении амилоида в миокарде развиваются разнообразные нарушения ритма, прогрессирующая сердечная недостаточность, чему могут предшествовать бессимптомные изменения на ЭКГ в виде снижения вольтажа зубцов. Эхокардиографическое исследование выявляет концентрическое утолщение стенок левого и правого желудочков, уменьшение объема полостей сердца, умеренное снижение фракции выброса, диастолическую дисфункцию миокарда левого желудочка.
Часто отмечаются симптомы вовлечения нервной системы — вегетативной, в виде ортостатической гипотензии, и периферической — в виде расстройств чувствительности. В последние годы стали описывать также поражения ЦНС, хотя ранее считалось, что они не характерны для первичного амилоидоза.
Диспептические явления (ощущение переполнения, запоры, поносы) и синдром нарушенного всасывания могут быть обусловлены как поражением вегетативной нервной системы, так и амилоидозом желудочно-кишечного тракта. Очень характерна гепатомегалия, природу которой следует дифференцировать между застойными явлениями вследствие сердечной недостаточности и амилоидным поражением печени. Последнее подтверждается повышением уровня щелочной фосфатазы сыворотки крови. Селезенка поражается часто, однако спленомегалия обнаруживается не всегда и большого клинического значения не имеет.
Макроглоссия, классический признак первичного амилоидоза, отмечается у 20% пациентов, инфильтрация мягких тканей может приводить к атрофии мышц, кожи, дистрофии ногтей, алопеции и появлению опухолевидных образований — амилоидом.
Реже встречается поражение сосудов, симптомами которого являются периорбитальная пурпура — «глаза енота» и экхимозы. Могут наблюдаться кровотечения, в том числе мочепузырные, обусловленные как изменением сосудистой стенки, так и нарушением свертывающей системы, в первую очередь дефицитом X-фактора, который связывается с амилоидом. Дефицитом факторов свертывания принято объяснять и характерный для амилоидоза тромбоцитоз.
Амилоидоз легких часто обнаруживается лишь при аутопсии. Однако в некоторых случаях одышка, кровохарканье и гидроторакс могут быть обусловлены не только застойной сердечной недостаточностью и нефротическим синдромом, но и амилоидным поражением легких. Возможны отложение амилоида в альвеолах и развитие легочных амилоидом. Рентгенологически могут выявляться сетчатые и нодулярные изменения в легочной ткани.
Поражение надпочечников может привести к надпочечниковой недостаточности, нередко остающейся нераспознанной, так как гипотензия и гипонатриемия рассматриваются как симптомы сердечной недостаточности и поражения вегетативной нервной системы. У 10—20% больных может иметь место гипотиреоз как проявление поражения щитовидной железы, нередко встречается увеличение подчелюстных слюнных желез.
Диагноз первичного амилоидоза помимо указанных клинических черт, которые могут быть сходными и при вторичном амилоидозе, базируется на ряде лабораторных данных. У 85% пациентов при иммуноэлектрофорезе белков сыворотки крови и мочи выявляются моноклональные иммуноглобулины. При рутинных исследованиях те же моноклональные иммуноглобулины обнаруживаются в моче в виде белка Бенс-Джонса. Биопсия костного мозга позволяет провести дифференциальный диагноз с множественной миеломой, а также выявить умеренное повышение количества плазматических клеток и их моноклональность при иммуногистохимическом окрашивании.
Однако даже сочетания характерной клинической картины и наличия моноклональных плазмоцитов и белков еще недостаточно для подтверждения диагноза первичного амилоидоза. Решающую роль здесь играют данные биопсии. Наименее инвазивной является аспирация подкожной жировой клетчатки передней брюшной стенки, дающая 80—90% положительных результатов при AL-амилоидозе (в нашей стране этот метод пока не нашел применения). Определенное диагностическое значение имеет биопсия десны и слизистой оболочки прямой кишки, но процент положительных результатов широко варьирует, в зависимости от стадии процесса, поэтому целесообразно выполнение биопсии одного из пораженных орга-нов — почки, печени, сердца, дающее почти 100% положительных результатов при амилоидозе AL-типа.
В первую очередь биопсийный материал окрашивается конго-красным. При обнаружении конгофилии исследуемого материала необходимо его исследование в поляризованном свете, эффект двойного лучепреломления характерен только для амилоида, другие конгофильные вещества яблочно-зеленой окраски не приобретают. После этого желательно типирование амилоида. Наиболее точным является иммуногистохимический метод с использованием моноклональных антител к белкам-предшественникам амилоида. Однако в настоящее время в нашей стране он практически недоступен. Поэтому для диагностики используется окраска с помощью растворов щелочного гуанидина или перманганата калия, что позволяет, хотя и косвенно, определить тип фибриллярных отложений.
Прогноз при первичном амилоидозе хуже, чем при других формах заболевания, средняя продолжительность жизни не превышает двух лет, при наличии поражения сердца или мультисистемного поражения без лечения больные погибают в течение нескольких месяцев. Наиболее частыми причинами смерти являются сердечная и почечная недостаточность, сепсис, сосудистые осложнения и кахексия. Патогенетическое сходство с миеломной болезнью позволяет рассчитывать на торможение прогрессирования заболевания при химиотерапии, проводимой с целью подавления моноклональных плазмоцитов. Существует несколько схем лечения (табл. 2).
Применение химиотерапии в случае успеха лечения позволяет увеличить продолжительность жизни больных на срок от 10 до 18 мес. Но эффективность терапии невысока, в частности, в связи с тем, что во многих случаях прогрессирование заболевания приводит к гибели больных до завершения курса лечения, а также из-за развития цитопении, инфекционных осложнений, фатальных нарушений ритма при лечении сверхвысокими дозами дексазона. Применение высоких доз мельфолана с трансплантацией аутологичных стволовых клеток позволяет достичь ремиссии более чем в 50% случаев, однако использование этого метода ограничено тяжестью состояния, возрастом больных, функциональными нарушениями со стороны сердца и почек. Во многих случаях возможна лишь симптоматическая поддерживающая терапия.
AA-амилоидоз
Развитие AA-амилоидоза происходит при хронических воспалительных процессах, предшественниками AA-амилоида являются сывороточные острофазовые белки, α-глобулины, продуцируемые клетками разных типов, в основном нейтрофилами и фибробластами. Вторичный амилоидоз развивается при ревматоидном артрите, болезни Бехтерева, псориатическом артрите, различных опухолях, лимфогранулематозе, неспецифическом язвенном колите и болезни Крона, при периодической болезни (семейной средиземноморской лихорадке), а также при туберкулезе, остеомиелите, бронхоэктатической болезни.
Характерными клиническими особенностями АА-амилоидоза является поражение почек у большинства пациентов, а также относительно редкое поражение печени и/или селезенки (около 10%) и сердца (выявляется лишь при эхокардиографии). Макроглоссия для вторичного амилоидоза не характерна. Диагноз основан на сочетании амилоидоза почек и хронического воспалительного заболевания, подтверждением служит иммуногистохимическое окрашивание биопсийного материала, в нашей стране используются уже упомянутые выше косвенные окрасочные методы.
Прогноз во многом зависит от природы основного заболевания, при естественном течении у трети больных через 5 лет от момента выявления протеинурии развивается почечная недостаточность. При периодической болезни пятилетняя выживаемость составляет 25%.
Лечение основано на подавлении очага — источника продукции сывороточных белков-предшественников. Удаление опухолей, секвестрэктомия, резекция кишки, лечение туберкулеза, уменьшение активности ревматоидного артрита (при использовании цитостатиков) приводят к прекращению прогрессирования амилоидоза, а иногда и к обратному развитию клинических проявлений, в частности нефротического синдрома.
Применение колхицина при периодической болезни является методом выбора, эффективность его доказана, лечение предотвращает развитие амилоидоза и тормозит его прогрессирование. При других формах вторичного амилоидоза эффективность колхицина не подтверждена.
Сенильные и наследственные формы системного амилоидоза, так же как и локальные формы, встречаются редко, диализный амилоидоз хорошо известен специалистам, в общей практике с ним сталкиваться практически не приходится.
Симптоматическая терапия зависит не от типа амилоидоза, а от пораженных органов-мишеней (табл. 3).
Амилоидоз, особенно первичный, считается нечастой патологией, однако в действительности он не столько редко встречается, сколько с трудом диагностируется. Адекватная диагностика требует не только знания клиники и патогенеза данного заболевания, но и наличия определенных диагностических возможностей. Чтобы проиллюстрировать это положение, приведем собственные данные (см. таблицу 4). В нефрологическом отделении МГКБ имени С. П. Боткина в 1993—2003 гг. наблюдалось 88 больных, которым был поставлен диагноз амилоидоза.
Диагноз был подтвержден морфологически у всех больных с AL-амилоидозом, старческим и неуточненным по типу амилоидозом, и у 30 пациентов со вторичным амилоидозом — всего в 53 случаях. У 12 больных выполнялась биопсия почки, а у двоих — биопсия печени, у восьми — биопсия кишки, в 12 случаях — десны, еще в 19 случаях диагноз был подтвержден при морфологическом исследовании секционного материала.
В большинстве случаев диагноз амилоидоза был установлен впервые в результате обследования в нефрологическом отделении. Нами было проведено сопоставление среди больных с AL-амилоидозом направительного и клинического диагнозов (табл. 5).
Лишь в двух случаях из 20 (10%) направительным диагнозом был «первичный амилоидоз», причем одному из этих больных он был поставлен в клинике терапии и профзаболеваний ММА, а другому — в зарубежной клинике.
Все больные, у которых диагностировалась миеломная болезнь с развитием AL-амилоидоза, были переведены в гематологические отделения. Из 11 больных с первичным амилоидозом семь пациентов получали химиотерапию комбинацией мельфолана с преднизолоном внутрь прерывистыми курсами, четверо из них — в сочетании с диализным лечением, и еще одна больная — только диализное и симптоматическое лечение. Из числа этих больных пять человек умерли в сроки от двух недель до двух лет от начала лечения (все с почечной недостаточностью и полиорганным поражением), один больной находится на диализе, один больной был направлен на трансплантацию аутологичных стволовых клеток, и одна больная получает лечение до настоящего времени. У одного пациента химиотерапия отложена в связи с наличием длительно не рубцующейся язвы желудка, и еще двое больных отказались от лечения.
Среди больных с вторичным амилоидозом в нашем исследовании преобладали пациенты с ревматоидным артритом, на втором месте среди причин — хронический остеомиелит и псориатический артрит, остальные заболевания встречались реже (табл. 6).
Лечение ревматоидного артрита и псориатического артрита проводилось с применением цитостатиков (метатрексата, азатиоприна), хотя во многих случаях возможности терапии были ограничены из-за наличия ХПН и сопутствующей патологии. Больные с хроническим остеомиелитом были направлены в отделения гнойной хирургии. Пациенты с болезнью Бехтерева и болезнью Крона получали специфическое лечение, больные с ХНЗЛ и туберкулезом также были направлены в профильные стационары. Одна из больных с опухолью желудка была успешно оперирована, и на протяжение четырех лет наблюдения нефротический синдром постепенно регрессировал, в остальных случаях опухолей распространенность процесса позволяла проводить только симптоматическую терапию, больной с лимфогранулематозом поступил в терминальном состоянии. Смертность среди пациентов со вторичным амилоидозом составила 38% (за счет больных с далеко зашедшим поражением на момент постановки диагноза). Все больные с периодической болезнью получали терапию колхицином.
Особенности диагностики и применения современных методов лечения первичного амилоидоза можно проиллюстрировать на следующем примере: больная К., 46 лет, впервые госпитализирована в конце октября 2002 г. с жалобами на отеки на ногах, сердцебиения, аменорею. В анамнезе — простудные заболевания, аппендэктомия, два нормальных срочных родоразрешения, указаний на заболевание почек, какие-либо хронические заболевания нет. В апреле 2002 г. перенесла острую пневмонию в верхней доле правого легкого, лечилась амбулаторно, получала инъекции абактала, линкомицина. В связи с локализацией пневмонии была обследована в туберкулезном диспансере, диагноз туберкулеза исключен. В начале июня впервые появились отеки на ногах, по поводу которых не обследовалась. Отеки через короткое время самостоятельно ликвидировались, затем возобновились. Больная была госпитализирована в терапевтический стационар, при обследовании выявлена протеинурия до 1,65%, гипопротеинемия (общий белок сыворотки крови 52 г/л), артериальное давление в норме (120/80 мм рт. ст.), мочевой осадок без изменений, креатинин плазмы также в пределах нормы. Установлен диагноз «острый гломерулонефрит», проведено лечение ампициллином, курантилом, гепарином, триампуром, выполнена тонзиллэктомия. Протеинурия сохранялась, отеки постепенно нарастали, в связи с чем для дальнейшего обследования и лечения больная с диагнозом «хронический гломерулонефрит» была направлена в больницу им. С. П. Боткина.
При осмотре — кожа чистая, обычной окраски, анасарка, отеки массивные, плотные, определяется асцит, периферические лимфатические узлы не увеличены. АД 110/70 мм рт. ст., тоны сердца звучные, ясные, ритмичные, ЧСС 90 уд/мин, печень и селезенка не увеличены, диурез до 1000 мл/сут, стул регулярный, без патологических примесей. При обследовании выявлен нефротический синдром — протеинурия 3 г/л, мочевой осадок скудный, гиподиспротеинемия, гиперлипидемия (общий белок сыворотки крови 39 г/л, альбумины 12 г/л, глобулины 7-30-15-19% соответственно α1-α2-β-γ холестерин 17,8 ммоль/л, β-липопротеиды 250 ЕД), при анализе мочи на белок Бенс-Джонса — реакция отрицательная, суточная экскреция 17-КС не снижена. Клинический анализ крови и другие биохимические показатели в пределах нормы, коагулограмма — выраженная гиперфибриногенемия, повышение уровня РКФМ. Исследование иммуноглобулинов крови: Ig-A — 0,35, Ig-M — 35,7 (две нормы), Ig-G — 1,96 г/л. Рентгенография органов грудной клетки, костей черепа и таза, УЗИ брюшной полости, почек, щитовидной железы, ЭХО-КГ без патологии, УЗИ малого таза — признаки аденомиоза тела матки, ЭГДС — рефлюкс-эзофагит, хронический гастрит. При осмотре невропатологом патологии не найдено, онкологом установлена фиброзно-кистозная мастопатия.
С целью уточнения генеза нефротического синдрома под местной анестезией под УЗ-наведением выполнена тонкоигольная пункционная биопсия правой почки, осложнений не было. При исследовании биоптата в мезангии клубочков и во внегломерулярных сосудах отмечается отложение амилоида. Амилоид загружает до 25% сосудистых петель клубочков. При иммуногистохимическом исследовании специфической люминисценции не найдено. При обработке препаратов раствором щелочного гуанидина в течение 2 ч конгофилия и их свойства в поляризованном свете сохраняются, что характерно для AL-амилоидоза.
Для выяснения природы AL-амилоидоза выполнено иммунохимическое исследование крови и мочи в лаборатории «Иммунотест». Выявлена М-лямбда парапротеинемия со снижением уровня поликлональных иммуноглобулинов и парапротеинурия Бенс-Джонса лямбда-типа на фоне массивной неселективной протеинурии. Больная была консультирована гематологом, высказано предположение о наличии болезни Вальденстрема, произведена трепанобиопсия костного мозга. Заключение: в имеющихся костно-мозговых полостях видны клетки всех трех ростков нормального гемопоэза, а также лимфоидные клетки, не образующие скоплений. Диагноз болезни Вальденстрема отвергнут в связи с отсутствием лимфоидной инфильтрации костного мозга, увеличения лимфоузлов и селезенки и отсутствием субстрата опухоли.
Установлен диагноз первичного амилоидоза с поражением почек, нефротическим синдромом, сохранной почечной функцией, признаков иных органных поражений не выявлено. С января 2003 г. начата химиотерапия мельфоланом 16 мг/сут и преднизолоном 100 мг/сут, курсами по четыре дня каждые шесть недель. Проводится также симптоматическое лечение: фуросемид, верошпирон, препараты калия, фамотидин, переливания альбумина. К настоящему времени проведено пять курсов химиотерапии с хорошей переносимостью, отеки уменьшились, протеинурия снизилась до 1,8 г/л, несколько уменьшилась выраженность гиподиспротеинемии (общий белок 46 г/л, альбумины 18 г/л, α2-глобулины 20%). Функция почек остается сохранной, креатинин плазмы 1,3 мг/Дл, признаков поражения других органов и систем при контрольных динамических обследованиях не выявлено.
Данный случай наглядно иллюстрирует тот факт, что для диагностики амилоидоза необходимо морфологическое, иммунологическое и иммунохимическое обследование. Так, у нашей пациентки наиболее очевидным клиническим диагнозом был «хронический гломерулонефрит», и в отсутствии возможности выполнения биопсии почки именно этот диагноз, скорее всего, и был бы поставлен. Никаких клинических указаний на системный характер заболевания, хронический воспалительный процесс, заболевание системы крови, за исключением повышения уровня Ig-M, у больной не было. И лишь полученные при исследовании почечного биоптата данные повлекли за собой трепанобиопсию костного мозга и иммунохимическое исследование, что в совокупности позволило поставить диагноз первичного амилоидоза до появления системных повреждений. Патогенетическая терапия была начата хотя и на фоне уже развившегося нефротического синдрома, но до наступления почечной недостаточности и при загрузке лишь 25% клубочков амилоидом, что прогностически относительно благоприятно.
В заключение отметим, что амилоидоз представляет собой тяжелое заболевание с высоким уровнем летальности, которое чрезвычайно трудно диагностировать, однако своевременное и качественное обследование больных позволяет поставить диагноз в более ранние сроки, а своевременное назначение адекватной терапии, в свою очередь, дает возможность улучшить прогноз в этой группе больных.
Литература
- Варшавский В. А., Проскурнева Е. П. Значение и методы морфологической диагностики амилоидоза в современной медицине // Практическая нефрология. — 1998. — 2:16-23.
- Виноградова О. М. Первичный и генетический варианты амилоидоза. — М.: Медицина, 1980.
- Захарова Е. В., Хрыкина А. В., Проскурнева Е. П., Варшавский В. А. Случай первичного амилоидоза: трудности диагностики и лечения // Нефрология и диализ. — 2002. — 1:54-61.
- Рамеев В. В. Особенности поражения почек при AA и AL-амилоидозе: дисс … канд. мед. наук. — М., 2003.
- Козловская Л. В., Варшавский В. А., Чегаева Т. В. и др. Амилоидоз: современный взгляд на проблему // Практическая нефрология. — 1998. — 2:24-26.
- Rodney H., Raymond L.C and Skinner M. // The systemic Amyloidoses; New England Journal of Medicine, 1997. — 337:898-909.
- Dhodapkar M.V., Jagannath S., Vesole d. et al // Treatment of AL-amyloidosis with dexamethasone plus alpha interferon / Leuc Lymphoma. 1997. — 27(3-4):351-365
- Gertz M.A., Lacy M.Q., Lust J.A. et all // Phase II trial of high-dose dexamethasone for previosly treated immunoglobulin light-chain amyloidosis. Am J Hematol, 1999,61(2):115-119.
- Gertz M.A., Lacy M.,Q., Lust J.A. et al // Phase II trial of high-dose dexamethasone of untreated patients with primary systenic amyloidosis. Med Oncol 1999.- 16(2):104-109
- Sezer O., Schmid P.,Shweigert M. et al // Rapid reversal of nephrotic syndrome due to primary systemic AL amyloidosis after VAD and subsequent high-dose chemotherapy with autologous stem sell support. Bone Marrow Transplant. 1999. — 23(9): 967-969.
- Sezer O., Neimoller K., Jakob C. et al // Novel approaches to the treatment of primary amyloidosis. Expert Opin Investig Grugs. 2000. — 9(10):2343-2350
- Sezer O., Eucker J., Jakob C., Possinger K. // Diagnosis and treatment of AL amyloidosis. Clin Nephrol. 2000. — 53(6):417-423.
- Skinner M. «Amyloidosis» Current Therapy in Allergy, Immunology, and Rheumatology. Mosby-Year Book. 1996. — 235-240.
- Palladini G., Anesi E., Perfetti V. et al. A modified high-dose dexamethasone regimen for primary systemic (AL) amyloidosis. British Journal of Haematology. 2001. — 113:1044-1046.
Е. В. Захарова
Московская городская клиническая больница им. С. П. Боткина
Таблица 2.Схемы лечения первичного амилоидоза
- Циклическое пероральное применение мельфолана (0,15-0,25 мг/кг веса в сутки) и преднизолона (1,5-2,0 мг/кг в сутки) по четыре—семь дней каждые четыре—шесть недель в течение года, до достижения курсовой дозы 600 мг
- Пероральное применение мельфолана в дозе 4 мг/сут в течение трех недель, затем, после двухнедельного перерыва — 2—4 мг/сут четыре дня в неделю постоянно, до достижения курсовой дозы 600 мг, в комбинации с преднизолоном
- Внутривенное введение высоких доз мельфолана (100–200 мг/мІ поверхности тела в течение двух дней) с последующей трансплантацией аутологичных стволовых клеток
- Внутривенное введение дексаметазона в дозе 40 мг в течение четырех дней каждые три недели — восемь циклов
- Внутривенное введение дексаметазона в дозе 40 мг в первый—четвертый, 9–12-й и 17–20-й дни 35-дневного цикла, три—шесть циклов, с последующим применением a-интерферона в дозе 3—6 млн единиц три раза в неделю
- Схема винкристин-доксорибуцин-дексаметазон (VAD)
Амилоидоз — Диагностика и лечение
Диагноз
Амилоидоз часто упускают из виду, поскольку признаки и симптомы могут имитировать симптомы более распространенных заболеваний.
Ранняя диагностика может помочь предотвратить дальнейшее повреждение органов. Точный диагноз важен, потому что лечение сильно различается в зависимости от вашего конкретного состояния.
Лабораторные исследования
Ваша кровь и моча могут быть проанализированы на аномальный белок, который может указывать на амилоидоз.В зависимости от ваших признаков и симптомов вам также могут пройти функциональные пробы щитовидной железы и печени.
Биопсия
Можно взять образец ткани и проверить на наличие признаков амилоидоза. Биопсия может быть взята из подкожного жира на животе (аспират жира), костного мозга или пораженного органа, например печени или почки. Специализированное исследование ткани может помочь определить тип амилоидного отложения.
Визуализирующие тесты
Изображения органов, пораженных амилоидозом, могут помочь определить степень вашего заболевания.Тесты могут включать:
- Эхокардиограмма. Эта технология использует звуковые волны для создания движущихся изображений, которые могут показать, насколько хорошо работает ваше сердце. Он также может указывать на поражение сердца, которое может быть специфическим для определенных типов амилоидоза.
- Магнитно-резонансная томография (МРТ). MRI использует радиоволны и сильное магнитное поле для создания подробных изображений органов и тканей вашего тела. Их можно использовать для оценки структуры и функции вашего сердца.
- Ядерная визуализация. В этом тесте крошечные количества радиоактивного материала (индикаторы) вводятся в вену. Это может выявить раннее повреждение сердца, вызванное определенными типами амилоидоза. Это также может помочь различать разные типы амилоидоза, что может помочь в принятии решения о лечении.
Лечение
Лекарства от амилоидоза нет. Но лечение может помочь справиться с признаками и симптомами и ограничить дальнейшее производство амилоидного белка.Если амилоидоз был вызван другим заболеванием, например ревматоидным артритом или туберкулезом, лечение основного заболевания может оказаться полезным.
Лекарства
- Химиотерапия. Многие из тех же типов лекарств, которые используются для лечения некоторых форм рака, используются при амилоидозе AL, чтобы остановить рост аномальных клеток, которые производят белок, ведущий к образованию амилоида.
- Сердечные препараты. Если ваше сердце поражено, ваш врач может порекомендовать препараты, разжижающие кровь, чтобы снизить риск образования тромбов, и лекарства для контроля частоты сердечных сокращений. Вам также может потребоваться ограничить потребление соли и принять лекарства, усиливающие мочеиспускание, что может снизить нагрузку на сердце и почки.
- Таргетная терапия. При некоторых типах амилоидоза такие препараты, как патисиран (Onpattro) и инотерсен (Тегседи), могут мешать командам, посылаемым ошибочными генами, которые создают амилоид.Другие препараты, такие как тафамидис (Vyndamax, Vyndaqel) и дифлунисал, могут стабилизировать кусочки белка в кровотоке и предотвратить их превращение в амилоидные отложения.
Хирургические и другие процедуры
- Трансплантация аутологичных стволовых клеток крови. Эта процедура включает в себя сбор ваших собственных стволовых клеток из крови через вену и их кратковременное хранение, пока вы проходите высокодозную химиотерапию. Затем стволовые клетки возвращаются в ваше тело через вену.Это лечение наиболее подходит для людей, у которых болезнь не запущена и сердце не сильно пострадало.
- Диализ. Если ваши почки были повреждены амилоидозом, вам может потребоваться диализ. В этой процедуре используется машина для регулярной фильтрации шлаков, солей и жидкости из вашей крови.
- Пересадка органов. Ваш врач может предложить операцию по замене сердца или почек, если отложения амилоида серьезно повредили эти органы.Некоторые типы амилоида образуются в печени, поэтому трансплантация печени может остановить это производство.
Клинические испытания
Изучите исследования клиники Мэйо, в которых тестируются новые методы лечения, вмешательства и тесты как средства предотвращения, обнаружения, лечения или контроля этого состояния.
Подготовка к приему
Вас могут направить к врачу, специализирующемуся на заболеваниях крови (гематологу).
Что вы можете сделать
- Запишите свои симптомы, включая те, которые могут показаться не связанными с причиной, по которой вы записались на прием.
- Составьте список всех ваших лекарств, витаминов и пищевых добавок.
- Запишите основную медицинскую информацию, включая другие состояния.
- Запишите ключевую личную информацию, включая любые недавние изменения или факторы стресса в вашей жизни.
- Запишите вопросы, которые задайте своему врачу.
- Попросите родственника или друга сопровождать вас, поможет вам вспомнить, что говорит врач.
Вопросы, которые следует задать врачу
- Какая наиболее вероятная причина моих симптомов?
- Какой у меня амилоидоз?
- Какие органы поражены?
- На какой стадии мое заболевание?
- Какие тесты мне нужны?
- Какое лечение мне нужно?
- Есть ли у меня риск долгосрочных осложнений?
- Какие побочные эффекты можно ожидать от лечения?
- Нужно ли мне соблюдать какие-либо ограничения в питании или активности?
- У меня другое состояние здоровья.Как мне лучше всего управлять ими вместе?
В дополнение к вопросам, которые вы подготовили задать своему врачу, не стесняйтесь задавать другие вопросы во время приема.
Чего ожидать от врача
Ваш врач, скорее всего, задаст вам ряд вопросов. Готовность ответить на них может дать время, чтобы обсудить те моменты, на которые вы хотите потратить больше времени. Вас могут спросить:
- Когда у вас впервые появились симптомы? Насколько они серьезны, являются ли они постоянными или случайными?
- Кажется, что-нибудь улучшает или ухудшает ваши симптомы?
- Как твой аппетит? Вы недавно похудели без всяких попыток?
- Были ли у вас отеки на ногах?
- Испытывали ли вы одышку?
- Можете ли вы работать и выполнять обычные повседневные задачи? Вы часто устаете?
- Вы заметили, что у вас легко появляются синяки?
- У кого-нибудь из вашей семьи когда-либо диагностировали амилоидоз?
Лечение амилоидоза в клинике Мэйо
14 марта 2020 г.
Показать ссылки- Goldman L, et al., ред. Амилоидоз. В: Медицина Гольдмана-Сесила. 26-е изд. Эльзевир; 2020. https://www.clinicalkey.com. По состоянию на 1 октября 2019 г.
- Hoffman R, et al. Амилоидоз легкой цепи иммуноглобулина (первичный амилоидоз). В кн .: Гематология: основные принципы и практика. 7-е изд. Эльзевир; 2018. https://www.clinicalkey.com. По состоянию на 1 октября 2019 г.
- Амилоидоз. Руководство Merck Professional Version. https://www.merckmanuals.com/professional/endocrine-and-metabolic-disorders/amyloidosis/amyloidosis?query=amyloidosis.По состоянию на 1 октября 2019 г.
- Ferri FF. Амилоидоз. В: Клинический советник Ферри 2020. Elsevier; 2020. https://www.clinicalkey.com. По состоянию на 1 октября 2019 г.
- Gorevic PD. Обзор амилоидоза. https://www.uptodate.com/contents/search. По состоянию на 1 октября 2019 г.
- AskMayoExpert. Сердечный амилоидоз. Клиника Майо; 2018.
- Fontana M, et al. Амилоидоз миокарда: типичное интерстициальное заболевание. Журнал Американского колледжа кардиологии: сердечно-сосудистые изображения.2019. doi: 10.1016 / j.jcmg.2019.06.023.
- AskMayoExpert. Амилоидоз почек. Клиника Майо; 2019.
- Feehally J, et al. Амилоидоз почек и заболевания клубочков с отложением моноклональных иммуноглобулинов. В кн .: Комплексная клиническая нефрология. 6-е изд. Эльзевир. 2019. https://www.clinicalkey.com. По состоянию на 1 октября 2019 г.
- Morrow ES Jr. Allscripts EPSi. Клиника Майо. 1 ноября 2019 г.
- Пруты РК (заключение эксперта). Клиника Майо. 13 января 2020 г.
Связанные
Продукты и услуги
Показать больше продуктов и услуг Mayo ClinicАмилоидоз: варианты лечения | Рак.Net
НА ЭТОЙ СТРАНИЦЕ : Вы узнаете о различных методах, которые врачи используют для лечения людей с этим заболеванием. Для просмотра других страниц используйте меню.
Часто наиболее эффективным лечением амилоидоза является лечение и контроль основного заболевания, если оно есть.
В этом разделе описаны стандартные методы лечения амилоидоза. «Стандарт лечения» означает лучшие известные методы лечения. При принятии решения о плане лечения пациентам также рекомендуется рассмотреть возможность проведения клинических испытаний.Клиническое испытание — это научное исследование, в котором проверяется новый подход к лечению. Врачи хотят узнать, безопасно ли это, эффективно и, возможно, лучше, чем стандартное лечение. В клинических испытаниях можно проверить новое лекарство, новую комбинацию стандартных методов лечения или новые дозы стандартных лекарств или других методов лечения. Ваш врач может помочь вам рассмотреть все варианты лечения. Чтобы узнать больше о клинических испытаниях, см. Разделы «О клинических испытаниях» и «Последние исследования».
Обзор лечения
Врачи разных типов часто работают вместе, чтобы составить общий план лечения пациента, который сочетает в себе разные виды лечения.Это особенно важно, потому что амилоидоз поражает очень много разных органов. Это называется мультидисциплинарной командой.
В состав лечебной бригады часто входят следующие специалисты:
Врач-гематолог. Врач, специализирующийся на заболеваниях крови
Кардиолог. Врач, лечащий сердечные заболевания
Гастроэнтеролог. Врач, специализирующийся на заболеваниях желудочно-кишечного тракта
Пульмонолог. Врач, специализирующийся на заболеваниях легких
Нефролог. Врач, который лечит проблемы с почками
Невролог. Врач, специализирующийся на проблемах, связанных с мозгом и нервной системой
Часто гематолог берет на себя ведущую роль в координации этой многопрофильной команды. Бригады здравоохранения также могут включать в себя множество других специалистов в области здравоохранения, в том числе помощников врачей, медсестер, социальных работников, фармацевтов, консультантов, диетологов и других.
Описание наиболее распространенных вариантов лечения амилоидоза приведено ниже. Варианты лечения и рекомендации зависят от нескольких факторов, включая тип амилоидоза, тип основного заболевания, возможные побочные эффекты, а также предпочтения пациента и общее состояние здоровья. Ваш план ухода также будет включать лечение симптомов и побочных эффектов. Найдите время, чтобы узнать обо всех вариантах лечения, и обязательно задавайте вопросы о том, что неясно. Кроме того, поговорите со своим врачом о целях каждого лечения и о том, чего вы можете ожидать от лечения.Узнайте больше о принятии решений о лечении.
Лекарства, применяемые для лечения амилоидоза
Лекарство можно использовать для контроля проблем, связанных с амилоидозом. Доказано, что стероиды работают хорошо, и их обычно комбинируют с другими лекарствами.
Химиотерапия
Химиотерапия — это использование лекарств для уничтожения аномальных клеток, обычно путем прекращения способности клеток расти и делиться. Чаще всего используется для лечения рака. Однако химиотерапия также полезна при других состояниях, включая амилоидоз.Химиотерапию может назначить гематолог или онколог, врач, специализирующийся на химиотерапии для лечения рака.
Во время лечения амилоидоза химиотерапия используется для разрушения аномальных клеток в крови. Обычные способы проведения химиотерапии включают внутривенный (IV) зонд, вводимый в вену с помощью иглы, укол под кожу или таблетку или капсулу, которые проглатываются (перорально).
Схема (расписание) химиотерапии обычно состоит из определенного количества циклов, проводимых в течение определенного периода времени.Пациент может получать по 1 лекарству за раз или комбинации разных лекарств одновременно.
Некоторые из распространенных типов химиотерапии, используемых для лечения амилоидоза, — это циклофосфамид (Cytoxan, Neosar) и мелфалан (Alkeran) в сочетании с дексаметазоном (несколько торговых марок) и преднизоном (несколько торговых марок).
Побочные эффекты химиотерапии
Побочные эффекты химиотерапии зависят от человека и применяемой дозы, но могут включать тошноту, рвоту и утомляемость.Как правило, они поддаются лечению, когда они возникают, и обычно проходят после завершения лечения. Некоторые виды химиотерапии могут вызывать необычные долгосрочные побочные эффекты, включая повреждение костного мозга и других органов.
Анемия часто встречается у людей с амилоидозом, особенно у тех, кто получает химиотерапию, например мелфалан. Анемия — это аномально низкий уровень эритроцитов (эритроцитов). В эритроцитах есть железосодержащий белок, называемый гемоглобином, который переносит кислород во все части тела.Если уровень эритроцитов слишком низкий, части тела не получают достаточно кислорода и не могут работать должным образом. Большинство людей с анемией чувствуют усталость или слабость.
Узнайте больше об основах химиотерапии и подготовке к лечению. Лекарства, используемые для лечения болезней, постоянно проходят оценку. Зачастую лучший способ узнать о прописанных вам лекарствах, их назначении и их потенциальных побочных эффектах или взаимодействии с другими лекарствами — поговорить с врачом. Узнайте больше о своих рецептах с помощью доступных для поиска баз данных о лекарствах.
Таргетная терапия
Таргетная терапия — это лечение, направленное на определенные гены, белки или тканевую среду, которая способствует развитию амилоидоза. Этот тип лечения блокирует рост и распространение аномальных клеток, ограничивая повреждение здоровых клеток.
Недавние исследования показывают, что не все отклонения имеют одни и те же цели. Чтобы найти наиболее эффективное лечение, ваш врач может провести тесты для выявления генов, белков и других факторов. Это помогает врачам лучше подбирать каждому пациенту наиболее эффективное лечение, когда это возможно.Кроме того, сейчас проводится множество научных исследований, чтобы узнать больше о конкретных молекулярных мишенях и новых методах лечения, направленных на них. Узнайте больше об основах целевого лечения.
Таргетная терапия амилоидоза включает терапию против ангиогенеза, моноклональные антитела и ингибиторы протеасом.
Иммуномодулирующие препараты. Лекарства этого класса включают леналидомид (Ревлимид), помалидомид (Помалист) и талидомид (Синовир, Таломид).
Моноклональные антитела. Моноклональные антитела — это тип таргетной терапии. Он распознает и прикрепляется к определенному белку в аномальных клетках и не влияет на клетки, в которых этого белка нет. К препаратам этого класса относятся даратумумаб (Дарзалекс) и элотузумаб (Эмплицит). Второй тип моноклональных антител напрямую нацелен на сам амилоид. В настоящее время несколько таких антител проходят клинические испытания.
Ингибиторы протеасом. Ингибирование протеасом — это тип таргетной терапии. Препараты этого класса нацелены на определенные ферменты, называемые протеасомами, которые переваривают белки в клетках. Этот класс включает бортезомиб (Велкейд), иксазомиб (Нинларо) и карфилзомиб (Кипролис).
Исследователи продолжают изучать эти препараты, чтобы выяснить, насколько хорошо каждый из них лечит амилоидоз. Эти препараты не отменяют накопление амилоидных белков в тканях или органах. Однако исследования комбинации бортезомиба, дексаметазона и мелфалана показали, что они могут помочь органам, пораженным амилоидозом, работать лучше.
Недавние исследования начали изучать роль методов лечения, которые могут улучшить функцию органов, непосредственно воздействуя на отложения амилоида. Этот вид лечения все еще изучается в клинических испытаниях.
Побочные эффекты таргетной терапии
Таргетная терапия может вызывать побочные эффекты, отличные от тех, которые обычно связаны с химиотерапией. У пациентов, получающих таргетную терапию, могут развиться проблемы с кожей, волосами, ногтями и / или глазами. Узнайте больше о кожных реакциях на таргетную терапию.
Хирургия
Хирургическое лечение амилоидоза может включать трансплантацию органов. Трансплантация печени оказалась эффективной при лечении некоторых типов наследственного амилоидоза. Также может помочь трансплантация почек и сердца. Однако трансплантация органов может не подходить для всех пациентов, особенно для тех, у кого имеется большое количество амилоидных белков, отложившихся в их органах. Поговорите со своим врачом или в центре, специализирующемся на трансплантации органов, о возможных вариантах.
Трансплантация стволовых клеток / трансплантация костного мозга
Трансплантация костного мозга / стволовых клеток — это медицинская процедура, при которой плазматические клетки костного мозга, производящие амилоидный белок, сначала разрушаются высокими дозами химиотерапии, а затем заменяются высокоспециализированными клетками, называемыми гемопоэтическими стволовыми клетками, которые превращаются в здоровые Костный мозг. Гемопоэтические стволовые клетки — это кроветворные клетки, обнаруживаемые как в кровотоке, так и в костном мозге. Сегодня эту процедуру чаще называют трансплантацией стволовых клеток периферической крови, а не трансплантацией костного мозга, потому что обычно пересаживаются стволовые клетки, собранные из кровотока, а не сама ткань костного мозга.
Для некоторых людей с амилоидозом, у которых есть нормальные функции органов, может быть полезна трансплантация стволовых клеток периферической крови. Во время этой процедуры пациенту вводят высокие дозы химиотерапии для разрушения клеток крови, вырабатывающих амилоидные белки. Затем пациент получает здоровые стволовые клетки периферической крови, которые позволяют организму снова начать производить здоровые клетки крови. Выживаемость можно значительно улучшить с помощью высокодозной химиотерапии и трансплантации стволовых клеток периферической крови.Однако многие пациенты не могут получить это лечение, потому что накопление амилоидного белка повлияло на функцию других органов.
Прежде чем рекомендовать трансплантацию стволовых клеток, врачи обсудят с пациентом риски этого лечения и рассмотрят несколько других факторов, таких как тип заболевания, результаты любого предыдущего лечения, а также возраст пациента и общее состояние здоровья.
Узнайте больше об основах трансплантации стволовых клеток и костного мозга.
Помощь при симптомах и побочных эффектах
Амилоидоз и его лечение часто вызывают побочные эффекты.Облегчение симптомов и побочных эффектов у человека — важная часть лечения. Этот подход называется паллиативным или поддерживающим уходом и включает в себя поддержку пациента с его физическими, эмоциональными и социальными потребностями.
Паллиативная помощь — это любое лечение, направленное на уменьшение симптомов, улучшение качества жизни и поддержку пациентов и их семей. Любой человек, независимо от возраста или заболевания, может получить паллиативную помощь. Лучше всего это работает, когда паллиативную помощь начинают как можно раньше.
Люди часто получают лечение от амилоидоза и одновременно лечение, облегчающее побочные эффекты. Фактически, пациенты, которые получают и то, и другое, часто имеют менее серьезные симптомы, лучшее качество жизни и сообщают, что они более удовлетворены лечением.
Паллиативные методы лечения широко различаются и часто включают медикаменты, диетическую терапию (см. Выше), методы релаксации, эмоциональную поддержку и другие методы лечения. Вы также можете получить паллиативное лечение, подобное тому, которое предназначено для устранения болезни, например химиотерапию.Поговорите со своим врачом о целях каждого лечения в вашем плане лечения.
Перед началом лечения поговорите со своим лечащим врачом о возможных побочных эффектах вашего конкретного плана лечения и вариантах паллиативной помощи. Во время и после лечения обязательно сообщите своему врачу или другому члену медицинской бригады, если у вас возникла проблема, чтобы ее можно было решить как можно быстрее. Узнайте больше о паллиативной помощи.
Если лечение не удалось
Излечение от амилоидоза не всегда возможно.Если болезнь не поддается лечению или контролю, ее можно назвать запущенной или терминальной.
Этот диагноз вызывает стресс, и многим людям трудно обсуждать запущенную болезнь. Однако важно вести открытые и честные беседы со своим врачом и медицинским персоналом, чтобы выразить свои чувства, предпочтения и опасения. Медицинская бригада всегда готова помочь, и многие члены команды обладают особыми навыками, опытом и знаниями, чтобы поддерживать пациентов и их семьи. Чрезвычайно важно убедиться, что человеку физически комфортно и он не испытывает боли.
Пациенты с запущенным заболеванием и ожидаемая продолжительность жизни менее 6 месяцев могут пожелать рассмотреть вариант паллиативной помощи, называемой хосписной помощью. Уход в хосписе призван обеспечить максимально возможное качество жизни людям, находящимся на грани конца жизни. Вам и вашей семье рекомендуется подумать о том, где вам будет наиболее комфортно: дома, в больнице или в хосписе. Медсестринский уход и специальное оборудование могут сделать пребывание дома реальной альтернативой для многих семей.Узнайте больше о расширенном планировании ухода.
После смерти любимого человека многим людям нужна поддержка, чтобы помочь им справиться с утратой. Узнайте больше о горе и утрате.
Следующий раздел в этом руководстве — О клинических испытаниях . Он предлагает больше информации об исследованиях, направленных на поиск лучших способов ухода за людьми с амилоидозом. Или используйте меню, чтобы выбрать другой раздел, чтобы продолжить чтение этого руководства.
Причины, типы, симптомы, диагностика, лечение и прогноз
Амилоидоз — это когда аномальный белок, называемый амилоидом, накапливается в ваших тканях и органах.Когда это происходит, это влияет на их форму и то, как они работают. Амилоидоз — серьезная проблема для здоровья, которая может привести к опасной для жизни органной недостаточности.
Причины и типы амилоидоза
Многие различные белки могут приводить к отложению амилоида, но лишь некоторые из них связаны с серьезными проблемами со здоровьем. Тип белка и место его скопления говорят о типе амилоидоза. Амилоидные отложения могут накапливаться по всему телу или только в одной области.
Различные типы амилоидоза включают:
AL амилоидоз (амилоидоз легкой цепи иммуноглобулина). Это наиболее распространенный тип, который раньше назывался первичным амилоидозом. AL означает «легкие амилоидные цепи», тип белка, ответственного за это состояние. Причины неизвестны, но это случается, когда костный мозг вырабатывает аномальные антитела, которые невозможно расщепить. Это связано с раком крови, называемым множественной миеломой. Это может повлиять на ваши почки, сердце, печень, кишечник и нервы.
Продолжение
АА амилоидоз. Ранее известное как вторичный амилоидоз, это состояние является результатом другого хронического инфекционного или воспалительного заболевания, такого как ревматоидный артрит, болезнь Крона или язвенный колит.В основном это влияет на ваши почки, но также может повлиять на пищеварительный тракт, печень и сердце. AA означает, что белок амилоидного типа A вызывает этот тип.
Амилоидоз, связанный с диализом (DRA). Это чаще встречается у пожилых людей и людей, находящихся на диализе более 5 лет. Эта форма амилоидоза вызвана отложениями бета-2-микроглобулина, которые накапливаются в крови. Отложения могут накапливаться во многих различных тканях, но чаще всего поражают кости, суставы и сухожилия.
Семейный или наследственный амилоидоз. Это редкая форма, передающаяся от семьи. Часто поражает печень, нервы, сердце и почки. Многие генетические дефекты связаны с более высокой вероятностью амилоидного заболевания. Например, причиной может быть аномальный белок, такой как транстиретин (TTR).
Возрастной (старческий) системный амилоидоз. Это вызвано отложениями нормального TTR в сердце и других тканях. Чаще всего это происходит у пожилых мужчин.
Органоспецифический амилоидоз. Это вызывает отложения амилоидного белка в отдельных органах, включая кожу (кожный амилоидоз).
Хотя некоторые типы отложений амилоида были связаны с болезнью Альцгеймера, мозг редко поражается амилоидозом, который происходит по всему телу.
Факторы риска амилоидоза
Мужчины заболевают амилоидозом чаще, чем женщины. Риск амилоидоза повышается с возрастом. Амилоидоз поражает 15% пациентов с формой рака, называемой множественной миеломой.
Амилоидоз также может развиться у людей с терминальной стадией заболевания почек, которые длительное время находятся на диализе (см. «Амилоидоз, связанный с диализом» выше).
Симптомы амилоидоза
Симптомы амилоидоза часто незаметны. Они также могут сильно различаться в зависимости от того, где в организме накапливается амилоидный белок. Важно отметить, что описанные ниже симптомы могут быть вызваны различными проблемами со здоровьем. Только ваш врач может поставить диагноз амилоидоза.
Общие симптомы амилоидоза могут включать:
- Изменение цвета кожи
- Сильная усталость
- Чувство полноты
- Боль в суставах
- Низкое количество эритроцитов (анемия)
- Одышка
- Отек языка
- Покалывание и онемение в ногах и стопах
- Слабый хват
- Сильная слабость
- Внезапная потеря веса
Сердечный (сердечный) амилоидоз
Отложения амилоида в сердце могут сделать стенки сердечной мышцы жесткими.Они также могут ослабить сердечную мышцу и повлиять на электрический ритм сердца. Это состояние может привести к уменьшению притока крови к сердцу. В конце концов, ваше сердце больше не сможет нормально перекачивать кровь. Если амилоидоз поражает ваше сердце, у вас может быть:
- Одышка с легкой активностью
- Нерегулярное сердцебиение
- Признаки сердечной недостаточности, включая отек стоп и лодыжек, слабость, усталость и тошноту, среди прочего
Амилоидоз почек (почек)
Почки фильтруют отходы и токсины из крови.Амилоидные отложения в почках мешают им выполнять эту работу. Когда ваши почки не работают должным образом, в вашем теле накапливаются вода и опасные токсины. Если амилоидоз поражает почки, у вас могут быть:
- Признаки почечной недостаточности, включая отек стоп и лодыжек и отечность вокруг глаз
- Высокий уровень белка в моче
Желудочно-кишечный амилоидоз
Амилоидные отложения вдоль вашего тела. Желудочно-кишечный тракт замедляет движение пищи через кишечник.Это мешает пищеварению. Если амилоидоз поражает ваш желудочно-кишечный тракт, у вас может быть:
- Снижение аппетита
- Диарея
- Тошнота
- Боль в желудке
- Снижение веса
Если ваша печень поражена, это может вызвать ее увеличение и скопление жидкости в организме .
Амилоидная нейропатия
Отложения амилоида могут повредить нервы вне головного и спинного мозга, которые называются периферическими нервами. Периферические нервы несут информацию между головным и спинным мозгом и остальным телом.Например, они заставляют ваш мозг воспринимать боль, если вы обожжете руку или ударите пальцы ног. Если амилоидоз поражает нервы, у вас могут быть:
- Проблемы с равновесием
- Проблемы с контролем мочевого пузыря и кишечника
- Проблемы с потоотделением
- Покалывание и слабость
- Головокружение при стоянии из-за нарушения способности вашего тела контролировать кровяное давление
Диагностика амилоидоза
Тщательное медицинское обследование и подробное и точное описание вашей истории болезни имеют решающее значение для того, чтобы помочь вашему врачу диагностировать амилоидоз.
Анализы крови и мочи могут выявить аномальные белки. В зависимости от ваших симптомов врач может также проверить вашу щитовидную железу и печень.
Ваш врач проведет биопсию, чтобы подтвердить диагноз амилоидоза и узнать, какой у вас конкретный тип белка. Образец ткани для биопсии может быть взят из жира на животе (брюшной жировой подушечки), костного мозга или иногда изо рта, прямой кишки или других органов. Не всегда необходимо проводить биопсию части тела, поврежденной амилоидными отложениями.
Также могут помочь визуализирующие тесты. Они показывают степень повреждения таких органов, как сердце, печень или селезенка.
Ваш врач проведет генетический тест, если он сочтет, что у вас тип, передающийся от семьи. Лечение наследственного амилоидоза отличается от лечения других типов заболевания.
После постановки диагноза врач может проверить ваше сердце с помощью эхокардиограммы или вашу печень и селезенку с помощью визуализационных тестов.
Лечение амилоидоза
Лекарства от амилоидоза нет.Ваш врач назначит лечение, чтобы замедлить выработку амилоидного белка и справиться с вашими симптомами. Если амилоидоз связан с другим заболеванием, лечение будет включать в себя лечение этого основного состояния.
Конкретное лечение зависит от типа амилоидоза и количества пораженных органов.
- Высокодозная химиотерапия с трансплантацией стволовых клеток может помочь удалить вещество, которое приводит к образованию амилоида у некоторых людей с первичным амилоидозом AL.Только химиотерапевтические препараты могут использоваться для лечения других пациентов с первичным амилоидозом AL.
- Вторичный амилоидоз (AA) лечится путем контролирования основного заболевания и с помощью мощных противовоспалительных препаратов, называемых стероидами, которые борются с воспалением.
- Пересадка печени может помочь в лечении этого заболевания, если у вас есть определенные типы наследственного амилоидоза.
- Новые методы лечения могут замедлить выработку аномального белка TTR.
- Ваш врач может также порекомендовать пересадку почки.
Другие методы лечения симптомов включают:
- Мочегонные препараты для удаления лишней воды из вашего тела
- Загустители для добавления в жидкости, чтобы предотвратить удушье, если у вас есть проблемы с глотанием
- Компрессионные чулки для снятия отеков в ногах или ступнях
- Изменения в том, что вы едите, особенно если у вас желудочно-кишечный амилоидоз
Чего ожидать
Амилоидоз может быть смертельным, особенно если он поражает ваше сердце или почки.Ранняя диагностика и лечение важны и могут помочь улучшить выживаемость.
Исследователи продолжают задаваться вопросом, почему некоторые типы амилоида вызывают у людей заболевание и как можно остановить образование амилоида. Исследования по поиску новых методов лечения продолжаются. Если у вас амилоидоз, подумайте о том, чтобы спросить своего врача, есть ли какие-либо клинические испытания, к которым вы можете присоединиться, или найдите их, посетив www.clinicaltrials.gov и введя поисковый запрос «амилоидоз».
Лечение — многопрофильная программа по амилоидозу
Лечение амилоидоза направлено на устранение симптомов, ограничение выработки амилоидных белков и / или поддержку дисфункции пораженных органов.При отсутствии лечения прогноз для амилоидоза плохой. Поэтому врачи NYP уделяют первоочередное внимание своевременному вмешательству до того, как несколько органов серьезно пострадают.
К каждому пациенту применяется индивидуальный подход, и лечение зависит от количества пораженных органов, физиологического возраста пациента и уровня его / ее активности. Если у пациента диагностирован первичный (AL) амилоидоз, обычно врачи назначают режим на основе химиотерапии (аналогичный тому, который используется для лечения множественной миеломы), чтобы разрушить аномальные плазматические клетки, которые производят предшественники амилоидного белка.Новый класс препаратов, называемых ингибиторами протеасом, обычно используется в различных комбинациях с другими препаратами для лечения амилоидоза AL.
Помимо лечения по схемам на основе химиотерапии, исследователи NYP занимаются изучением новых методов лечения амилоидоза, включая лекарства, которые используются для лечения множественной миеломы. Кроме того, некоторым пациентам может быть назначена трансплантация стволовых клеток. Поскольку амилоидоз является прогрессирующим заболеванием, врачи NYP немедленно предложат подходящему пациенту трансплантат.Если пациент с амилоидозом соответствует критериям отбора и находится в хорошем состоянии (например, <3 пораженных органов, хорошая сердечная функция и хорошие лабораторные критерии), специалист по трансплантации костного мозга в NYP может собрать стволовые клетки и провести трансплантацию. Если у пациента более запущенное заболевание, команда NYP предварительно обработает пациента курсом химиотерапии, чтобы снизить уровень амилоидоза, а затем выполнит трансплантацию стволовых клеток. Специалисты по пересадке костного мозга из NYP сочли эту процедуру очень многообещающей для пациентов с амилоидозом.
Сердечный амилоидоз
При аномальном накоплении амилоидного белка в сердце пациенты могут испытывать такие симптомы, как одышка, головокружение и отек. Накопление амилоидного белка в сердце снижает способность сердца к наполнению и может привести к повреждению электрической системы сердца. Если не лечить, сердечный амилоидоз может привести к сердечной недостаточности. Поэтому врачи в NYP уделяют первоочередное внимание вмешательству на ранней стадии до того, как будет затронут этот основной орган.
Врачи NYP обычно начинают с медицинского осмотра, за которым следуют анализы крови и мочи и электрокардиограмма. Далее проводится эхокардиограмма. Если анализы согласуются и есть подозрение на амилоидоз сердца, окончательный диагноз может быть подтвержден биопсией сердца. Процедура безопасна, если проводится в опытном учреждении. Врачи NYP обладают значительным опытом выполнения эндомиокардиальной биопсии, потому что NYP имеет одну из крупнейших программ по сердечной недостаточности и трансплантации в стране, и они обычно выполняют более 20 биопсий сердца в неделю.
Недавно исследователи из NYP успешно использовали магнитно-резонансную томографию сердца (CMRI) — менее инвазивный метод — для точной диагностики сердечного амилоидоза. Врачи NYP также разработали новую технику сканирования с использованием пирофосфата технеция, которая может точно различать две наиболее распространенные формы сердечного амилоидоза — AL и ATTR.
Если у пациента есть подтвержденный диагноз амилоид в сердце, следующим шагом врачей NYP является определение типа сердечного амилоидоза — первичный (AL) или наследственный (ATTR).Около половины пациентов, поступающих в NYP с амилоидом в сердце, имеют AL, а другая половина — амилоидоз ATTR. Наиболее распространенной формой сердечного ATTR является амилоидоз сердца дикого типа или старческий амилоидоз. Кардиологи NYP сотрудничают с гематологами-онкологами, чтобы разработать лучший курс лечения для пациентов с сердечным амилоидозом.
Типичное лечение первичного сердечного амилоидоза включает химиотерапию для ограничения накопления белка в сердце, а также диуретики и антикоагулянты среди других методов лечения.По мере того как население продолжает стареть, TTR становится все более обычным явлением. Врачи NYP активно участвуют в исследованиях, направленных на пациентов с амилоидом TTR.
Амилоидоз почек
Амилоидный белок может откладываться в почках и приводить к дисфункции органов. Пациенты могут испытывать такие симптомы, как пенистая моча или отек ног. Врачи NYP проведут простой анализ мочи, чтобы оценить наличие амилоидного белка в моче. Иногда для подтверждения диагноза может потребоваться биопсия почки.
Как правило, лечащий нефролог в NYP будет сотрудничать с гематологом-онкологом, чтобы сначала вылечить потенциально лежащую в основе дискразию плазматических клеток. Если лечение эффективно ограничивает дальнейшее производство амилоида, функция почек может стабилизироваться и даже улучшиться. Затем нефролог может лечить любые сохраняющиеся симптомы амилоида почек, такие как задержка жидкости.
Амилоидоз почек мешает почкам правильно выводить отходы из организма, и, если его не лечить, может привести к почечной недостаточности.Поэтому врачи NYP уделяют первоочередное внимание своевременному вмешательству до того, как почки серьезно пострадают. Как только амилоид находится под контролем, подходящим пациентам также доступна трансплантация почки и костного мозга.
NORD (Национальная организация по редким заболеваниям)
УЧЕБНИКИ
Beers MH, Berkow R., eds. Руководство Merck, 17-е изд. Станция Уайтхаус, Нью-Джерси: Исследовательские лаборатории Мерк; 1999: 219-220.
Берков Р., изд. Руководство Merck для дома. Станция Уайтхаус, Нью-Джерси: Исследовательские лаборатории Мерк; 1997: 690-91.
Бенсон Мэриленд. Амилоидоз. В: Scriver CR, et al., Eds. Метаболические и молекулярные основы наследственного заболевания. 7-е изд. Нью-Йорк, штат Нью-Йорк; McGraw-Hill Companies, Inc; 1995: 4159-91.
Каткарт ES. Амилоидоз. В: Kelley WN, et al., Eds. Учебник ревматологии. 4-е изд. Филадельфия, Пенсильвания: W.B. Компания Сондерс; 1993: 1413-28.
СТАТЬИ ЖУРНАЛА
Стоппини М., Беллотти В. Системный амилоидоз: уроки B2-микроглобулина. J Biol Chem. 2015; 290: 9951-9958.
Герц М.А., Бенсон М.Д., Дайк П.Дж. и др.Диагностика, прогноз и терапия транстиретинового амилоидоза. J Am Coll Cardiol. 2015; 66: 2451-2466.
Махмуд С., Палладини Дж., Санчоравала В., Вечалекар А. Последние сведения о лечении амилоидоза легких цепей. Haematologica. 2014; 99: 209-221.
Falk RH, Dubrey SW. Амилоидный порок сердца. Прогресс сердечно-сосудистых заболеваний. 2010; 52: 347-361.
Comenzo RL. Как я лечу амилоидоз. Blood 2009; 114: 3147-57
Palladini G, Merlini G. Текущее лечение амилоидоза AL.Haematologica 2009; 94: 1044-1048.
Дембер Л. Заболевание почек, связанное с амилоидозом. Варенье. Soc. Нефрол. 2006; 17: 3458-3471.
Герц MA, Lacy MQ, Dispenzieri A, Hayman SR. Амилоидоз. Передовая практика и исследования в области клинической гематологии. 2005; 18 (4): 709-727.
Бенсон М. Наследственные амилоидозы. Передовая практика и исследования в клинической ревматологии. 2003; 17: 909-927.
Park KI, Ourednik J, Ourednik V и др. Глобальные стратегии замены генов и клеток с помощью стволовых клеток.Gene Ther. 2002; 9: 613-24.
Рокен С., Шекспир А. Патология, диагностика и патогенез амилоидоза АА. Арка Вирхова. 2002; 440: 111-22.
Гринберг С.М. Церебральная амилоидная ангиопатия и дисфункция сосудов. Cerebrovasc Dis. 2002; 13 (приложение 2): 42-47.
Герц М.А., Лейси М.К., Диспензиери А. Амилоидоз легкой цепи иммуноглобулина и почки. Kidney Int. 2002; 61: 1-9.
Jaikaran ET, Clark A. Islet амилоид и диабет 2 типа; от молекулярного неправильного свертывания к патофизиологии островков.Biochim Biophys Acta. 2001; 1537: 179-203.
Санчоравала V, Райт Д.Г., Селдин округ Колумбия и др. Обзор использования высоких доз мелфалана с трансплантацией аутологичных стволовых клеток для лечения амилоидоза AL. Пересадка костного мозга. 2001; 28: 637-42.
Скиннер М., Санчоравала В., Селдин, округ Колумбия, Дембер Л.М., Фальк Р.Х., Берк Д.Л., Андерсон Дж.Дж., О’Хара С.Дж., Финн К.Т., Либби, Калифорния, Висман Дж., Квиллен К., Свон Н., Райт Д.Г.: Мелфалан в высоких дозах. и трансплантация аутологичных стволовых клеток пациентам с амилоидозом AL: 8-летнее исследование.Анналы Int Med, 2004; 140: 85-93.
Селдин Д.К., Андерсон Дж., Санчоравала В., Малек К., Райт Д. Г., Квиллен К., Финн К. Т., Берк Дж. Л., Дембер Л. М., Фальк Р. Х., Скиннер М.: Улучшение качества жизни пациентов с амилоидозом AL, получавших высокие дозы мелфалана и трансплантация аутологичных стволовых клеток. Кровь, 2004; 104: 1888-1893.
Хан MF, Falk RH. Амилоидоз. Postgrad Med J. 2001; 77: 686-93.
Добсон СМ. Сворачивание белка и его связь с болезнями человека. Biochem Soc Sympos. 2001; 68: 1-26.
Адамс Д. Наследственные и приобретенные амилоидные невропатии. J Neurol. 2001; 248: 647-57.
Сараива MJ. Транстиретиновый амилоидоз: рассказ о слабых взаимодействиях. FEBS Lett. 2001; 498: 201-203.
Floege J, Schaffer J, Koch KM. Сцинтиграфические методы выявления амилоидоза, связанного с бета2-микроглобулином (амилоидоз Abeta2-микроглобулина). Пересадка нефрола Dial. 2001; 16 (приложение 4): 12-16.
Walker LC, LeVine H. Церебральные протеопатии: нейродегенеративные нарушения конформации и сборки белков.Mol Neurobiol. 2000; 21: 83-95.
Эль-Шанти HE. Семейная средиземноморская лихорадка. Саудовская медицина, 2001; 22: 104-9.
Cunnane G. Предшественники амилоида и амилоидоз при воспалительном артрите. Curr Opin Rheumatol. 2001; 13: 67-73.
Plante-Bordeneuve V, Said G. Транстиретиновая родственная знакомая амилоидная полинейропатия. Curr Opin Neurol. 2000; 13: 569-73.
Герц М.А., Коменцо Р., Фальк Р.Х. и др. Определение вовлечения органов и ответа на лечение при амилоидозе легкой цепи иммуноглобулина (AL): согласованное мнение 10-го Международного симпозиума по амилоиду и амилоидозу.Являюсь. J. Hematol. 2005; 79: 319-328.
ИНТЕРНЕТ
ИНФОРМАЦИЯ О амилоидозе: для пациентов и их сети поддержки, включая врачей, медсестер и студентов-медиков. Группы поддержки амилоидоза. Октябрь 2013 г. http://www.amyloidosissupport.com/AmyloidAware_Booklet.pdf По состоянию на 24 октября 2018 г.
Basu A, Bogdan CA, Matute R. Бета-2m амилоидоз, связанный с диализом. Medscape. Обновлено: 3 февраля 2017 г. Доступно по адресу: http://emedicine.medscape.com/article/246542-overview Проверено 24 октября 2018 г.
Что такое амилоидоз? Программа лечения и исследования амилоидов Бостонского университета. http://www.bu.edu/amyloid/about/what/ По состоянию на 24 октября 2018 г.
Amyloidosis. Фонд Мэйо медицинского образования и исследований. 7 июля 2017 г. http://www.mayoclinic.com/health/amyloidosis/DS00431 По состоянию на 24 октября 2018 г.
Амилоидоз — NHS
Амилоидоз — это группа редких серьезных заболеваний, вызванных накоплением аномального белка, называемого амилоидом, в органах и тканях по всему телу.
Накопление амилоидных белков (отложений) может затруднить правильную работу органов и тканей. Без лечения это может привести к органной недостаточности.
Эта страница посвящена амилоидозу AL, который является наиболее распространенным типом, и амилоидозу ATTR, который часто передается в семье.
Для получения информации о других типах амилоидоза посетите сайт информации для пациентов Национального центра амилоидоза UCL.
Симптомы амилоидоза AL
Симптомы амилоидоза AL зависят от пораженных тканей и органов.
Почечная недостаточность
У большинства людей с амилоидозом AL накапливается амилоидный белок в почках, и они подвержены риску почечной недостаточности.
Симптомы почечной недостаточности включают:
- отек, часто в ногах, вызванный задержкой жидкости (отек)
- усталость
- слабость
- потеря аппетита
Сердечная недостаточность
Отложения амилоида в сердце могут заставляют мышцы становиться жестче, что затрудняет перекачивание крови по телу.Это может привести к сердечной недостаточности, которая может вызвать:
Другие симптомы
Амилоидные белки также могут накапливаться в других областях, таких как печень, селезенка, нервы или пищеварительная система. Симптомы могут включать:
AL амилоидоз не влияет на мозг, поэтому он не вызывает, например, проблем с памятью или мышлением.
Обратитесь к терапевту, если у вас есть какие-либо из вышеперечисленных симптомов и вы беспокоитесь. Врач общей практики может назначить лечение, чтобы помочь с этими симптомами.
В некоторых случаях амилоидоз AL может быть связан с типом рака кости, называемым множественной миеломой.
Благотворительная организация Myeloma UK предоставляет дополнительную информацию о множественной миеломе и ее связи с амилоидозом AL.
Причина амилоидоза AL
Амилоидоз AL вызывается аномалией в определенных клетках костного мозга, называемых плазматическими клетками.
Аномальные плазматические клетки продуцируют аномальные формы белков легкой цепи, которые попадают в кровоток и могут образовывать амилоидные отложения.
У здоровых людей в крови нормальные белки легкой цепи, которые являются частью их естественных белков антител.Они помогают защитить организм от инфекции.
Аномальные легкие цепи у пациентов с амилоидозом AL собираются вместе в нитевидные нити (амилоидные фибриллы), от которых организм не может легко избавиться.
Со временем амилоидные фибриллы накапливаются в виде отложений амилоида AL в тканях и органах. Это постепенно останавливает их нормальное функционирование, вызывая многие симптомы амилоидоза AL.
В отличие от некоторых других типов амилоидоза, амилоидоз AL не передается по наследству, поэтому человек с этим заболеванием не может передать его своим детям.
Лечение амилоидоза AL
В настоящее время лекарства от амилоидоза не существует. Амилоидные отложения нельзя удалить напрямую.
Но есть методы лечения, которые останавливают производство аномальных белков и помогают избавиться от симптомов.
Эти процедуры могут дать вашему организму время постепенно очистить отложения, прежде чем они снова начнут накапливаться. Это может помочь предотвратить повреждение органов.
В большинстве случаев лечение будет включать химиотерапию.Химиотерапия повреждает аномальные клетки костного мозга и останавливает их производство аномальных белков, которые образуют отложения амилоида.
Стероиды обычно назначаются вместе с химиотерапией для усиления эффекта химиотерапевтических препаратов. Они также могут снизить ваши шансы на плохую реакцию на химиотерапию.
Ваш врач может также обсудить использование других методов лечения, таких как трансплантация стволовых клеток.
Вам также могут потребоваться специальные лекарства, если у вас сердечная или почечная недостаточность.
Вашим врачам и медсестрам необходимо будет тщательно контролировать количество употребляемой вами соли и количество выпиваемой вами жидкости. Вам также может потребоваться диализ, если у вас терминальная стадия почечной недостаточности.
Некоторым людям с почечной недостаточностью может подойти пересадка почки. Но основную проблему с костным мозгом все равно необходимо лечить с помощью химиотерапии, поскольку это предотвратит накопление амилоида в новой почке.
После химиотерапии вам понадобятся регулярные осмотры каждые 6–12 месяцев для выявления признаков возвращения амилоидоза AL.Если он вернется, возможно, вам придется снова начать химиотерапию.
Диагностика амилоидоза AL
Диагностика амилоидоза AL может быть сложной задачей, поскольку симптомы часто расплывчаты.
Небольшой образец ткани (биопсия) может быть взят из пораженной части вашего тела. Ваш врач расскажет вам, как это будет сделано.
Биопсия будет исследована под микроскопом в лаборатории, чтобы увидеть, есть ли в ней отложения амилоида.
Другие тесты
Вы также можете пройти другие тесты, чтобы оценить, как отложения амилоида повлияли на ваши отдельные органы.
Например:
- взятие образца костного мозга
- ультразвуковое сканирование сердца (эхокардиограмма) для проверки состояния вашего сердца
- различные анализы крови для выявления повреждений сердца, почек или других органов
- компьютерная томография или магнитно-резонансная томография для проверки состояния различных органов вашего тела
Национальный центр амилоидоза NHS при Королевской бесплатной больнице в Лондоне также предлагает тип сканирования тела, называемый сканированием SAP.
Это включает инъекцию небольшого количества радиоактивно меченного белка крови, называемого сывороточным амилоидным P-компонентом (SAP). Затем вас сканируют специальной камерой, которая обнаруживает радиоактивность.
Белок с радиоактивной меткой прикрепляется к любым отложениям амилоида в вашем теле, поэтому вы можете видеть пораженные участки тела.
Амилоидоз ATTR
АмилоидозATTR — очень редкое заболевание, вызванное отложениями амилоида из аномальных версий белка крови, называемого транстиретином (TTR).
Амилоидоз ATTR может передаваться по наследству и известен как наследственный амилоидоз ATTR. Люди с наследственным амилоидозом ATTR несут мутации в гене TTR.
Это означает, что их тела на протяжении всей жизни вырабатывают аномальные белки TTR, которые могут образовывать амилоидные отложения. Обычно они поражают нервы или сердце, или и то, и другое.
Другой тип амилоидоза ATTR не является наследственным. Это называется ATTR-амилоидозом дикого типа или старческим системным амилоидозом.
В этом состоянии отложения амилоида в основном поражают сердце, а также могут вызывать синдром запястного канала у некоторых людей.
Наследственный амилоидоз ATTR может вызывать симптомы в любом возрасте от 30 лет. Симптомы ATTR-амилоидоза дикого типа обычно появляются только в возрасте примерно 65 лет.
ATTR-амилоидоз можно диагностировать с помощью:
Лечение амилоидоза ATTR
Лекарства, используемые для лечения ATTR, включают:
- патизиран (Onpattro) — данные показывают, что он снижает инвалидность и улучшает качество жизни. Он также может остановить и потенциально обратить вспять болезнь
- inotersen (Тегседи) — данные показывают, что он замедляет прогрессирование болезни
Некоторые типы наследственного амилоидоза ATTR можно лечить с помощью трансплантации печени.
Сердечную недостаточность можно лечить, тщательно контролируя количество выпиваемой и выпиваемой соли, а также принимая лекарства от сердечной недостаточности. Трансплантация сердца может быть вариантом очень редко.
Информация о вас
Если у вас амилоидоз, ваша клиническая бригада передаст информацию о вас в Национальную службу регистрации врожденных аномалий и редких заболеваний (NCARDRS).
Это помогает ученым искать более эффективные способы профилактики и лечения этого состояния.Вы можете отказаться от регистрации в любое время.
Узнать больше о реестре
Последняя проверка страницы: 17 сентября 2020 г.
Срок следующей проверки: 17 сентября 2023 г.
Амилоидоз: причины, симптомы и лечение
Амилоидоз — редкое заболевание, при котором происходит накопление определенного белка, называемого амилоидом.
В отличие от других белков, амилоид не играет поддерживающей роли в организме. Вместо этого накопление амилоидного белка приводит к повреждению органов.
Амилоидоз обычно поражает органы, включая сердце, почки и печень.
Из этой статьи вы узнаете больше о причинах и симптомах амилоидоза, а также о том, как его лечат врачи.
Амилоидоз возникает, когда организм вырабатывает амилоидные белки. Причина развития амилоидов может варьироваться в зависимости от типа имеющегося амилоидоза.
Амилоидоз может поражать только один орган или может быть широко распространенным. Широко распространенный амилоидоз поражает несколько органов и систем организма.
Типы амилоидоза включают:
- амилоидоз легкой цепи иммуноглобулина (AL)
- вторичный амилоидоз (AA)
- семейный амилоидоз (ATTR)
- бета-2 амилоидоз микроглобулина (Abeta2m)
- локализованный амилоидоз (Abeta2m)
- Другие семейные амилоидозы
По данным Amyloidosis Foundation, AL встречается чаще, чем другие типы болезни. «AL» означает «амилоид» и «легкая цепь».
AL амилоидоз включает развитие аномальных белков антител в плазматических клетках костного мозга.
AA амилоидоз — это накопление амилоидных белков в результате реакции на другое заболевание.
Наследственная мутация гена также может вызывать наследственную форму амилоидоза.
Хотя амилоидоз может развиться у любого человека, определенные факторы повышают риск заболевания. К ним относятся:
- Возраст : амилоидоз может развиваться у молодых людей, но наиболее распространенная форма амилоидоза чаще возникает в возрасте от 50 до 80 лет.
- Семейный анамнез : существует генетическая форма амилоидоза, поэтому наличие близкого кровного родственника, такого как родитель, с этим заболеванием может увеличить риск для человека.
- Пол : Примерно две трети людей с амилоидозом AL — мужчины.
- Диализ : Люди, которые проходят длительный диализ для лечения заболевания почек, подвергаются повышенному риску развития определенной формы амилоидоза.
- История воспалительного заболевания : Некоторые состояния, такие как артрит или воспалительное заболевание кишечника, могут вызывать амилоидоз АА. По данным Национальной организации по редким заболеваниям, около 50% людей с амилоидозом AA страдают ревматоидным артритом.
Накопление амилоидных белков нарушает нормальные функции органов. Однако симптомы могут различаться в зависимости от того, какие органы поражает амилоидоз.
Общие симптомы могут включать:
Иногда амилоидные отложения могут накапливаться на определенном органе без широкого распространения в других областях. Например, амилоиды могут откладываться на коже, мочевом пузыре или гортани.
Однако чаще амилоидоз поражает более одного органа.
Симптомы амилоидоза могут имитировать другие заболевания. Например, симптомы, влияющие на функцию почек, могут привести к неправильной диагностике других заболеваний почек.
Поскольку амилоидоз — редкое заболевание, врачам может потребоваться некоторое время, чтобы поставить диагноз. Правильная диагностика амилоидоза имеет важное значение для выбора наиболее эффективного лечения.
Диагностическое исследование амилоидоза может включать:
- Биопсия ткани : Биопсия ткани включает в себя удаление небольшого образца ткани для проверки наличия амилоидных отложений.Врач обычно берет образец из жировой ткани под кожей в брюшной полости или из какого-либо органа.
- Биопсия костного мозга : Удаление костного мозга включает проверку на наличие отложений амилоида. Обычно врачи берут костный мозг из тазовой кости.
- Анализы крови и мочи : Различные анализы мочи и крови могут помочь определить, какие органы поражены. Например, анализы мочи могут указывать на повреждение почек, а анализы крови — на проблемы с сердцем.
В настоящее время нет лекарства от амилоидоза, но это состояние поддается лечению.
Лечение включает замедление прогрессирования заболевания, уменьшение симптомов и улучшение качества жизни человека.
Лечение зависит от тяжести симптомов и типа амилоидоза.
Возможные методы лечения для уменьшения выработки амилоидного белка включают:
Химиотерапия
Химиотерапия — это использование различных препаратов для уничтожения аномальных клеток крови, которые способствуют образованию амилоидов.
Иногда можно использовать лекарства от миеломы, которая представляет собой рак плазматических клеток.
Врач может порекомендовать следующие химиотерапевтические препараты:
- мелфалан
- бендамустин
- циклофосфамид
Тип химиотерапии, которую получает человек, будет зависеть от степени симптомов, возраста и симптомов органов.
Трансплантация стволовых клеток
В некоторых случаях врач может порекомендовать трансплантацию стволовых клеток после химиотерапии.
После разрушения аномальных клеток, производящих амилоиды, с помощью химиотерапии, трансплантация стволовых клеток может помочь в развитии здорового костного мозга.
Трансплантация стволовых клеток — сложный процесс, и не каждый человек с амилоидозом подходит для этого.
Борьба с основными заболеваниями
Лечение людей с амилоидозом AA часто включает борьбу с нижележащим воспалительным заболеванием, которое привело к накоплению амилоидов.
Как только человек вылечит основное заболевание, такое как ревматоидный артрит, у него может быть меньше симптомов амилоидоза.
Поддерживающее лечение
Человеку также может потребоваться лечение осложнений заболевания или изменение диеты или образа жизни, чтобы облегчить лечение.
Поддерживающее лечение может включать широкий спектр лекарств и методов лечения, в том числе:
- лекарства для контроля сердечной недостаточности
- лекарства от кровяного давления
- диализ для лечения повреждения почек
- нутритивная поддержка и рекомендации для людей с проблемами пищеварения
Поскольку амилоидные белки могут повредить органы, часто возникают осложнения.
Возможные осложнения амилоидоза включают:
- Поражение почек : амилоидоз часто поражает почки. Если почки не могут эффективно удалять продукты жизнедеятельности, это может привести к повреждению или отказу почек.
- Сердечная недостаточность : Накопление амилоида может отрицательно повлиять на работу сердца. Это может привести к нарушению сердечного ритма и неспособности сердца эффективно перекачивать кровь.
- Осложнения нервной системы : нервная система может работать неправильно, что может привести к головокружению, онемению, проблемам с пищеварением и болям в суставах.
Хотя исследования продолжаются, лекарства от амилоидоза в настоящее время не существует. Исход болезни часто зависит от пораженных органов.
Лечение амилоидоза может замедлить развитие аномальных белков и прогрессирование заболевания. Многие варианты лечения также помогают людям управлять своими симптомами.



 Важными симптомами являются геморрагии, фестончатый край зрачка, потеря
массы тела, снижение зрения [38-47].
Важными симптомами являются геморрагии, фестончатый край зрачка, потеря
массы тела, снижение зрения [38-47].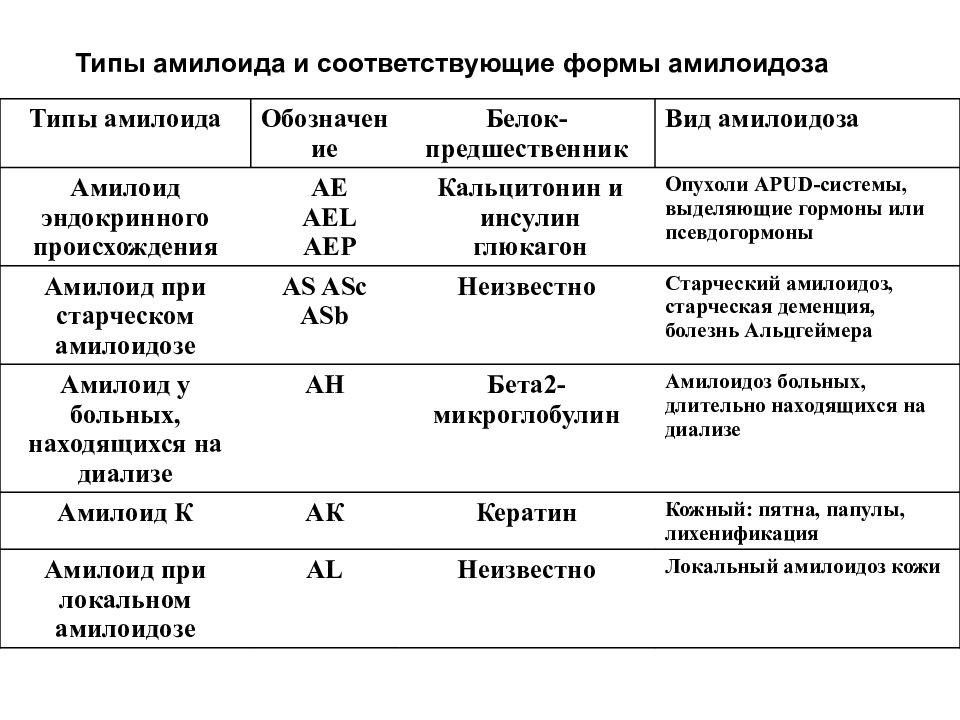

 Для установления связи протеинурии с амилоидозом необходимо также исключить
протеинурию, связанную с диабетической нефропатией и гипертонической почкой [4,5,29,48,51-56].
Для установления связи протеинурии с амилоидозом необходимо также исключить
протеинурию, связанную с диабетической нефропатией и гипертонической почкой [4,5,29,48,51-56].
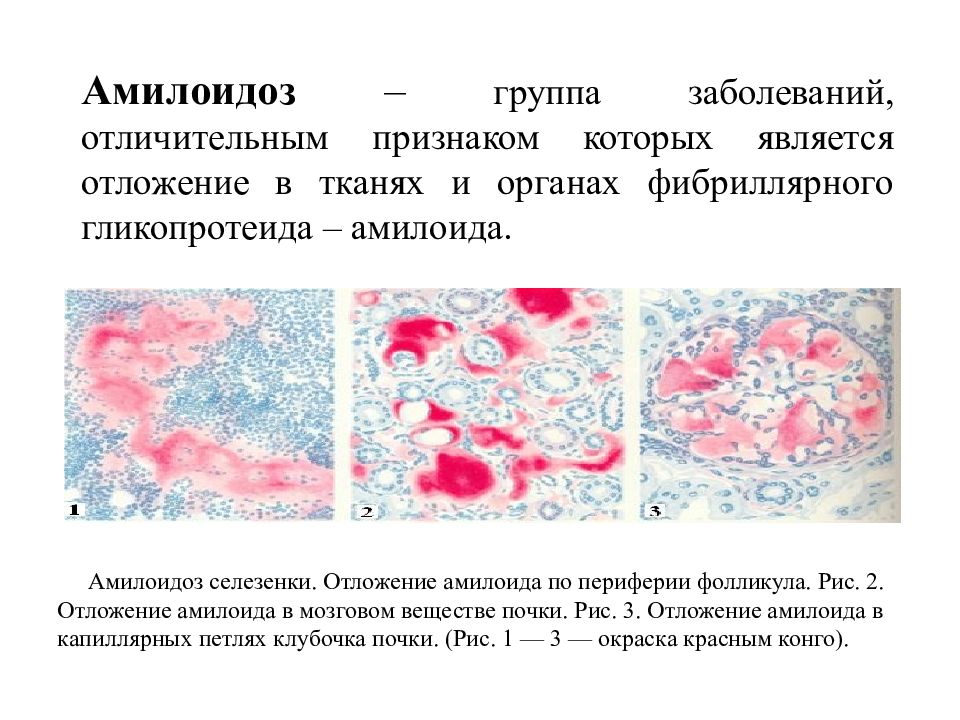
 Из-за
поражения преимущественно мелких немиелинизированных волокон электромиография и исследование скорости
проведения нервного импульса обычно неинформативны для ранней диагностики амилоидной полиневропатии [38,39].
Доминирование жалоб, связанных с поражением нервной системы, является отличительной чертой ATTR-амилоидоза.
Из-за
поражения преимущественно мелких немиелинизированных волокон электромиография и исследование скорости
проведения нервного импульса обычно неинформативны для ранней диагностики амилоидной полиневропатии [38,39].
Доминирование жалоб, связанных с поражением нервной системы, является отличительной чертой ATTR-амилоидоза.
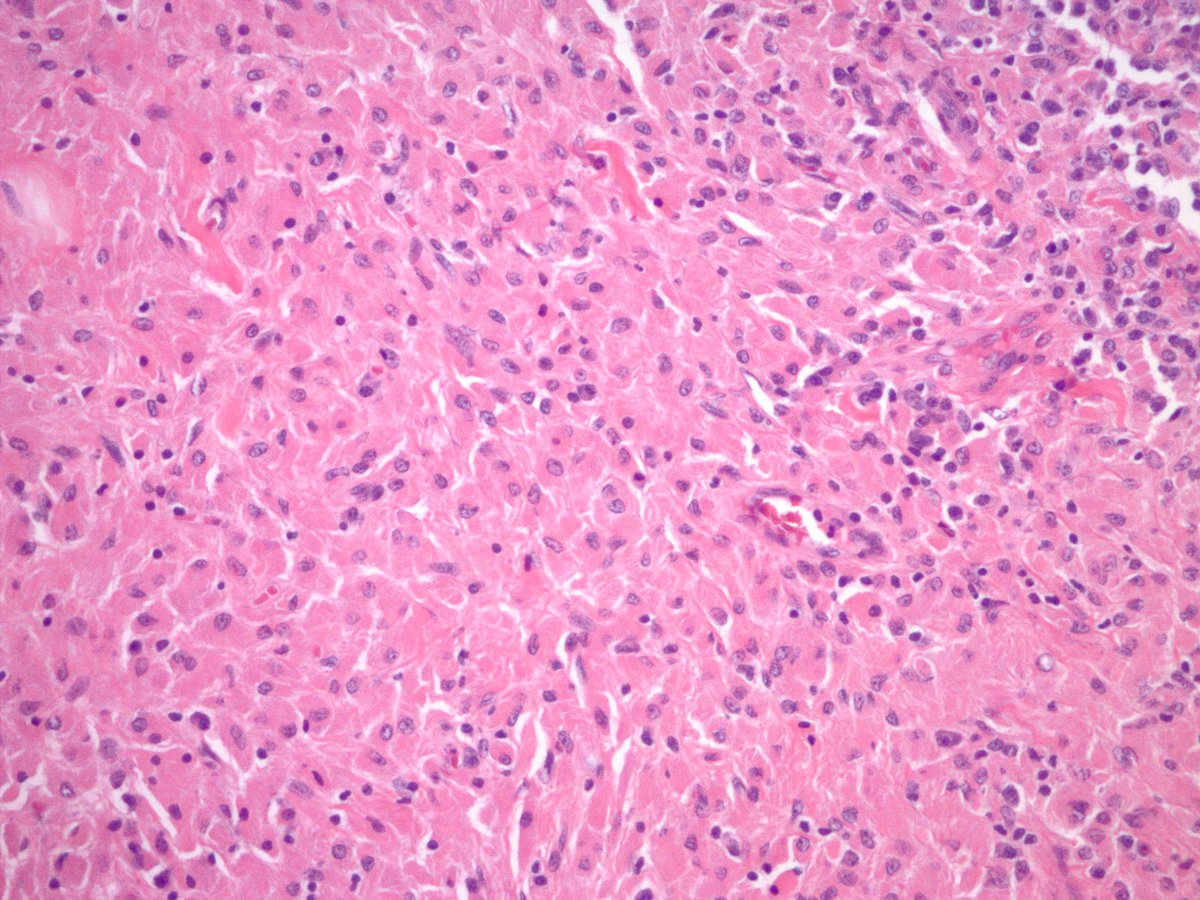
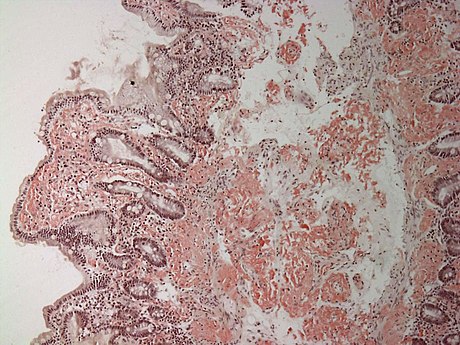 Другие частые проявления поражения вегетативной нервной системы – моторная диарея, дисфункция
мочевого пузыря, половой сферы, гипогидроз [1,2,38,51]. Наряду с моторной диареей причиной значительного (на
9-18 кг) снижения массы тела могут быть нарушения трофики мышц [38,39].
Другие частые проявления поражения вегетативной нервной системы – моторная диарея, дисфункция
мочевого пузыря, половой сферы, гипогидроз [1,2,38,51]. Наряду с моторной диареей причиной значительного (на
9-18 кг) снижения массы тела могут быть нарушения трофики мышц [38,39].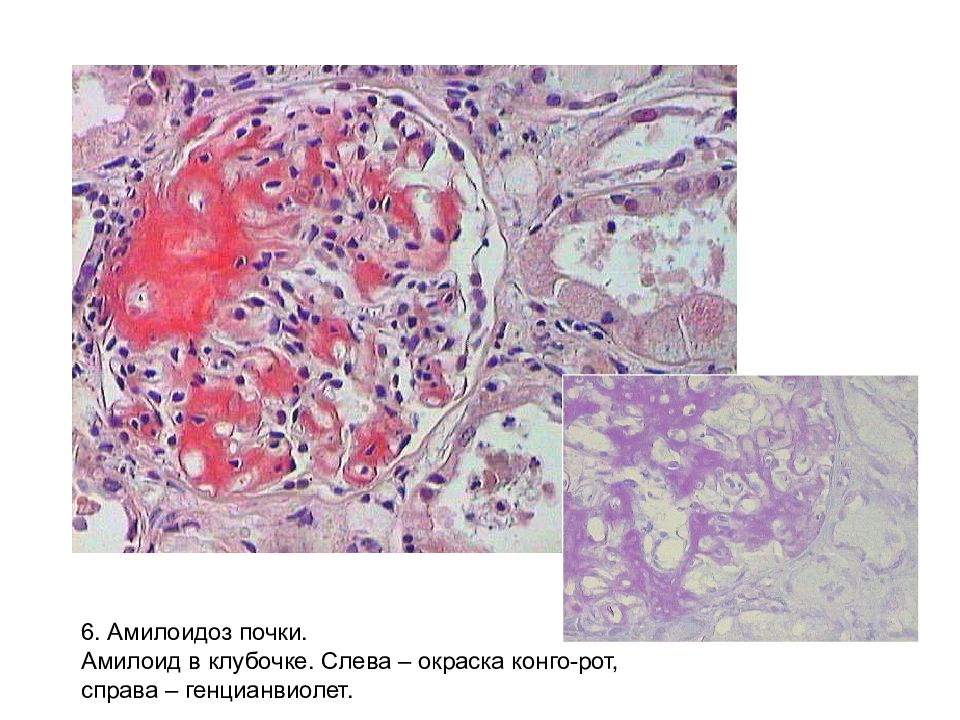 Ложная диагностика амилоидоза печени возможна у больных с тяжелой застойной правожелудочковой
недостаточностью [2,4,48,51].
Ложная диагностика амилоидоза печени возможна у больных с тяжелой застойной правожелудочковой
недостаточностью [2,4,48,51].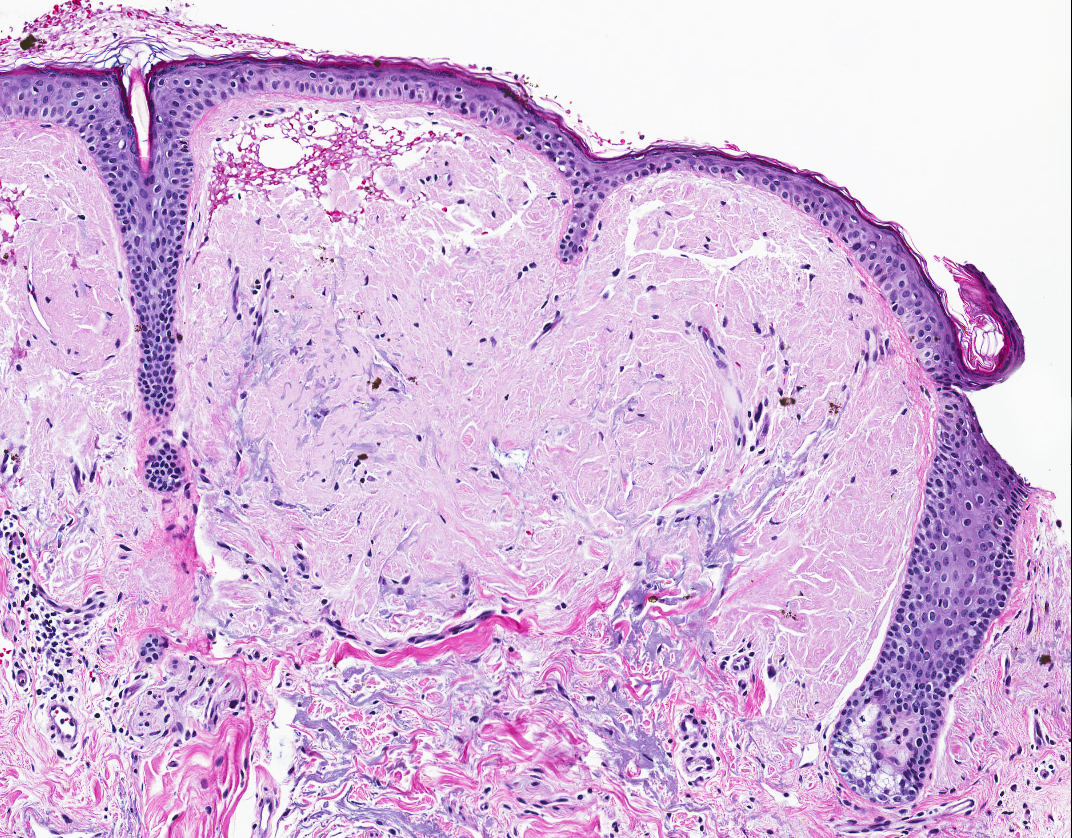 Для системного AL-амилоидоза характерно обнаружение диффузного интерстициального легочного
амилоидоза. В связи с редкостью дыхательной недостаточности необходимости в морфологической верификации
легочного амилоидоза обычно не возникает. Наиболее информативным методом диагностики амилоидоза легких
является компьютерная томография [1,2,48]. У больных локальным трахеобронхиальным AL-амилоидозом важными
методами мониторирования течения заболевания являются ларингоскопия и бронхоскопия [27,48].
Для системного AL-амилоидоза характерно обнаружение диффузного интерстициального легочного
амилоидоза. В связи с редкостью дыхательной недостаточности необходимости в морфологической верификации
легочного амилоидоза обычно не возникает. Наиболее информативным методом диагностики амилоидоза легких
является компьютерная томография [1,2,48]. У больных локальным трахеобронхиальным AL-амилоидозом важными
методами мониторирования течения заболевания являются ларингоскопия и бронхоскопия [27,48].
 Прогрес сирование полиневропатии
объективизируют на основании результатов стимуляционной электромиографии и других нейрофизиологических и
нейровизуализационных методов обследования (см. выше). Важным показателем тяжести больных AL-амилоидозом
является разница в содержании свободных легких цепей иммуноглобулинов более 180 мг/л, установленная методом
Freelite [2,38,51,48,60,61,64].
Прогрес сирование полиневропатии
объективизируют на основании результатов стимуляционной электромиографии и других нейрофизиологических и
нейровизуализационных методов обследования (см. выше). Важным показателем тяжести больных AL-амилоидозом
является разница в содержании свободных легких цепей иммуноглобулинов более 180 мг/л, установленная методом
Freelite [2,38,51,48,60,61,64].

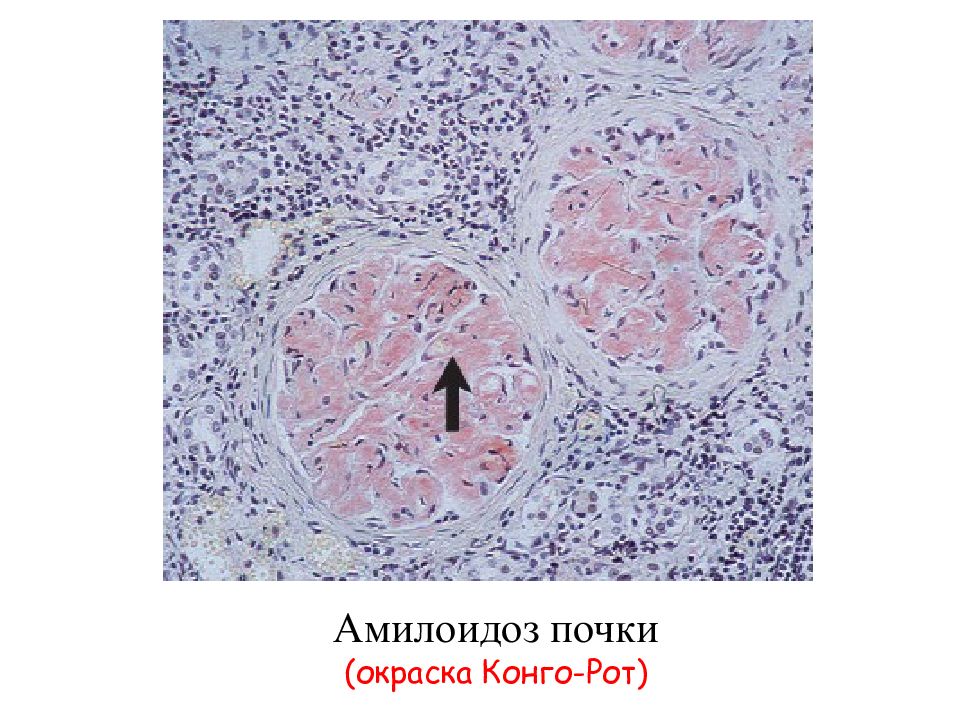 В этот период при отсутствии противопоказаний возможна высокодозная химиотерапия с
поддержкой аутологичными стволовыми клетками, которая позволяет достичь длительной ремиссии
[2,26,37,56,57,65,78,79].
В этот период при отсутствии противопоказаний возможна высокодозная химиотерапия с
поддержкой аутологичными стволовыми клетками, которая позволяет достичь длительной ремиссии
[2,26,37,56,57,65,78,79]. Особо выделяют NT-proBNP-ответ (снижение уровня маркера на 30% и более или на 300 нг/л и более у пациентов с
исходным уровнем более 650 нг/л). С клиническим эффектом лечения больше коррелирует почечный ответ (снижение
протеинурии на 75% и более, повышение сывороточного креатинина не более 25% от исходного). Ответ со стороны
других органов не обладает существенной прогностической информативностью. Эффективность лечения амилоидоза
печени оценивают по снижению активности щелочной фосфатазы (на 50% и более) и уменьшению размеров печени
(краниокаудальный размер по данным КТ должен уменьшиться на 30% в течение года после достижения
гематологической ремиссии). Эффективность лечения амилоидной полиневропатии определяют, главным образом, по
результатам клинического неврологического осмот ра. Уменьшение амилоидных депозитов в мягких тканях может
быть оценено по данным компьютерной томографии или МРТ. Эффективным методом оценки общего содержания
амилоида в тканях служит сцинтиграфия с радиоактивным амилоидным Ркомпонентом [2,26,37,57,60,61,64].
Особо выделяют NT-proBNP-ответ (снижение уровня маркера на 30% и более или на 300 нг/л и более у пациентов с
исходным уровнем более 650 нг/л). С клиническим эффектом лечения больше коррелирует почечный ответ (снижение
протеинурии на 75% и более, повышение сывороточного креатинина не более 25% от исходного). Ответ со стороны
других органов не обладает существенной прогностической информативностью. Эффективность лечения амилоидоза
печени оценивают по снижению активности щелочной фосфатазы (на 50% и более) и уменьшению размеров печени
(краниокаудальный размер по данным КТ должен уменьшиться на 30% в течение года после достижения
гематологической ремиссии). Эффективность лечения амилоидной полиневропатии определяют, главным образом, по
результатам клинического неврологического осмот ра. Уменьшение амилоидных депозитов в мягких тканях может
быть оценено по данным компьютерной томографии или МРТ. Эффективным методом оценки общего содержания
амилоида в тканях служит сцинтиграфия с радиоактивным амилоидным Ркомпонентом [2,26,37,57,60,61,64].