Вирус иммунодефицита человека — Википедия
Эта статья — о патогене — вирусе иммунодефицита человека. О заболевании см. ВИЧ-инфекция; о терминальной стадии болезни см. СПИД. Запросы «ВИЧ» и «Вич» перенаправляются сюда, см. также: Вич (значения)| Вирус иммунодефицита человека | |||
|---|---|---|---|
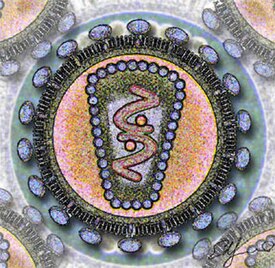 Стилизованное изображение сечения ВИЧ[1] | |||
промежуточные ранги
| |||
Primate lentivirus group | |||
| |||
VI: оцРНК-ОТ-вирусы | |||
Ви́рус иммунодефици́та челове́ка — ретровирус из рода лентивирусов, вызывающий медленно прогрессирующее[3] заболевание — ВИЧ-инфекцию[4][5].
Вирус поражает клетки иммунной системы, имеющие на своей поверхности рецепторы CD4: Т-хелперы, моноциты, макрофаги, клетки Лангерганса[6], дендритные клетки, клетки микроглии[7]. В результате работа иммунной системы угнетается и развивается
На 2017 г. вакцины против ВИЧ


В 1981 году появились первые три научные статьи о необычных случаях развития пневмоцистной пневмонии и саркомы Капоши у гомосексуальных мужчин
В июле 1982 года для обозначения этого состояния был предложен термин синдром приобретённого иммунного дефицита (СПИД, AIDS)[28]. В сентябре 1982 года СПИДу было дано полноценное определение как нозологической форме на основании наблюдения ряда оппортунистических инфекций у четырёх групп пациентов, указанных выше[22][29].
В период с 1981 по 1984 год вышло несколько работ, связывающих вероятность развития СПИДа с анальным сексом или с влиянием наркотиков
Вирус иммунодефицита человека независимо открыли в 1983 году в двух лабораториях: в Институте Пастера во Франции под руководством Люка Монтанье и в Национальном институте рака в США под руководством Роберта Галло. Результаты исследований, в которых из тканей пациентов с симптомами СПИДа впервые удалось выделить новый ретровирус, были опубликованы 20 мая 1983 года в журнале Science[36][37]. В этих же работах выделенный из больных СПИДом вирус был впервые успешно размножен в культивируемых Т-лимфоцитах. Французская группа исследователей показала, что серологически этот вирус отличается от HTLV-I, и назвала его LAV («вирус, ассоциированный с лимфаденопатией»), а американская группа назвала его HTLV-III, ошибочно отнеся к группе HTLV-вирусов. Исследователи выдвинули предположение, что вирус может вызывать синдром приобретённого иммунного дефицита
В 1986 году было обнаружено, что вирусы, открытые в 1983 французскими и американскими исследователями, генетически идентичны. Первоначальные названия вирусов были упразднены и предложено одно общее название — вирус иммунодефицита человека[38]. В 2008 году Люк Монтанье и Франсуаза Барр-Синусси были удостоены Нобелевской премии в области физиологии или медицины «за открытие вируса иммунодефицита человека»
Инфицирование[править | править код]
Вирус может передаваться через прямой контакт повреждённой или неповрежденной слизистой оболочки или повреждённой кожи здорового человека с биологическими жидкостями заражённого человека: кровью, предсеменной жидкостью (выделяющейся на протяжении всего полового акта), спермой, секретом влагалища, грудным молоком. Передача вируса может происходить при незащищённом анальном, вагинальном или оральном сексе[40][41].
Интактная, неповреждённая кожа является эффективным барьером для инфекции, так как в коже отсутствуют клетки, которые могут быть заражены ВИЧ. Для успешной инфекции требуется прямой контакт с кровеносной системой или с мембранами клеток слизистых оболочек. Слизистые оболочки половых органов и прямой кишки часто получают незначительные повреждения при половом акте, через которые вирус может проникать в кровь. Такие повреждения чаще возникают при наличии заболеваний, передающихся половым путём, например, в случае герпеса. Поэтому особенно опасной формой полового акта для принимающего партнёра является незащищённый анальный секс, так как при этой форме возникает наибольшее число мелких и крупных повреждений
Передача вируса происходит с большей вероятностью при использовании заражённых игл и шприцев (особенно потребителями инъекционных наркотиков), а также при переливании крови (в случае нарушения медицинским персоналом установленных процедур проверки донорской крови)[44]. Также передача вируса может произойти между матерью и ребёнком во время беременности, родов (заражение через кровь матери)[45][46] и при грудном вскармливании (причём как от заражённой матери к здоровому ребёнку через грудное молоко, так и от заражённого ребёнка к здоровой матери через покусывание груди во время кормления)
Вирус не передаётся воздушно-капельным путём, бытовым путём, при соприкосновении с неповреждённой кожей, через укусы большинства кровососущих насекомых[48] (исключение мухи-жигалки), слёзы[49] и слюну (из-за того, что концентрация вирионов ВИЧ в этих жидкостях ниже инфицирующей дозы, а также из-за того, что слюна — агрессивная среда, разрушающая своими ферментами вирионы ВИЧ)[49].
Болезнь[править | править код]

В течении болезни выделяют три стадии: острую инфекцию, латентный период и терминальную стадию (СПИД) (см. иллюстрацию). В ходе развития ВИЧ-инфекции у одного и того же человека в результате мутаций возникают новые штаммы вируса, которые различаются по скорости воспроизведения и способности инфицировать[8][9]. Размножившись, вирусные частицы высвобождаются из поражённых клеток и внедряются в новые — цикл развития повторяется. Инфицированные вирусом Т-хелперы постепенно гибнут из-за разрушения вирусом, апоптоза или уничтожения Т-киллерами. В процессе развития ВИЧ-инфекции количество Т-хелперов (CD4
Эпидемиология[править | править код]
По данным на 2011 год, в мире за всё время ВИЧ-инфекцией заболели 60 миллионов человек, из них: 25 миллионов умерли, а 35 миллионов живут с ВИЧ-инфекцией[51]. Более двух третей из них проживают в Африке к югу от пустыни Сахара[52]. Эпидемия началась здесь в конце 1970-х — начале 1980-х. Затем эпидемия перекинулась в США, Западную Европу и страны Южной Африки. Сегодня, за исключением стран Африки, быстрее всего вирус распространяется в Центральной Азии и Восточной Европе (в том числе в России). Эпидемическая ситуация в этих регионах сдерживалась до конца 1990-х, затем с 1999 по 2002 годы количество инфицированных почти утроилось — в основном за счёт инъекционных наркоманов. Значительно ниже среднего ВИЧ-инфекция распространена в Восточной Азии, Северной Африке и на Ближнем Востоке. В масштабе планеты эпидемическая ситуация стабилизировалась, количество новых случаев ВИЧ-инфекции снизилось с 3,5 миллионов в 1997 году до 2,7 миллионов в 2007 году[52]. По данным на конец 2016 года, в России 848 тысяч человек живут с ВИЧ-инфекцией, за период с 1986 по 2016 год умерло от разных причин 220 тысяч ВИЧ-инфицированных граждан России[53] (подробнее см. Статистика заболеваемости и смертности по России).
Диагностика[править | править код]
Анализ крови позволяет обнаружить антитела к белкам вируса (ИФА), реакцию антител на белки вируса (вестерн-блот), РНК вируса (ОТ-ПЦР)[54]. Определение вирусной нагрузки (подсчёт количества копий РНК вируса в миллилитре плазмы крови) позволяет судить о стадии заболевания и эффективности лечения[55][56].
Обязательная проверка донорской крови в развитых странах в значительной степени сократила возможность передачи вируса при её использовании. Тестирование на ВИЧ беременных женщин позволяет своевременно начать приём лекарств и родить здорового ребёнка.
Существует мнение, что принудительное тестирование населения бесперспективно с точки зрения сдерживания эпидемии[57] и нарушает права человека[58]. В России проведение теста без согласия человека является незаконным[59], однако существуют ситуации, в которых предоставление результатов тестирования на ВИЧ является обязательным, но не насильственным (донорство, трудоустройство медицинских работников, для иностранных граждан, получающих разрешение на пребывание в РФ, в местах лишения свободы при наличии клинических показаний)[60].
Лечение[править | править код]
Из 35 миллионов человек, живущих с ВИЧ-инфекцией, часть остаётся в живых благодаря антиретровирусной терапии. В случае отсутствия антиретровирусной терапии ВИЧ-инфекции, смерть наступает в среднем через 9—11 лет после заражения[8][61]. При проведении антиретровирусной терапии продолжительность жизни пациента составляет 70—80 лет[14][15][16]. Антиретровирусные препараты мешают ВИЧ размножаться в клетках иммунной системы человека, блокируя внедрение вирионов в клетки и нарушая на разных этапах процесс сборки новых вирионов. Своевременно начатое лечение антиретровирусными препаратами в сотни раз снижает риск развития СПИДа и последующей смерти[62][63][64]. Антиретровирусные препараты у части пациентов вызывают побочные эффекты, в некоторых случаях даже требующие сменить схему лечения (набор принимаемых лекарств).
Терапию назначают при снижении иммунитета и/или высокой вирусной нагрузке. Если число CD4+-лимфоцитов велико и вирусная нагрузка низкая, терапию не назначают. После назначения терапии лекарства нужно принимать ежедневно в одно и то же время и пожизненно, что создаёт неудобства для пациентов. Кроме того, следует учитывать высокую стоимость месячного курса лекарств. В 2014 году необходимые лекарства получали менее половины из 9,5 млн человек, нуждающихся в противовирусной терапии[65].
Также все беременные женщины с ВИЧ-инфекцией должны начинать незамедлительную ВААРТ для предотвращения передачи ВИЧ плоду[66].
Согласно рекомендациям ВОЗ, ВААРТ следует незамедлительно начинать всем ВИЧ-инфицированным детям до полутора лет[67]. Начало терапии у детей, получивших ВИЧ от матери, в течение 3 месяцев после родов снижает смертность на 75 %[68]. В отсутствие лечения треть ВИЧ-инфицированных детей умирает в течение первого года жизни и 50 % — в течение второго года. Если диагностика ВИЧ невозможна, лечение следует начинать в возрасте 9 месяцев, либо ранее, в случае появления симптомов[69].
По состоянию на февраль 2016 года было объявлено, что группе немецких учёных удалось полностью удалить тип ВИЧ-1 из живых клеток. Испытания проводились на клетках человека, вживлённых подопытным мышам. Испытания на людях должны проводиться в ближайшее время[70][71][72].
В 2018 году Администрацией по контролю над продуктами и лекарствами (FDA) был одобрен ибализумаб (ibalizumab-uiyk) для применения в терапии пациентов с мультирезистентным ВИЧ-1. Препарат представляет собой моноклональное антитело, которое связывается с CD4 рецепторами T-клеток и подавляет процесс проникновения вируса в клетку человека. Ибализумаб может применяться в терапии с другими антиретровирусными лекарствами. По результатам клинических исследований с участием 40 пациентов, ранее прошедших лечение более чем 10 различными антиретровирусными агентами, вирусная нагрузка снизилась у большинства испытуемых через одну неделю после введения первой дозы препарата. Через 24 недели терапии вирусологическая супрессия была достигнута у 43 % участников клинических испытаний[73].
ВИЧ в 2019 году вносили в спиcок десяти основных проблем здравоохранения, которые требуют особого внимания ВОЗ[74].
Вирус иммунодефицита человека относят к семейству ретровирусов (Retroviridae), роду лентивирусов (Lentivirus). Название Lentivirus происходит от латинского слова lente — медленный. Такое название отражает одну из особенностей вирусов этой группы, а именно — медленную и неодинаковую скорость развития инфекционного процесса в макроорганизме. Для лентивирусов также характерен длительный инкубационный период[75].
Для вируса иммунодефицита человека характерна высокая частота генетических изменений, возникающих в процессе самовоспроизведения. Частота возникновения ошибок у ВИЧ составляет 10−3 — 10−4 ошибок на геном на цикл репликации, что на несколько порядков больше аналогичной величины у эукариот. Размер генома ВИЧ составляет примерно 104нуклеотидов. Из этого следует, что практически каждый дочерний геном хотя бы на один нуклеотид отличается от своего предшественника. В современной классификации различают два основных вида ВИЧ — ВИЧ-1 и ВИЧ-2. Эти вирусы предположительно возникли в результате независимой передачи людям SIV (вируса иммунодефицита обезьян) шимпанзе и мангабеев соответственно[76].
И ВИЧ-1, и ВИЧ-2 способны вызывать серьёзный иммунодефицит, однако клиническое течение болезни несколько различается. Известно, что ВИЧ-2 менее патогенен и передаётся с меньшей вероятностью, чем ВИЧ-1. Вероятно, это связано с тем, что ВИЧ-2-инфекция характеризуется более низким числом вирусных частиц на миллилитр крови. Отмечено, что инфекция ВИЧ-2 обеспечивает носителю небольшую защиту от заражения ВИЧ-1. Однако описаны случаи двойной инфекции, причём заражение может происходить в любом порядке. Инфекция ВИЧ-2 реже заканчивается развитием СПИДа. Есть сведения о несколько большей частоте развития саркомы Капоши, кандидоза ротовой полости и хронической лихорадки при ВИЧ-1/СПИДе. При ВИЧ-2/СПИДе чаще развивается энцефалит, хроническая или бактериальная диарея, серьёзные цитомегаловирусные инфекции и холангит[76]. К роду Lentivirus также относят виды, вызывающие схожие заболевания у обезьян, кошек, лошадей, овец и т. д.[8][77][78].
ВИЧ-1[править | править код]
ВИЧ-1 описан в 1983 году и является наиболее распространённым и патогенным видом ВИЧ[79]. Глобальная эпидемия ВИЧ-инфекции главным образом обусловлена распространением ВИЧ-1. В подавляющем большинстве случаев, если не оговорено иначе, под ВИЧ подразумевают ВИЧ-1[80].
Вид ВИЧ-1 классифицируют на главную группу М и несколько побочных групп. Считается, что группы M, N, O, P образовались в результате независимых случаев передачи SIV от обезьяны к человеку, и последующей мутации вируса до ВИЧ[81].
- Вирусы группы М (англ. main — основная) являются причиной более 90 % случаев ВИЧ-инфекции. Группу М классифицируют на несколько клад, называемых подтипами, также обозначаемых буквами:
- подтип A широко распространён, например, в Западной Африке и России[82];
- подтип B доминирует в Европе, Северной Америке, Южной Америке, Японии, Таиланде, Австралии[83];
- подтип C преобладает в Южной и Восточной Африке, Индии, Непале, некоторых частях Китая[83];
- подтип D обнаружен только в Восточной и Центральной Африке[83];
- подтип E не был выявлен в нерекомбинантном виде, лишь совместно с подтипом А как CRF01_AE в Юго-Восточной Азии[83];
- подтип F выявлен в Центральной Африке, Южной Америке и Восточной Европе[84];
- подтип G и рекомбинантная форма CRF02_AG выявлены в Африке и Центральной Европе[84];
- подтип H обнаружен только в Центральной Африке[84];
- подтип I был предложен для описания штамма-продукта множественной рекомбинации CRF04_cpx нескольких подтипов[85];
- подтип J распространён в Северной, Центральной и Западной Африке и странах Карибского бассейна[86];
- подтип K обнаружен только в Конго и Камеруне[84].
- Группа O (англ. outlier — непохожий) обнаружена в Центральной Африке и Западной Африке. Наиболее распространена в Камеруне, где в 1997 году более 2 % пациентов были заражены вирусом группы О[87] (около 100 000 человек, по данным на 2013 год)[88]. Вирусы этой группы не определялись ранними версиями тест-систем на ВИЧ-1; современные тесты определяют вирусы и группы О, и группы N[89].
- Группа N (англ. non-M, non-O — ни M, ни O) обозначает штаммы не М и не О, описана в 1998 году и обнаружена только в Камеруне. С 2006 года выявлены лишь 10 заражений вирусами группы N[90].
- Группа P — в 2009 году была определена нуклеотидная последовательность РНК ВИЧ, значительно сходная с вирусом иммунодефицита обезьян, описанным у горилл (SIVgor), но не с SIV, характерным для шимпанзе (SIVcpz). Вирус был выделен из образцов, полученных от женщины камерунского происхождения, проживающей во Франции[91][92][93].
ВИЧ-2[править | править код]
ВИЧ-2 идентифицирован в 1986 году[94], генетически очень близок к T-лимфотропному вирусу SIVsmm мангабеев, и в меньшей степени к вирусу ВИЧ-1. Геномы ВИЧ-1 и ВИЧ-2 имеют гомологию консервативных генов gag и pol около 60 %, и до 45 % генов белков оболочки[95]. По состоянию на 2010 год, описано 8 групп ВИЧ-2, лишь группы A и B являются эпидемическими. Вирусы группы А распространены в Западной Африке, Анголе, Мозамбик, Бразилии, Индии и мало распространены в США и Европе[96][97]. Вирусы группы В распространены в Западной Африке[98][99].
Строение вируса иммунодефицита человекаВирионы ВИЧ имеют вид сферических частиц, диаметр которых составляет около 100—120 нанометров[100]. Это приблизительно в 60 раз меньше диаметра эритроцита[101]. В состав зрелых вирионов входит несколько тысяч белковых молекул различных типов.
Капсид зрелого вириона, состоящий из примерно 2000 молекул белка р24, имеет форму усечённого конуса[102].
Внутри капсида находится белково-нуклеиновый комплекс: две нити вирусной РНК, прочно связанные с белком нуклеокапсида p7, ферменты (обратная транскриптаза, протеаза, интеграза)[102]. С капсидом также ассоциированы белки Nef и Vif (7—20 молекул Vif на вирион). Внутри вириона (и, вероятнее всего, за пределами капсида) обнаружен белок Vpr[40]:8-11. Кроме того, с капсидом ВИЧ-1 (но не ВИЧ-2) связаны около 200 копий клеточного фермента пептидилпролилизомеразы A[en] (циклофилин А), необходимого для сборки вириона[103].
Капсид окружён оболочкой, образованной примерно 2000 молекул матриксного белка p17[102]. Матриксная оболочка, в свою очередь, окружена двуслойной липидной мембраной, являющейся наружной оболочкой вируса. Она образована молекулами фосфолипидов, захваченными вирусом во время его отпочковывания от клетки, в которой он сформировался[104]. В липидную мембрану встроены 72 гликопротеиновых комплекса Env, каждый из которых образован тремя молекулами трансмембранного гликопротеина gp41 (TM), служащего «якорем» комплекса, и тремя молекулами поверхностного гликопротеина gp120 (SU)[103]. С помощью белка gp120 вирус присоединяется к рецептору CD4 и корецептору, находящимся на поверхности Т-лимфоцитов человека. Стехиометрическое соотношение p24:gp120 в вирионе составляет 60—100:1[40]:11. При формировании наружной оболочки вируса также происходит захват некоторого количества мембранных белков клетки, в том числе человеческих лейкоцитарных антигенов (HLA) классов I и II и молекул адгезии[102][105].
Белки вириона интенсивно изучаются, поскольку являются мишенями разрабатываемых лекарств и вакцины против ВИЧ.
Функции важных структурных белков ВИЧ-1[102][105]
| Сокращение | Описание | Функции |
|---|---|---|
| gp41 (TM, transmembrane) | Трансмембранный гликопротеин массой 41 кДа | Располагается во внешнем слое липидной мембраны, играет роль «якоря», удерживающего молекулы белка gp120 |
| gp120 (SU, surface) | Гликопротеин массой 120 кДа | Наружный белок вириона. Нековалентно связан с трансмембранным белком gp41. С одной молекулой gp41 связаны 3—5 молекул gp120. Способен связывать рецептор CD4. Играет важную роль в процессе проникновения вируса в клетку. |
| p24 (CA, capsid) | Белок массой 24 кДа | Образует капсид вируса |
| p17 (MA, matrix) | Матриксный белок массой 17 кДа | Около двух тысяч молекул этого белка образуют слой толщиной 5—7 нм, располагающийся между внешней оболочкой и капсидом вируса. |
| p7 (NC, nucleocapsid) | Нуклеокапсидный белок массой 7 кДа | Входит в состав капсида вируса. Образует комплекс с вирусной РНК. |
Генетический материал ВИЧ представлен двумя копиями положительно-смысловой (+)РНК[103]. Геном ВИЧ-1 имеет длину 9000 нуклеотидов. Концы генома представлены длинными концевыми повторами (англ. long terminal repeat, LTR), которые управляют продукцией новых вирусов и могут активироваться и белками вируса, и белками инфицированной клетки.
9 генов ВИЧ-1 кодируют, по крайней мере, 15 белков[106]. Ген pol кодирует ферменты: обратную транскриптазу (RT), интегразу (IN) и протеазу (PR). Ген gag кодирует полипротеин Gag/p55, расщепляемый вирусной протеазой до структурных белков p6, p7, p17, p24. Ген env кодирует белок gp160, расщепляемый клеточной эндопротеазой фурином на структурные белки gp41 и gp120[40]:8-12. Другие шесть генов — tat, rev, nef, vif, vpr, vpu (vpx у ВИЧ-2) — кодируют белки, отвечающие за способность ВИЧ-1 инфицировать клетки и производить новые копии вируса. Репликация ВИЧ-1 in vitro возможна без генов nef, vif, vpr, vpu, однако их продукты необходимы для полноценной инфекции in vivo[107][108][109].
Gag[править | править код]
Полипротеин-предшественник Gag/p55 синтезируется с полноразмерной геномной РНК (которая в данном случае служит в качестве мРНК) в процессе стандартной кэп-зависимой трансляции, но возможна и IRES-зависимая трансляция. Предшественники функциональных белков располагаются в составе полипротеина Gag/p55 в следующем порядке: p17…p24…p2…p7…p1…p6[40]:8 (р1 и р2 — соединительные пептиды; другие продукты расщепления Gag/p55 описаны выше). Нерасщеплённый протеазой Gag/p55 содержит три основных домена: домен мембранной локализации (М, membrane targeting), домен взаимодействия (I, interaction) и «поздний» домен (L, late). Домен М, расположенный внутри области p17/МА, миристилируется (присоединяются остатки миристиновой кислоты) и направляет Gag/p55 к плазматической мембране. Домен I, находящийся внутри области p7NC (NC, nucleocapsid), отвечает за межмолекулярные взаимодействия отдельных мономеров Gag/p55. Домен L, также локализованный в области p7NC, опосредует отпочковывание вирионов от плазматической мембраны; в этом процессе участвует также р6 область полипротеина Gag/p55[40]:8[110].
Vpu[править | править код]
Двумя важными функциями белка Vpu являются: 1) разрушение клеточного рецептора CD4 в эндоплазматическом ретикулуме путём привлечения убиквитинлигазных комплексов и 2) стимуляция выделения дочерних вирионов из клетки путём инактивации интерферон-индуцируемого трансмембранного белка CD317/BST-2, получившего также название «tetherin» за его способность подавлять выделение вновь образовавшихся дочерних вирионов посредством их удержания на поверхности клетки[107][108][111][112][113][114].
Vpr[править | править код]
Белок Vpr необходим для репликации вируса в неделящихся клетках, в том числе макрофагах. Этот белок, наряду с другими клеточными и вирусными белками, активирует транскрипцию с использованием длинных концевых повторов генома ВИЧ в качестве промоторов. Белок Vpr играет важную роль в переносе вирусной ДНК в ядро и вызывает задержку деления клетки в периоде G2[115].
Vif[править | править код]
Белок Vif играет важную роль в поддержке репликации вируса. Vif индуцирует убиквитинилирование и деградацию клеточного антивирусного белка APOBEC3G, который вызывает деаминирование ДНК, приводящее к мутационным заменам G на A в вирусной ДНК, синтезируемой в ходе обратной транскрипции. Штаммы, лишённые Vif, не реплицируются в CD4+-лимфоцитах, некоторых линиях T-лимфоцитов и макрофагах. Эти штаммы способны проникать в клетки-мишени и начинать обратную транскрипцию, однако синтез вирусной ДНК остаётся незавершённым[115].
Nef[править | править код]
Белок Nef выполняет несколько функций. Он подавляет экспрессию молекул CD4 и HLA классов I и II на поверхности инфицированных клеток, и тем самым позволяет вирусу ускользать от атаки цитотоксических T-лимфоцитов и от распознавания CD4+-лимфоцитами. Белок Nef может также угнетать активацию T-лимфоцитов, связывая различные белки-компоненты систем внутриклеточной передачи сигнала[115].
У инфицированных вирусом иммунодефицита макак-резусов активная репликация вируса и прогрессирование болезни возможны только при интактном гене nef. Делеции гена nef были обнаружены в штаммах ВИЧ, выделенных у группы австралийцев с длительным непрогрессирующим течением инфекции[116]. Однако у части из них со временем появились признаки прогрессирования инфекции, в том числе снижение числа CD4+-лимфоцитов. Таким образом, хотя делеции гена nef и могут замедлять репликацию вируса, это не гарантирует полной невозможности прогрессирования заболевания[117].
Tat и Rev[править | править код]
Регуляторные белки Tat (транс-активатор) и Rev накапливаются в ядре клетки и связывают определённые участки вирусной РНК. Белок Tat имеет молекулярную массу около 14-15 кДа, связывает вторичную структуру геномной РНК вблизи 5′-нетранслируемой области[115][118], активирует обратную транскрипцию геномной РНК ВИЧ, синтез вирусных мРНК, необходим для репликации вируса почти во всех культурах клеток, регулирует выход вирионов из заражённых клеток[115][118], нуждается в клеточном кофакторе — циклине T1. Белок Rev регулирует экспрессию белков вириона, связывает мРНК гена env в области RRE (англ. Rev response element) интрона, разделяющего экзоны генов Tat и Rev[115][118].
Белки Tat и Rev стимулируют транскрипцию провирусной ДНК и транспорт РНК из ядра в цитоплазму, а также необходимы для трансляции. Белок Rev обеспечива
📒 История болезни ВИЧ | Gepatit ABC
ВИЧ-инфекция печально известна человеку уже не первое десятилетие. Однако в сравнении с многими другими возбудителями инфекционных заболеваний вирус иммунодефицита человека возник относительно недавно. Его появление во всем мире посеяло настоящую панику во всем мире, так как в течение длительного времени от ВИЧ-инфекции не существовало лекарства, и заболевшие были обречены на мучительную смерть.
Но как появился ВИЧ и СПИД? Как эта болезнь распространилась во всем мире? Что именно вызвало всеобщую панику по поводу ВИЧ и СПИДа? Как появился в России ВИЧ? Когда было разработано первое лекарство от рассматриваемого заболевания? Чтобы ответить на каждый из этих вопросов, рассмотрим краткую история ВИЧ.
История болезни ВИЧ
История болезни ВИЧ начинается с ее возникновения и первых случаев заражения. В полной мере неизвестно, когда именно первый человек заразился вирусом иммунодефицита. Некоторые ученые предполагают, что ВИЧ передался человеку от обезьяны примерно в 1926 году, однако до середины 1930-х годов патоген себя никак не проявлял. Корни заболевания уходят в западную часть Африканского континента.
Первым пациентом, скончавшимся от ВИЧ и СПИДа, стал неизвестный мужчина из Конго. Больной умер в 1959 году. Ученые занялись подробным изучением его истории болезни уже после его смерти. Изучив образцы тканей погибшего, специалисты пришли к выводу, что причиной смерти стал неизвестный ранее вирус, который привел к полной деградации иммунной системы больного.
Таки образом, неизвестный мужчина из Конго сал первой зафиксированной жертвой нового заболевания — СПИДа. На тот момент пути передачи и другие особенности инфекционной болезни не были известны, поэтому результаты исследования врачей в Африке в течение длительного времени не разглашались.
Эпидемия заболевания

Скорость распространения ВИЧ на территории африканского континента остается неизвестной. Первые зафиксированные случаи данной болезни в США были выявлены у проституток в 1969 году. Врачи не сразу обратили внимание на необычное заболевание, ошибочно приняв его за атипичную форму пневмонии.
Чуть позднее, в 1978 году, новый вирус были обнаружен в крови группы гомосексуалистов из США и Швеции, а также у некоторых гетеросексуальных мужчин на Гаити и в Танзании. Однако лишь в 1981 году Центр по Контролю и Профилактике Болезней (CDC) уведомил общественность о том, что у молодых гомосексуалистов из Нью-Йорка и Лос-Анджелеса выявлена новая болезнь.
5 июня того же года ученый из озвученного выше центра, Майкл Готлиб, впервые в истории описал новую болезнь, акцентируя ее губительное влияние на иммунитет пациента. В 1982 году заболевание, провоцируемое вирусом ВИЧ, получило официальное название Aquired Immune Deficience Syndrom (AIDS) – синдром приобретенного иммунодефицита (СПИД).
Тем временем, число заболевших постепенно росло. Болезнь попала в Европу и стала там стремительно распространяться. К концу 20-го века ВИЧ-инфекция по праву стала называться «чумой 20-го века».
Всеобщая паника
Специалисты к концу 80-х годов прошлого века выявили в США примерно 440 носителей вируса ВИЧ, из которых умерло около 200. По случайному совпадению большинство этих людей оказалось гомосексуалистами. Это спровоцировало новую волну гомофобии, а новое заболевание получило названия «гомосексуальный рак» и «чума, передаваемая гомосексуалистами».
В США было выявлено около 440 носителей вируса ВИЧ. Около 200 из этих людей умерли. Так как большинство больных были гомосексуалистами, новая болезнь получила название «Иммунодефицит, передаваемый гомосексуалистами» (Gay Related Immuno Deficiency – GRID) или «Гомосексуальный рак» (A Gay Cancer).
Из-за страха перед болезнью и недостаточной осведомленности о ее течении и способах передачи, начались настоящие гонения ВИЧ-положительных людей. С ними отказывались идти на контакт, им отказывали в оказании медицинской помощи. Конец этой темной полосе в краткой истории ВИЧ положило массовое просвещение населения по поводу особенностей данной болезни.
Как появился в России ВИЧ?

Итак, как появился ВИЧ и СПИД в мире примерно известно. Болезнь впервые обнаружилась в Африке, а затем распространилась в США и Европе. Но как появился в России ВИЧ? До середины 1980-х годов на территории СССР о ВИЧ знали очень мало. Болезнь пренебрежительно называли «капиталистической заразой».
Было принято считать, что болеют ею только проститутки и наркоманы. Еще в 1986 году в программе «Время» министр здравоохранения утверждал, что «СПИД — это болезнь Запада». Но уже в 1988 году в СССР было зафиксировано около 30 случаев заражения, и количество заболевших начало неуклонно расти.
Как же появилась на территории тогда еще СССР такая «западная болезнь», как ВИЧ-инфекция? Предполагается, что причиной заражения стали незащищенные сексуальные контакты между советской молодежью и зарубежными студентами. Так как Минздрав СССР долго не хотел признавать опасность «западной болезни», распространению ВИЧ в РФ это пренебрежительное отношение, а также использование нестерильных шприцев, лишь способствовало.
Когда разработали первое лекарство?
Директор Института вирусологии человека Мэрилендского университета доктор Роберт Галло 24 апреля 1984 года объявил об обнаружении причины новой инфекции — вирус из семейства ретровирусов. В 1987 годе Всемирная Организация Здравоохранения (ВОЗ) утвердила известное многим в наше время название возбудителя болезни – «вирус иммунодефицита человека» (ВИЧ, или в английской аббревиатуре HIV).
В этом же году была утверждена глобальная программа ВОЗ по ВИЧ и СПИДу. Началась разработка вакцины и лекарства от смертельно опасного недуга. Разработчики вакцины поначалу потерпели неудачу, так как патоген склонен к мутации и имеет нестабильную генетическую формулу. С разработкой лекарства дела обстояли несколько лучше, и уже в конце 1987 года в оборот внедряется первый препарат для терапии ВИЧ – Азидотимидин (Зидовудин, Ретровир).
История болезни ВИЧ на этом не заканчивается. В настоящее время это заболевание все еще можно отнести к неизлечимым, однако инновационные препараты способствуют снижению вирусной активности и купированию риска перехода в стадию синдрома приобретенного иммунодефицита (СПИДа). Разработка вакцины от ВИЧ-инфекции все еще в процессе.
Оцените статью:
| Всего голосов: 1 Средняя оценка: 5СПИД: история возникновения, распространение, симптомы. Справка
Некоторые ученые считают, что вирус ВИЧ был передан от обезьян к человеку примерно в 1926 году. Последние исследования показывают, что человек приобрел этот вирус в Западной Африке. До 1930-х годов вирус никак не проявлял себя. В1959 году в Конго умер мужчина.Позднейшие исследования медиков, проанализировавших его историю болезни, показали, что, возможно, это был первый зафиксированный в мире случай смерти от СПИДа. В 1969 году в США среди проституток были зафиксированы первые случаи болезни, протекавшей с симптомами СПИДа. Тогда медики не обратили на них особого внимания, посчитав редкой формой пневмонии. В 1978 году у гомосексуалистов в США и Швеции, а также среди гетеросексуальных мужчин в Танзании и на Гаити были обнаружены симптомы одного и того же заболевания.
И только в 1981 году Центр по контролю и профилактике болезней (CDC) сообщил о выявлении у молодых гомосексуалистов в Лос-Анджелесе и Нью-Йорке новой болезни. В США было выявлено около 440 носителей вируса ВИЧ. Около 200 из этих людей умерли. Так как большинство больных были гомосексуалистами, новая болезнь получила название «Иммунодефицит, передаваемый гомосексуалистами» (Gay Related Immuno Deficiency – GRID) или «Гомосексуальный рак» (A Gay Cancer).
5 июня 1981 года американский ученый из Центра по контролю над заболеваниями Майкл Готлиб впервые описал новое заболевание, протекающее с глубоким поражением иммунной системы. Тщательный анализ привел американских исследователей к выводу о наличии неизвестного ранее синдрома, получившего в 1982 году название Aquired Immune Deficience Syndrom (AIDS) – синдром приобретенного иммунодефицита (СПИД). Тогда же СПИД назвали болезнью четырех «Н», по заглавным буквам английских слов — гомосексуалисты, больные гемофилией, гаитяне и героин, выделив этим самым группы риска для новой болезни.
Иммунный дефицит (снижение иммунитета), от которого страдали заболевшие СПИДом, ранее встречался только как врожденный порок недоношенных новорожденных детей. Врачи установили, что у этих больных снижение иммунитета не было врожденным, но было приобретено в зрелом возрасте.
В 1983 году французским ученым Монтанье была установлена вирусная природа болезни. Он обнаружил в удаленном у больного СПИДом лимфатическом узле вирус, назвав его LAV (lymphadenopathy associated virus).
24 апреля 1984 года директор Института вирусологии человека Мэрилендского университета доктор Роберт Галло объявил о том, что он нашел истинную причину СПИДа. Ему удалось выделить вирус из периферической крови больных СПИДом. Он изолировал ретровирус, получивший название HTLV-III (Human T-lymphotropic virus type III). Эти два вируса оказались идентичными.
В 1985 году было установлено, что ВИЧ передается через жидкие среды тела: кровь, сперму, материнское молоко. В том же году был разработан первый тест на ВИЧ, на основе которого в США и Японии начали проверять на ВИЧ донорскую кровь и ее препараты.
В 1986 году группа Монтанье объявила об открытии нового вируса, который получил название HIV-2 (ВИЧ-2). Сравнительное изучение геномов ВИЧ-1 и ВИЧ-2 показало, что в эволюционном плане ВИЧ-2 далеко отстоит от ВИЧ-1. Авторы высказали предположение, что оба вируса существовали задолго до возникновения современной эпидемии СПИДа. ВИЧ-2 был впервые выделен в 1985 году от больных СПИДом в Гвинее-Бисау и Островах Зеленого Мыса. Исследования показали, что обусловленные ВИЧ-2 и ВИЧ-1 заболевания являются самостоятельными инфекциями, так как имеются различия в особенностях возбудителей, клинике и эпидемиологии.
В 1987 году Всемирная Организация Здравоохранения утвердила название возбудителя СПИД – «вирус иммунодефицита человека» (ВИЧ, или в английской аббревиатуре HIV).
В 1987 году была учреждена Глобальная программа ВОЗ по СПИДу, а Всемирной ассамблеей здравоохранения принята глобальная стратегия борьбы со СПИДом. В этом же году в ряде стран внедряется в лечение больных первый противовирусный препарат – азидотимидин (зидовудин, ретровир).
Необходимо подчеркнуть, что ВИЧ и СПИД не синонимы. СПИД – понятие более широкое и означает дефицит иммунитета. Такое состояние может возникнуть в результате самых различных причин: при хронических истощающих заболеваниях, воздействии лучевой энергии, у детей с дефектами иммунной системы и у больных старческого возраста с инволюцией иммунной защиты, некоторых медикаментозных и гормональных препаратов. В настоящее время название СПИД применяется для обозначения только одной из стадий ВИЧ-инфекции, а именно манифестной ее стадии.
ВИЧ-инфекция — новое инфекционное заболевание, называвшееся до открытия ее возбудителя как синдром приобретенного иммунодефицита (СПИД). ВИЧ-инфекция — прогрессирующее антропонозное инфекционное заболевание, с кровоконтактным механизмом заражения, характеризующееся специфическим поражением иммунной системы с развитием тяжелого иммунодефицита, который проявляется вторичными инфекциями, злокачественными новообразованиями и аутоиммунными процессами.
Источником ВИЧ-инфекции является больной СПИДом человек или бессимптомный вирусоноситель. Основной механизм передачи инфекции – кровоконтактный. Болезнь передается при половых контактах, особенно гомосексуальных; от инфицированной матери к ребенку в период беременности через плаценту, во время родов, при грудном вскармливании от матери к плоду; через бритвенные приборы и другие колюще-режущие предметы, зубные щетки и т. п. Эпидемиологи ВИЧ не допускают существования воздушно-капельного и фекально-орального путей передачи, так как выделение ВИЧ с мокротой, мочой и калом весьма незначительно, а также незначительно и число восприимчивых клеток в желудочно-кишечном тракте и дыхательных путях.
Существует и искусственный путь передачи: при лечебно-диагностических манипуляциях путем проникновения вируса через поврежденную кожу, слизистые оболочки (транс¬фузии крови и ее препаратов, трансплантации органов и тканей, инъекции, операции, эндоскопические процедуры и т. п.), искусственном оплодотворении, при внутривенном введении наркотических веществ, выполнении различного рода татуировок.
В группу риска входят: пассивные гомосексуалисты и проститутки, у которых более вероятны повреждения слизистых оболочек в виде микротрещин. Среди женщин основную группу риска составляют наркоманки, вводящие наркотики внутривенно. Среди больных детей 4/5 составляют дети, матери которых больны СПИДом, инфицированы ВИЧ или принадлежат к известным группам риска. Второе по частоте место занимают дети, которым производили гемотрансфузии, третье – больные гемофилией, медицинский персонал, имеющий профессиональный контакт с кровью и другими биологическими жидкостями ВИЧ-инфицированных пациентов.
Вирус иммунодефицита может существовать в организме человека в течение десяти – двенадцати лет, никак себя не проявляя. А на начальные признаки его проявления многие люди не обращают должного внимания, принимая их за симптомы других, на первый взгляд не опасных заболеваний. Если вовремя не начать процесс лечения, наступает конечная стадия ВИЧ – СПИД. Вирус иммунодефицита может стать базой для развития других болезней, носящих инфекционный характер. Наряду с риском развития СПИДа повышается и риск появления других инфекционных заболеваний.
Симптомы
Лихорадка более 1 месяца, диарея более 1 месяца, необъяснимая потеря массы тела на 10% и более, пневмонии затяжные, рецидивирующие или не поддающиеся стандартной терапии, постоянный кашель более 1 месяца, затяжные, рецидивирующие вирусные, бактериальные, паразитарные болезни, сепсис, увеличение лимфоузлов двух и более групп свыше 1 месяца, подострый энцефалит, слабоумие у ранее здоровых людей.
Последняя стадия – СПИД – протекает в трех клинических формах: онко-СПИД, нейро-СПИД и инфекто-СПИД. Онко-СПИД проявляется саркомой Капоши и лимфомой головного мозга. Нейро-СПИД характеризуется разнообразными поражениями ЦНС и периферических нервов. Что касается инфекто-СПИДа, то он проявляется многочисленными инфекциями.
При переходе ВИЧ в заключающую стадию — СПИД — симптомы заболевания становятся более явными. Человека все чаще и чаще начинают поражать различные заболевания, такие как пневмония, туберкулез легких, вирус герпеса и другие заболевания, получившие название оппортунистические инфекции. Именно они и ведут к самым тяжелым последствиям. В это время вирус иммунодефицита становится тяжелейшим заболеванием. Бывает, что состояние больного настолько тяжелое, что человек даже не в состоянии вставать с постели. Такие люди чаще всего даже не подлежат госпитализации, а находятся дома под присмотром близких им людей.
Диагностика
Основным методом лабораторной диагностики ВИЧ-инфекции является обнаружение антител к вирусу с помощью иммуноферментного анализа.
Лечение
На современном этапе развития медицины лекарства, способного полностью вылечить это заболевание, не существует. Однако, при своевременном начале лечения ВИЧ можно надолго отодвинуть момент перехода вируса иммунодефицита в развитие СПИДа, а следовательно и продлить более-менее нормальную жизнь больному.
Уже разработаны схемы лечения, которые могут существенно замедлить развитие заболевания, а так как инфекция протекает в большинстве случаев длительно, то можно надеяться на создание за это время эффективных лечебных средств.
История болезни вич инфекция 4 стадии – ВИЧ и СПИД
Паспортные данные
Возраст: 25 лет
Профессия, место работы: офис-менеджер, «Агенство прямых инвестиций»
Время поступления в клинику: 18. 02. 2007
Предварительный диагноз: ВИЧ-инфекция IVВ (потеря в весе более 10%, двусторонняя пневмоцистная пневмония, орофарингеальный кандидоз.)
Осложнения основного заболевания: ДН II.
Сопутствующие заболевания: Хронический вирусный гепатит С в фазе ремиссии.
Дата курации: 9. 03. 2007 (85-й день болезни)
Окончательный диагноз: ВИЧ-инфекция, IVВ (Потеря массы тела более 10%. Двусторонняя полисегментарная пневмония смешанной этиологии: цитомегаловирус, пневмоциста, микоплазма. Орофарингеальный кандидоз).
Осложнения основного заболевания: ДН II.
Сопутствующие: Хронический вирусный гепатит С в фазе ремиссии. Желчекаменная болезнь. Хронический бронхит вне обострения.
Жалобы на момент осмотра:
на слабость, одышку инспираторного характера в покое и при физической нагрузке, кашель с трудноотделяемой мокротой слизистого характера, боли в грудной клетке при глубоком вдохе.
История заболевания:
Примерно с середины декабря отмечает появление слабости, одышки при физической нагрузке, через некоторое время присоединился сухой мучительный кашель. Отмечает снижение аппетита, подъем температуры до 38 С. Обратилась за медицинской помощью в районную поликлинику, где были назначены лазолван и макропен. Принимала указанные лекарственные средства без эффекта. Самостоятельно принимала аспирин для снижения температуры. Больный лист не оформляла. Примерно с середины февраля отмечает ухудшение состояния, при кашле появилась трудноотделяемая мокрота слизистого характера, температура повышалась до 40 оС в вечернее время, одышка стала появляться в покое. За прошедший период отмечает значительную потерю в весе (более 10%). Продолжала принимать аспирин.
18. 02. 2007 в связи с ухудшением состояния вызвала «03», была госпитализирована в КИБ № 2 с диагнозом «ВИЧ-инфекция, двусторонняя пневмония».
Эпидемиологический анамнез:
Источник водоснабжения централизованный
Канализация централизованная
Грызуны дома и на работе- нет.
Контакт с домашними животными — есть домашняя кошка.
В открытых водоемах не купалась, воду из них не пила.
В стационаре не лечилась
Посещение стоматолога отрицает.
С 16-летнего возраста (с 1998 г.) принимала внутривенно героин. Первый половой партнер ВИЧ-инфицированный. В 2000 году перестала употреблять наркотические вещества. Анализ крови на Анти- HIV и Анти-НСV не сдавала. В 2001 году забеременела, при сдаче анализов крови в женской консультации обнаружены Анти- HIV, положительная реакция иммуноблоттинга и Анти-НСV. Поставлена на учет в МГЦ СПИД. В течение всего срока беременности проходила химиопрофилактику. Роды посредством кесарева сечения. Ребенок здоров, последний раз обследован в возрасте 3,5 лет. После рождения ребенка, с 2002 г., в МГЦ СПИД не обращалась, иммунный профиль не проверяла, антиретровирусную терапию не принимала.
История жизни:
Родилась 19. 09. 1981 года в г. Москва, в росте и развитии от сверстников не отставала. В детстве перенесла ветряную оспу. Работает офис-менеджером.
Семейный анамнез: замужем 2-ой раз: первый муж — ВИЧ-инфицированный, второй — здоров, ребенок 5 лет — здоров.
Наследственность: не отягощена
Пищевой анамнез: питается регулярно и разнообразно, предпочтений в еде нет.
Аллергологический анамнез: аллергических реакций на лекарственные препараты, пищевые продукты, запахи не отмечает.
Вредные привычки: курит по 1 пачке сигарет в день. В анамнезе употребление наркотических средств (героин внутривенно) в течение 1 года (с 2000 по 2001 г.). Со слов больной перестала употреблять наркотики, когда узнала о беременности.
Хронические заболевания: ВИЧ-инфекция и ХВГ С, обнаруженные в 2001 году. Туберкулез, сифилис, травмы отрицает.
Гинекологический анамнез: менструация с 11 лет, регулярные, безболезненные. Половая жизнь с 14 лет. Беременностей — 4; родов — 1, без осложнений; аборты -3, самопроизвольный-1.
Общий осмотр
Общее состояние больного: средней тяжести
Сознание: ясное.
Положение больного: активное.
Телосложение: правильное, конституция нормостеническая.
Рост: 170 см. Масса: 70 кг.
Температура: 36,6 ° С.
Осанка: правильная
Походка: твердая, уверенная.
При осмотре лица выражение его спокойное, патологические маски отсутствует, деформации носа и асимметричности носогубной складки нет, отмечается цианоз губ.
При осмотре глаз и век склеры и конъюнктивы бледно-розовые, иктеричности нет. Форма зрачка правильная, реакция на свет сохранена.
Изменений формы головы и шеи нет, искривления и деформации, пульсация сонных артерий и яремных вен отсутствуют.
Кожные покровы бледные, отмечается акроцианоз, влажность кожи умеренная, тургор сохранен. Варикозных расширений вен не отмечается. На коже передней стенки живота папулезная сыпь, следы от расчесов.
Состояние волосяного покрова соответствует полу и возрасту.
Состояние ногтей: не деформированы, ломкость и исчерченность отсутствуют. При осмотре видимых слизистых на слизистой ротовой полости отмечается творожистый налет. Язык без налета, умеренно влажный, сосочковый рисунок умеренно выражен. Конъюнктивы и склеры бледно-розовые, без патологических элементов, сосудистый рисунок умеренно выражен. Подкожная клетчатка развита умеренно (толщина складки на уровне пупка 2,5 см, на уровне угла лопатки — 3 см), распределена равномерно, пастозность и отеки отсутствуют.
Лимфатические узлы: Пальпируются шейные и надключичные лимфоузлы. Размеры около 1 см, мягкоэластической консистенции, безболезненны, не спаяны между собой и с окружающими тканями. Другие группы лимфоузлов не пальпируются. Мышцы развиты достаточно, тонус и сила симметричных групп мышц одинаковы, атрофии и гипертрофии каких-либо мышц не выявлено, болезненность при пальпации отсутствует. Кости правильной формы, без деформаций, при пальпации и перкуссии болезненности нет. Концевые фаланги пальцев рук и ног без изменений. Суставы правильной конфигурации, припухлость отсутствует, при ощупывании безболезненны, температура над суставами соответствует температуре окружающих кожных покровов. Активные и пассивные движения сохранены в полном объеме, хруст при движениях отсутствует.
Исследование органов дыхания
Осмотр:
Правильная форма грудной клетки, нормостенического типа. Подключичные и надключичные ямки умеренно выражены. Межреберные промежутки умеренно выражены, эпигастральный угол прямой, лопатки и ключицы умеренно выступают
дыхательные экскурсии обеих половин грудной клетки симметричны. Обе половины грудной клетки симметричны и участвуют в дыхании. Искривления позвоночника отсутствуют. Дыхание через нос, ритмичное, выражена одышка. ЧДД — 26 в минуту, дыхание средней глубины.
При пальпации болезненность отсутствует. Грудная клетка ригидная, голосовое дрожание одинаковое над симметричными участками легких.
Перкуссия
Над нижними отделами обоих легких перкуторный звук тупой, над верхними отделами -притуплено-тимпанический.
вирусный гепатит сердечный кровь
Таблица. Топографическая перкуссия
Верхняя граница легких | Справа | Слева | ||
Высота стояния верхушки спереди | 3 см вверх от ключицы | 4 см вверх от ключицы | ||
Высота стояния верхушки сзади Ширина полей Кренига | Уровень остистого отростка СVII 7 см | Уровень остистого отростка СVII 7 см | ||
Нижняя граница легких | По окологрудинной линии | V межреберье | – | |
По средне ключичной линии | VI ребро | – | ||
По передней подмышечной линии | VII ребро | VII ребро | ||
По средней подмышечной линии | VIII ребро | VIII ребро | ||
По задней подмышечной линии | IX ребро | IX ребро | ||
По лопаточной линии | X ребро | X ребро | ||
По околопозвоночной линии | Ост. отр ThXI | Ост. отр ThXI | ||
Дыхательная экскурсия нижнего края легких по средней подмышечной линии | 5 см | 5,5 см | ||
Аускультация легких
В области надключичных ямок, 1−3-го межреберий спереди и сзади в надостных ямках выслушивается везикулярное дыхание, в нижнебоковых отделах обоих легких ослабленное везикулярное дыхание и выслушиваются хрипы. В левом легком в нижнебоковых отделах влажные крупнопузырчатые хрипы, в верхних отделах единичные сухие хрипы, в правом в аналогичных отделах мелкопузырчатые влажные хрипы. Шум трения плевры отсутствует. Бронхофония одинакова над симметричными участками легких.
Исследование сердечно-сосудистой системы
Осмотр
Сердечный горб, сердечный толчок, пульсация во II межреберье у правого и у левого края грудины, пульсация в эпигастральной области, прекардиальная пульсация, пульсация сонных артерий, положительный венный пульс (пульсация яремных вен) и набухание шейных вен не наблюдается. Верхушечный толчок не виден. Варикозного расширения вен в области грудины нет.
Пальпация
Верхушечный толчок локализован в 5-ом межреберье на 1 см кнутри от среднеключичной линии, ширина 2,5 см, средней силы, невысокий, резистентный.
Сердечный толчок не пальпируется, симптома «кошачьего мурлыканья» не наблюдается.
Перкуссия
Границы относительной тупости сердца:
Правая — 1,5 см кнаружи от правого края грудины на уровне 4-го межреберья
Левая — 1 см кнаружи от левой среднеключичной линии в 5-ом межреберье
Верхняя — верхний край 3-го ребра у левого края грудины
Поперечник сердца — 12 см
Ширина сосудистого пучка — 5 см
Границы абсолютной тупости сердца:
правая граница абсолютной тупости сердца — по левому краю
грудины в 4-ом межреберье
левая граница абсолютной тупости сердца — совпадает с левой границей относительной тупости.
верхняя граница абсолютной тупости сердца — по верхнему краю 4-го ребра у левого края грудины
Аускультация
Аускультация сердца в 1-й точке: первый тон совпадает с пульсовым толчком сонной артерии, громче второго примерно в 2 раза.
Аускультация сердца во 2-й точке: второй тон громче первого примерно в 2 раза.
Аускультация сердца во 3-й точке: второй тон громче первого примерно в 2 раза.
Аускультация сердца в 4-й точке: первый тон совпадает с пульсовым толчком сонной артерии, громче второго примерно в 2 раза.
Аускультация сердца в 5-й точке: I и II тоны по громкости примерно равны друг другу.
Шумов не выслушивается.
Исследование сосудов
При осмотре и пальпации артерий отмечается эластичность стенки, извитость артерий отсутствует. Пульсация аорты в яремной ямке не наблюдается. На сонных и бедренных артериях шумов не выслушивается.
Пульс синхронный и одинаковый на обеих руках, ритмичный, ЧСС- 104 удара в минуту, АД -110/70 мм рт. ст., умеренного напряжения и наполнения, равномерный, дефицита пульса нет.
Расширения вен грудной клетки, брюшной стенки и конечностей нет. Уплотнений и болезненности вен не обнаружено.
Исследование органов пищеварения. Осмотр
Полость рта:
Кариозных и вставных зубов нет. Язык без налетов, умеренно влажный, сосочковый слой умеренно выражен, трещин и язв нет.
Десны бледно-розовые, без налета и патологических изменений.
Небные миндалины не увеличены, бледно-розовые, без налетов и пленок.
На слизистой щек творожистый налет.
При осмотре живота отмечается его правильная форма, симметричность обеих половин, участвует в дыхании, видимой перистальтики нет, венозных коллатералей не обнаружено. Отмечается папулезная сливного характера сыпь на передней брюшной стенке. Пупок втянут. Грыжевых выпячиваний нет.
Перкуссия:
Над всей поверхностью живота слышится тимпанический перкуторный звук,
Притупление в отлогих местах живота отсутствует.
Поверхностная ориентировочная пальпация:
Живот мягкий, безболезненный, расхождение прямых мышц живота, грыжи и перитонеальные симптомы отсутствуют. Опухолевых образований нет.
Аускультация живота:
По всей поверхности живота выслушиваются нормальные кишечные шумы. Шум трения брюшины отсутствует. Сосудистых шумов не выслушивается.
Глубокая пальпация:
Сигмовидная кишка пальпируется в виде безболезненного плотного гладкого цилиндра, не урчит под рукой. Слепая кишка пальпируется в виде безболезненного мягко-эластического цилиндра, урчит под рукой, обладает умеренной подвижностью.
При пальпации поперечно-ободочной, восходящего и нисходящего отделов толстого кишечника ощущается мягкий с гладкой поверхностью, безболезненный цилиндр. Большую кривизну желудка не пальпируется {27, ‘www.sinp.com.ua’}.
Исследование печени
Осмотр
Выпячивания правого подреберья и подложечной области и ограничения указанных областей в дыхании нет. Пульсации брюшной стенки в области правого подреберья нет. Венозного рисунка на брюшной стенке нет.
Перкуссия
Верхняя граница абсолютной тупости — 6 ребро по правой среднеключичной линии
Нижняя граница абсолютной тупости
По правой среднеключичной линии — ннна 1,5 см ниже реберной дуги
По передней срединной линии — на 4 см выше пупка
По левой реберной дуге — 7 ребро
Размеры печени по Курлову:
По правой среднеключичной линии — 10 см
По передней срединной линии — 8 см
По левой реберной дуге — 7 см
Пальпация
Нижний край печени острый, мягкий, безболезненный, гладкий.
Исследование желчного пузыря
Пальпация
Желчный пузырь не пальпируется.
Симптомы Захарьина, Василенко, Ортнера, Кера, Мерфи, Мюсси отрицательные.
Исследование селезенки
При осмотре выпячивания в области левого подреберья нет.
При перкуссии размеры селезенки:
Длинник — 12 см
Поперечник — 5 см
Не пальпируется
Исследование почек
При осмотре выпячивания в поясничной области нет. Половины поясничной области симметричны. Дизурических расстройств не выявлено.
Симптом поколачивания отрицательный с обеих сторон.
ПАЛЬПАЦИЯ
Почки не пальпируются.
Исследование мочевого пузыря
Выбухания над лобковой областью нет.
Мочевой пузырь не пальпируется.
Предварительный клинический диагноз и его обоснование:
ВИЧ-инфекция IVВ (потеря в весе более 10%, двусторонняя пневмоцистная пневмония, орофарингеальный кандидоз.)
Осложнения основного заболевания: ДН II.
Сопутствующие заболевания: Хронический вирусный гепатит С в фазе ремиссии.
Диагноз поставлен на основании данных анамнеза (внутривенное употребление героина в период с 1998 по 2000 год) и выявлении при обследовании в 2001 году антител к ВИЧ. На основании данных анамнеза (постепенное начало, наличие сухого кашля, а затем с трудноотделяемой слизистой мокротой, подъем температуры до цифр 38 С, слабость, утомляемость снижение аппетита на протяжении около 2,5 месяцев), осмотра (цианоз губ и периферических отделов конечностей, одышка в покое), объективного обследования (ослабленное дыхание в легких и наличие разнокалиберных влажных хрипов в нижнебоковых отделах обоих легких, единичных сухих хрипов в верхних отделах) сделано заключение о наличии двусторонней пневмонии. Учитывая давность ВИЧ-инфекции (не менее 6 лет), развитие легочной патологии, связанной, скорее всего, с наличием оппортунистического заболевания (предположительно пневмоцистная пневмония), а также развитие кандидоза слизистой оболочки полости рта (творожистый налет на слизистой) и значительную потерю весу за период от начала заболевания, можно думать о стадии вторичных проявлений IVВ ВИЧ-инфекции. Учитывая выраженность одышки (не только при физической нагрузке, но и в покое), данные осмотра (периферический цианоз) правомочен диагноз дыхательной недостаточности II степени.
Диагноз хронического вирусного гепатита С поставлен на основании данных анамнеза (со слов больной при обследовании в 2001 году были также обнаружены Анти-HCV).
План обследования:
Общий анализ крови
Общий анализ мочи
Биохимический анализ крови
Коагулограмма
Исследование КОС
Рентгенологическое исследование органов грудной клетки
УЗИ органов брюшной полости
ЭхоКГ
Исследование крови на ВИЧ и гепатит В, С (HBsAg, анти HCV, анти HIV)
Бронхофиброскопия
Кровь на вирусную нагрузку (РНК ВИЧ)
Иммунный статус
RW
ЭКГ
Мазок из носоглотки на менингококк
Термометрия
Данные инструментальных и лабораторных исследований:
1. Клинический анализ крови от 18. 02. 07
Hb 128 г/л
Лейкоциты 13,5*10 в 9/л
Палочкоядерные 19%
Сегментоядерные 55%
Лимфоциты 19%
Моноциты 7%
СОЭ 10 мм/час
От 20. 02. 07
Эритроциты — 4,55*10 в 12/л
Гемоглобин — 11 г/л
Гематокрит — 0,365
Лейкоциты — 5,9*10 в 9/л
Гранулоциты — 65,8%
Лимфоциты — 26,4%
Моноциты — 7,8%
Тромбоциты — 178*10 в 9/л
от 2. 03. 2007
Эритроциты — 3,89*10 в 12
Hb 102 г/л
Гематокрит 0,280 (норма 0,34−0,48)
Лейкоциты 11*10 в 9/л
Палочкоядерные 1%
Гранулоциты88,3%
Лимфоциты 8,3%
Моноциты 3. 4%
Тромбоциты — 342*10 в 9/л
СОЭ 40 мм/ч
Общий анализ мочи
цвет светло-желтый, прозрачная,
относительная плотность — 1018 ,
среда — кислая
глюкозы — нет;
белок — 0,14 г/л
билирубин — отр
переходный эпителий — 7 в поле зрения,
лейкоциты — 0−1 в поле зрения.
. Биохимический анализ крови от 19. 02. 07
Общий белок 81 г/л
Мочевина 10,2 ммоль/л
Билирубин 10.1 мкмоль/л
Общ. холестерин 6,56 ммоль/л
АлАТ 38 МЕ
АсАТ 31 МЕ
глюкоза натощак 4,95 ммоль/л
Ca 1. 17 ммоль/л
Na 140 ммоль/л
K 3. 92 ммоль/л
Cl 4. 95 ммоль/л
Биохимический анализ крови от 2. 03. 07
Общий белок 79 г/л
Мочевина 6,4ммоль/л
Билирубин 11,8 мкмоль/л
АлАТ 51 МЕ
АсАТ 40 МЕ
глюкоза натощак 5,0 ммоль/л
Коагулограмма от 1. 03. 07
АЧТВ — 32,2 сек (26−36 сек)
ПТИ 93% (80−100%)
Тромбоцитарное время 17,4 сек (15−20 сек)
Фибриноген 4,2 г/л (2,5−4,5 г/л)
КОС от 1. 03. 07
рН — 7,391
рСО2 — 31,3 мм рт ст (N 32−45 mmHg)
рО2 — 20,8 мм рт ст (N 75−100 mmHg)
BE (ecf) — -6,4 ммоль/л
BE — -5,2 ммоль/л
Натрий — 140 ммоль/л
Калий — 3,92 ммоль/л
Кальций — 1,17 ммоль/л
О2 SAT — 34,6%
Рентгенологическое исследование органов грудной клетки:
От 19. 02. 07 — Легочный рисунок диффузно усилен по сосудистому типу и интерстицию. Снижение прозрачности легочной ткани в проекции базальных сегментов обоих легких. Затемнение средней интенсивности, негомогенно, без четких контуров. Корни легких малоструктурированы, не расширены. Диафрагма обычна. Тень сердца и аорты без особенностей. Заключение: при наличии клиники нельзя исключить двустороннюю нижнедолевую интерстициальную пневмонию.
От 27. 02. 07.- конец правого подключичного катетера проекционно в левой плечеголовной вене. Признаков пневмоторакса нет. Оба легочных поля субтотально затемнены (по типу «матового стекла») Легочный рисунок диффузно обогащен за счет интерстициального компонента и деформирован, прослеживаются множественные мелкие очаговые тени. Корни легких уплотнены, отечные, неструктурные. Левый синус затемнен. Диафрагма без особенностей. Талия сердца сглажена. Умеренное выбухание дуги легочного ствола. Заключение: двусторонняя субтотальная интерстициальная пневмония. По-видимому слабовыраженная гипертензия в МКК.
УЗИ органов брюшной полости:
Печень — толщина правой доли до 138 мм, левой доли до 68 мм, контур ровный, структура паренхимы без видимых очагов, диффузно изменена, эхогенность средней степени. Внутрипеченочные желчные протоки и холедох не расширены. Воротная вена 13 мм, селезеночная вена до 8 мм.
Желчный пузырь: 112*34 мм, форма овальная, стенка не утолщена, умеренно уплотнена. В просвете определяется мелкодисперстный осадок и множественные конкременты от 5 до 7 мм в диаметре, смещаемые, дающие акустическую тень.
Поджелудочная железа: 28*19*23 мм, контур ровный, структура мелкоточечная, эхогенность средней степени. Вирсунгов просток не расширен.
Селезенка: 136*45, контур ровный, структура без видимых очагов, диффузно изменена, эхогенность средней степени.
Почки расположены типично, правая 123*45 мм, левая — 121*47 мм, контур ровный, паренхима толщиной до 16−18 мм, дифференциация на слои сохранена, рисунок смазан, эхогенность коркового слоя средней степени. ЧЛС не расширена, конкременты не определяются.
Свободной жидкости и увеличенных лимфоузлов в брюшной полости не выявлено.
В плевральных синусах жидкостных участков не выявлено, контур плевры утолщен.
УЗИ органов брюшной полости (заключение): увеличение печени, диффузное изменения в паренхиме. Увеличение селезенки, диффузные изменения в паренхиме. Эхо признаки дискинезии желчного пузыря, множественные конкременты в желчном пузыре
ЭхоКГ: Полости сердца не расширены. Убедительных данных за наличие дополнительных наложений на створках клапанов не получено. Регургитация в полость левого предсердия дл II степени. Признаки умеренной гипертензии по показателям среднего систолического давления в легочной артерию глобальная сократимость миокарда удовлетворительная. Перикардиальная щель не расширена.
Исследование крови Гепатит и ВИЧ от 19. 02. 07
HBsAg — отриц.
Анти HCV — «+»
Анти HIV (ВИЧ) — ИФА «+»
Бронхофиброскопия от 5. 03. 07:
Местная анестезия с анемизацией. Нафтизин 0,1%. Лидокаин 10%. Лидокаин 4% – 12.0. Состояние тяжелое. Тахипноэ.
Фиброскоп «Олимпас» введен трансназально (через левый носовой ход). Гортань сформирована правильно, слизистая гладкая, блестящая, несколько застойная. Голосовые складки четкие, симметрично подвижны. Голосовая щель правильной формы, неширокая. В трахее просвет не изменен: рисунок хрящевых полуколец четкий, слизистая розовой окраски с несколько усиленным сосудистым рисунком и цианотичностью. Карина по центру, тонкая, высокая. В просвете бронхов с обеих сторон небольшое количество пенистого слизистого секрета. Проходимость бронхов не нарушена. Слизистая пастозна, со сглаженной складчатостью, обедненным сосудистым рисунком, розово-цианотичной окраски, блестящая. Устья бронхов правильной, округло-овальной формы, шпоры чуть утолщены. Тонус и эластичность тканей сохранены.
Взятие смывов секрета на анализы. Биопсия на ПЦР
Заключение: Признаки хронического билатерального эндобронхита
Иммунный статус от 20. 02. 07:
CD4 — 5%
CD8 — 77%
Анализ крови Реакция Вассермана от 19. 02. 07 — отрицательно
Электрокардиологическое исследование (заключение):
Ритм синусовый, 100 ударов в минуту. ЭОС нормальная. Изменений не выявлено.
Мазок из носоглотки на менигококк 22. 02. 07
Менингококк не выделен. Рост дрожжевых грибов рода Candida
Анализ кала на ВД от 5. 03. 07.
Палочек дизентерии и сальмонелл не выявлено.
анализ лаважной жидкости от 5.3. 07.
Цвет розовый. Водянистая, консистенция жидкая.
Лейкоцитов 19−30 в поле зрения
Эритроцитов 50 в поле зрения
Микобактерий туберкулеза не выявлено клетки с признаками атипизма не обнаружены. Рост грибов рода Candida.
Результаты ПЦР от 5. 03. 07 — обнаружен ЦМВ и микоплазмы.
Дневники наблюдения
28. 02. 07
Состояние средней степени тяжести. Температура тела — 39 С Жалобы на слабость, головную боль. ЧСС-100 ударов в минуту, АД 11//75 мм рт. ст., ЧДД — 34 в минуту. Тоны сердца ритмичные, ясные, шумов нет. В легких разнокалиберные влажные хрипы в нижнебоковых отделах и единичные сухие хрипы в верхних отделах, дыхание ослабленное везикулярное. Живот мягкий, безболезненный. Печень выступает на 2 см из-под края реберной дуги Стул и диурез без особенностей.
1. 03. 07
Состояние средней тяжести. Жалобы на слабость, одышку в покое. Температура тела 38,5 С. АД — 110/75 мм рт. ст., ЧСС — 100 в минуту, ЧДД — 32 в минуту. Тогны сердца ясные, ритмичные, шумов нет. В легких хрипы сохраняются. Живот мягкий безболезненный, диурез и стул без особенностей.
9. 03. 07
Жалобы на слабость, одышку при незначительной нагрузке и иногда в покое. Температура 36,8, снизилась на фоне назначения бисептола. ЧДД — 28 в минуту, АД — 100/70 мм. рт. ст. Тоны сердца ясные, ритмичные, шумов нет, ЧСС — 90 в минуту. В легких сохраняются влажные хрипы и ослабленное дыхание. Живот мягкий, безболезненный, стул и диурез адекватные.
Заключительный диагноз и его обоснование:
ВИЧ-инфекция, IVВ (Потеря массы тела более 10%. Двусторонняя полисегментарная пневмония смешанной этиологии: цитомегаловирус, пневмоциста, микоплазма. Орофарингеальный кандидоз).
Осложнения основного заболевания: ДН II.
Сопутствующие: Хронический вирусный гепатит С в фазе ремиссии. Желчекаменная болезнь. Хронический бронхит вне обострения.
На основании данных анамнеза (внутривенное употребление героина в период с 1998 по 2000 гг, половые контакты с ВИЧ-инфицированным партнером, и обнаружение при обследовании в 2001 г. антител к ВИЧ в реакциях ИФА и иммунного блоттинга), полученных результатов настоящего лабораторного исследования (обнаружены антитела к ВИЧ в реакциях ИФА и иммунного блоттинга и исследование иммунного статуса показало снижение количества CD4-лимфоцитов до 5%, что указывает на значительное снижение напряженности иммунитета) диагностирована ВИЧ-инфекция. Учитывая анамнестические данные (значительная потеря веса за период с середины декабря- более 10%), наличие двусторонней интерстициальной субтотальной пневмонии с характерной симптоматикой (постепенное развитие клиники, длительная лихорадка с цифрами до 38 С и наличие сухого кашля, ослабленное дыхание, наличие сухих хрипов в верхних отделах и разнокалиберных влажных хрипов в нижнебоковых отделах обоих легких), рентгенологической картиной (Оба легочных поля субтотально затемнены по типу «матового стекла». Легочный рисунок диффузно обогащен за счет интерстициального компонента и деформирован), подтвержденной лабораторно (обнаружение при проведении ПЦР цитомегаловируса и микоплазм), орофарингеальный кандидоз, длительность заболевания (более 6 лет), сделано заключение о наличии стадии вторичных заболеваний IVВ. Этиология пневмонии подтверждается результатами ПЦР (материал получен при проведении бронхофиброскопии): обнаружены цитомегаловирус и микоплазма; а также положительным ответом на терапию бисептолом. О наличии дыхательной недостаточности свидетельствует акроцианоз, одышка при незначительной физической нагрузке и в покое и показатели газового состава крови (гипоксемия, гипокапния и снижение сатурации О2).
Хронический вирусный гепатит С диагностирован на основании данных анамнеза (эпидемиологический анамнез: употребление героина внутривенно с 1998 по 2000 гг. И обнаружение при лабораторных исследованиях, проводимых в 2001 г., антител к вирусу гепатита С), данных лабораторных исследований при настоящей госпитализации — обнаружение анти HCV, увеличение размеров печени и незначительное увеличение размеров селезенки при объективном обследовании, наличие диффузных изменений печени и селезенки при УЗИ органов брюшной полости. Так как в большинстве случаев хронический гепатит С протекает бессимптомно, то приведенные данные позволяют поставить данный диагноз.
Желчекаменная болезнь поставлена на основании данных УЗИ (обнаружение множественных конкрементов в желчном пузыре)
Учитывая эндоскопическую картину бронхов и курение больной, можно предполагать наличие хронического бронхита.
Дифференциальный диагноз:
Дифференциальная диагностика интерстициальной пневмонии:
1. Аспергиллез легких — характеризуется постепенным началом, снижением аппетита и нарастанием слабости, повышением температуры субфебрильного характера, возможен сухой мучительный кашель. Но чаще основной симптом — сильный приступообразный кашель с выделением обильной мокроты кровянистого цвета, содержащей зеленоватые хлопья (скопления мицелия гриба) и прожилок крови. Иногда возникает кровохарканье. В крови — лейкоцитоз, эозинофилия. При бронхоскопии обнаруживают катарально-гнойное воспаление слизистой оболочки бронхов, в просвете сегментарных бронхов — рыхлые или плотные зеленовато-серые массы (скопление грибковых колоний).
Идиопатический фиброзирующий альвеолит — также характерно постепенное начало заболевания, одышка инспираторного характера и непродуктивный кашель, на Rg — симптом «матового стекла». Но болезнь прогрессирует довольно медленно, пациенты успевают адаптироваться к своей одышке, постепенно снижая свою активность и переходя к более пассивному образу жизни. Анамнез заболевания может составлять 1−3 года и практически никогда менее 3-х месяцев. Лихорадка менее характерна для ИФА. При обследовании выслушивается нежная крепитация в заднебазальных отделах уже на ранних стадиях, что является патогномоничным для данного вида пневмоний. На Rg диффузные мелкоочаговые изменения в обоих легких, в поздних стадиях возможна картина «сотового легкого» (фиброз с кистозной деформацией легочного рисунка). Наиболее информативна торакоскопическая биопсия легкого.
Экзогенные аллергические альвеолиты — хронические формы данной группы заболеваний сопровождаются длительной лихорадкой, слабостью, утомляемостью, прогрессирующей одышкой и сухим кашлем, развитием дыхательной недостаточности. Но в отличие от диагностированной пневмонии для данной группы заболеваний характерен специфический анамнез (профессиональный- фермеры, птицеводы, сыровары, работники химической, текстильной, деревообрабатывающей промышленности). В легких возможно выслушать как влажные, так и сухие свистящие хрипы и крепитацию. На Rg затемнения обычно бывают только в нижних долях. Характерен регресс симптоматики при прекращении воздействия антигена. При бронхоальвеолярном лаваже обнаруживают увеличение количества лимфоцитов и эозинофилов.
Бактериальные пневмонии, вызванные стрептококком, гемофильной палочкой — характерен астено-вегетативный синдром (слабость, потеря аапетита, утомляемость), одышка, лихорадка. Характеризуется более быстрым развитием, резким подъемом температуры и критическим ее падением при крупозной пневмонии. Очень характерна боль в грудной клетке (вовлечение плевры), кашель (вначале сухой) становится продуктивным уже на 3−4 день болезни, «ржавый» оттенок мокроты или гнойная мокрота. Объективное обследование достаточно информативно: усиление голосового дрожания при лобарной пневмонии и укорочение перкуторного звука, характерна крепитация в начале и в стадии разрешения болезни. В крови лейкоцитоз со сдвигом влево, иногда появление токсической зернистости нейтрофилов. На Rg при крупозной пневмонии изменения в пределах доли легкого (усиление рисунка, расширение корня, интенсивное затемнение на 2−3 дни болезни), при очаговой пневмонии видны очаговые тени небольших размеров. При проведении бронхоальвеолярного лаважа и анализах мокроты получают соответствующего возбудителя.
Гриппозная пневмония — заболевание развивается постепенно, вначале появляется сухой кашель, но через некоторое время он приобретает продуктивный характер, нередко с примесью крови. Общее состояние больного тяжелое, характерным клиническим признаком гриппозной пневмонии является выраженная интоксикация Жалобы на разбитость, головную боль, общую слабость, боль в грудной клетке при вдохе. Наблюдается кашель со слизисто-кровянистой мокротой и сильная боль в груди. Выраженные перкуторные изменения отсутствуют. Аускультативно в некоторых участках определяются мелкопузырчатые влажные хрипы. При рентгеноскопии отмечается гомогенная тень, распространяющаяся от корня легкого к периферии.
При исследовании крови определяют лейкопению, нейтрофилез со сдвигом влево, моноцитоз.
Лечение больного:
1. Режим палатный
2. Стол № 15
3. Бисептол-480, 4 таблетки*4раза перорально. Так как имеется подозрение на пневмоцистоз, целесообразно прибегнуть к терапии ex juvantibus.
4. Цимевен 5 мг/кг в/в в течение 21 дня — противовирусный препарат с действием на цитомегаловирус.
5. Макропен 400 мг*3 раза перорально — антибиотик, действующий на микоплазму.
6. Увлажненный кислород — для купирования симптомов дыхательной недостаточности, в частности для повышения сатурации крови кислородом и устранения гипоксемии.
7. Дифлюкан 50 мг*1 раз, перорально — противогрибковый препарат в связи с наличием кандидоза слизистой полости рта.
8. Sol/ Vit. В6 — 2,0 в/м — применяется при хронических гепатитах, участвует в обмене многих аминокислот, липидов.
9. Sol. Acidi Ascorbinici 5% 5.0 в/м 1 раз в день — применяется при заболеваниях печени.
10. Tabl. Bromhexini 2 таблетки*3раза в день — муколитическое, отхаркивающее средство в связи кашля с трудноотделяемой мокротой.
В связи с наличием ХВГ С целесообразно использование гепатопротекторов:
11. Тыквеол 15,0 *3 раза перорально курсами по 1−1.5 месяца 2−3 раза в год
12. Витамин Е 100 мг*1 раз перорально курсами по 1−1.5 месяца 2−3 раза в год
Учитывая стадию ВИЧ-инфекции 4 В с выраженными клиническими проявлениями и результаты обследования на иммунный статус после выписки из стационара необходимо консультация в МГЦ СПИД по поводу подбора схемы высокоинтенсивной противовирусной терапии
Список литературы
1. Учебник «Инфекционные болезни», Н. Д. Ющук, Ю. Я. Венгеров, «Медицина», 2003
2. Практическое методическое пособие «Инфекционные и паразитарные болезни», часть 4, под редакцией Н. Д. Ющука, 2006
3. Внутренние болезни, под редакцией Н. А. Мухина, В. С. Моисеева, А. И. Мартынова, «Гэотар-Медиа», 2006
4. Лекарственные средства, М. Д. Машковский, «Новая волна», 2004
Source: sinp.com.ua
Мы в соц.сетях:
Почитайте еще:
Синдром приобретённого иммунного дефицита — Википедия
Синдро́м приобретённого имму́нного дефици́та (СПИД) — состояние, развивающееся на фоне ВИЧ-инфекции[1][2][3] и характеризующееся падением числа CD4+ лимфоцитов, множественными оппортунистическими инфекциями, неинфекционными и опухолевыми заболеваниями[4][5]. СПИД является конечной стадией ВИЧ-инфекции. СПИД был впервые описан Центрами по контролю и профилактике заболеваний США в 1981 году, а его возбудитель, вирус иммунодефицита человека (ВИЧ), был описан в начале 1980-х годов[6].
День 1 декабря — Всемирный день борьбы со СПИДом, провозглашён ВОЗ в 1988 году[7].
- 1981 год 5 июня — сообщение Центров по контролю и профилактике болезней, США (англ. Centers for Disease Control and Prevention, CDC) о 5 случаях пневмоцистной пневмонии[8] и 28 случаях саркомы Капоши. Все заболевшие — мужчины, практиковавшие секс с мужчинами. Первая научная статья, которая признала особенности оппортунистических (условно-патогенных) инфекций, иллюстрирующих СПИД, была опубликована в 1981 году[9]. Болезнь получила название гей-связанного иммунодефицита (англ. Gay-related immune deficiency)[10]. Также болезнь получила название «болезни четырёх Г» (англ. 4-H disease), так как была обнаружена у жителей или гостей Гаити, гомосексуалов, гемофиликов и лиц, употреблявших героин (англ. Haiti, homosexual, hemophilia, heroine)[11]. После того как было показано, что СПИД не является заболеванием, эндемичным лишь для гомосексуалов[12], термин GRID был признан вводящим в заблуждение, и аббревиатура AIDS (СПИД) была введена в обращение на конференции в июле 1982 года[13]. В сентябре 1982 года CDC точно определили характеристики заболевания и начали употребление термина СПИД[12].
- 1983 год — вирус иммунодефицита человека независимо открыли в двух лабораториях: Институте Пастера во Франции под руководством Люка Монтанье и Национальном институте рака в США под руководством Роберта Галло. Результаты исследований, в которых из тканей пациентов с симптомами СПИДа впервые удалось выделить новый ретровирус, были опубликованы 20 мая 1983 года в журнале Science[14][15]. В этих же работах выделенный из больных СПИДом вирус был впервые успешно размножен в культивируемых Т-лимфоцитах. Французская группа исследователей показала, что серологически этот вирус отличается от HTLV-I, и назвала его LAV («вирус, ассоциированный с лимфаденопатией»)[16], а американская группа назвала его HTLV-III, ошибочно отнеся к группе HTLV-вирусов. Позднее этот вирус получил название HIV (в переводе с английского — ВИЧ, вирус иммунодефицита человека), а болезнь, им вызываемую, назвали синдромом приобретённого иммунодефицита (AIDS (англ.)). В 2008 году Люк Монтанье и Франсуаза Барр-Синусси были удостоены Нобелевской премии в области физиологии или медицины «за открытие вируса иммунодефицита человека»[17][16].
- 6 августа 1983 от СПИДа умирает американский певец Клаус Номи, который становится одной из первых знаменитостей, погибших от этой болезни.
- 1984 год — от СПИДа умирает французский философ и историк Мишель Фуко.
- 1985 год — изучены основные пути передачи ВИЧ, разработан первый тест на ВИЧ[18]:21.
- 1985 год — регистрация первого случая ВИЧ/СПИДа в СССР у иностранного гражданина.
- 1986 год — Джиа Каранджи стала первой американской знаменитостью из числа женщин, умерших от СПИДа.
- 1986 год — после осознания, что названия LAV и HTLV-III относятся к одному и тому же вирусу, принято новое название — «вирус иммунодефицита человека», ВИЧ (англ. Human immunodeficiency virus, HIV)[18]:21. Группой Монтанье описан ВИЧ-2, изучение генома показало, что ВИЧ-1 в эволюционном плане далеко отстаёт от ВИЧ-2.
- 1987 год — учреждена Глобальная программа ВОЗ по СПИДу[18]:22. Разработан зидовудин — первый препарат для лечения СПИДа[19]. Регистрация первого случая ВИЧ-инфекции у гражданина СССР.
- 1988 год — 1 декабря объявлен ООН Всемирным днём борьбы со СПИДом[18]:22.
- 1988 год — в СССР произошёл первый случай массового заражения людей вирусом иммунодефицита человека.
- 1990 год — в США разработан новый противовирусный препарат диданозин (видекс)[18]:22.
- 1991 год — от СПИДа умирает вокалист легендарной рок-группы Queen Фредди Меркьюри.
- 1995 год — принятие Закона РФ от 30.03.95 г. № 38-ФЗ «О предупреждении распространения в РФ заболевания, вызываемого вирусом иммунодефицита человека (ВИЧ-инфекции)»[18]:22. Начало применения препаратов высокоактивной антиретровирусной терапии, позволяющих большинству больных ВИЧ/СПИДом продлевать жизнь.
- 1996 год — создание Объединённой программы ООН по СПИД[18]:23. В Ванкувере на XI Конференции по СПИДу объявлено о создании нового поколения лекарственных средств — ингибиторов протеазы.
- 1998 год — на XII Международной конференции по СПИДу было признано, что миллионы людей умирают от ВИЧ-инфекции из-за дороговизны и недоступности лекарств[18]:23.
- 2001 год — Генеральная Ассамблея ООН приняла резолюцию S-26/2 «Глобальный кризис — глобальные действия».
- 2003 год — пленарное заседание 58-й сессии Генеральной Ассамблеи ООН по проблематике ВИЧ/СПИДа.
- 2006 год — ежегодный доклад организации «Объединённая программа ООН по ВИЧ/СПИДу» (UNAIDS) — AIDS Epidemic Update 2006[20].
- 2007 год — опубликованы данные о том, что вирус распространился из Африки на Гаити и далее попал в США примерно в 1969 году[21].
- 2008 год — опубликованы данные о том, что вирус происходит из Конго (район Киншаса — Браззавиль) и попал в человеческую популяцию от обезьян в начале двадцатого века[22].
СПИД является терминальной стадией ВИЧ-инфекции, период от инфицирования вирусом иммунодефицита человека до развития СПИДа длится в среднем 9—11 лет. Большинство симптомов вызваны оппортунистическими инфекциями — бактериальными, вирусными, грибковыми или паразитическими инфекциями, которые не развиваются у лиц с полноценной иммунной системой и поражают практически все системы органов[23]
ВИЧ-инфицированные имеют повышенный уровень онкологических заболеваний, например, саркомы Капоши, ракa шейки матки, а также лимфом. Кроме того, ВИЧ-инфицированные часто имеют системные симптомы инфекций, например, лихорадка, повышенное потоотделение по ночам, опухание лимфатических узлов, озноб, слабость и потеря веса[24][25]. Разные оппортунистические инфекции развиваются у ВИЧ-инфицированных в зависимости от географического положения больного.
Лёгочные инфекции[править | править код]
Пневмоцистная пневмония (вызываемая Pneumocystis jirovecii) является относительно редким заболеванием у иммунокомпетентных лиц, но значительно распространено среди ВИЧ-инфицированных лиц. До разработки эффективных методов диагностики, лечения и профилактики ВИЧ-инфекции в западных странах пневмоцистная пневмония была одной из непосредственных причин смертей ВИЧ-инфицированных. В развивающихся странах пневмоцистная пневмония остаётся одним из первых признаков СПИДа у недиагностированных лиц, хотя, как правило, не развивается при числе CD4-лимфоцитов менее 200 в микролитре крови[26].
Среди других заболеваний, ассоциированных с ВИЧ-инфекцией, отдельно можно выделить туберкулёз, так как последний передаётся иммунокомпетентным лицам воздушно-капельным путём и трудно поддаётся лечению[27]. Согласно ВОЗ, коинфекция туберкулёза и ВИЧ является одной из основных проблем мирового здравоохранения: в 2007 умерло более 456000 ВИЧ-положительных больных туберкулёзом, что составляет треть от общего числа смертей от туберкулёза и примерно четверть от двух миллионов смертей от ВИЧ-инфекции в этом году[28].
Заболеваемость туберкулёзом значительно снижена в странах Запада, однако в развивающихся странах эпидемиологическая ситуация и по ВИЧ-инфекции, и по туберкулёзу остаётся тяжёлой. На ранних стадиях ВИЧ-инфекции (число CD4-лимфоцитов превышает 300 клеток в 1 мкл), туберкулёз развивается как заболевание лёгких. На поздних стадиях ВИЧ-инфекции клиническое проявление туберкулёза часто атипичное, развивается внелёгочное системное заболевание. Симптомы, как правило, конституциональны и затрагивают костный мозг, кости, мочеполовую систему, желудочно-кишечный тракт, печень, периферические лимфатические узлы и центральную нервную систему[29].
Желудочно-кишечные инфекции[править | править код]
Эзофагит — воспаление слизистой оболочки нижней части пищевода. У ВИЧ-инфицированных эзофагит, как правило, бывает грибковой (кандидоз) или вирусной (вирус простого герпеса первого типа, цитомегаловирус) этиологии, в редких случаях вызван микобактериями[30].
Хроническая диарея при ВИЧ-инфекции может быть вызвана бактериальными (роды Salmonella, Shigella, Listeria или Campylobacter Mycobacterium) и паразитарными инфекциями (криптоспоридиоз, микроспоридиоз), а также вирусами[31]: (астровирус, аденовирус, ротавирус и цитомегаловирус; последний является причиной колитов).
В отдельных случаях диарея может являться побочным эффектом некоторых противовирусных препаратов, а также антибиотиков, которые используют при лечении бактериальных инфекций, вызывающих диарею, например Clostridium difficile. На поздних стадиях ВИЧ-инфекции диарея может снижать всасывание питательных веществ в кишечнике и является одной из причин слабости и упадка сил[32].
Неврологические и психиатрические симптомы[править | править код]
ВИЧ-инфекция приводит к различным нейропсихиатрическим осложнениям, которые либо возникают в результате прямого поражения нервной системы ВИЧ, либо являются следствием оппортунистических инфекций[33].
Токсоплазмоз вызывается одноклеточным паразитом Toxoplasma gondii, который может инфицировать головной мозг и вызывать энцефалит, либо глаза и лёгкие[34].
Криптококковый менингит — вариант менингита (воспаления мозговых оболочек), вызываемый грибом Cryptococcus neoformans. Симптомами заражения являются лихорадка, головная боль, усталость, тошнота, рвота, припадки.
Прогрессивная мультифокальная лейкоэнцефалопатия — демиелинизирующее заболевание, при котором постепенно разрушается миелин, покрывающий аксоны нейронов, и нарушается проведение нервных импульсов. Причиной болезни является полиомавирус, которым в латентной форме заражены до 70 % человеческой популяции. В активной форме полиомавирус вызывает смерть в течение нескольких месяцев после появления симптомов[35].
У ВИЧ-инфицированных возможно развитие метаболической энцефалопатии, называемой комплексом слабоумия СПИДа (англ. AIDS dementia complex, ADC), которая развивается в заражённом мозге при участии макрофагов и микроглии. Эти клетки легко заражаются ВИЧ и вырабатывают нейротоксин[36].
Специфические неврологические отклонения проявляются в виде когнитивных, поведенческих, двигательных нарушений. Такие нарушения проявляются через несколько лет после инфицирования ВИЧ и связаны со снижением числа CD4+ Т-лимфоцитов и повышением числа вирусных частиц в плазме крови.
Нейрокогнитивные расстройства преобладают в западных странах (10—20 %)[37] и незначительны, например, в Индии (1—2 %)[38][39]. Такие различия, возможно, вызваны другим серотипом ВИЧ, преобладающим в Индии. Маниакальный синдром, вызванный ВИЧ, чаще встречается у пациентов с развитой ВИЧ-инфекцией. Неврологические расстройства реже встречаются в случае терапии многими лекарствами.
Опухоли[править | править код]
ВИЧ-инфицированные пациенты часто имеют повышенные уровни возникновения раковых опухолей. Это в первую очередь связано с коинфекцией онкогенными ДНК-вирусами, особенно вирусом Эпштейна — Барр (англ. EBV), герпесвирусом, ассоциированным с саркомой Капоши (герпесвирус человека 8), и папилломавирусом человека (англ. HPV)[40][41].
Саркома Капоши является самой распространённой опухолью, возникающей у ВИЧ-инфицированных пациентов. Появление таких опухолей среди молодых гомосексуалов в 1981 году стало одним из первых признаков эпидемии СПИДа. Саркома Капоши вызывается гаммагерпесвирусом, называемым вирусом герпеса, связанным с саркомой Капоши. Симптомом заболевания является появление пурпурных узелков на коже, либо в полости рта, на эпителии желудочно-кишечного тракта и в лёгких. В-клеточные лимфомы, например, лимфома Беркитта, диффузная крупноклеточная В-клеточная лимфома и первичная лимфома ЦНС, чаще встречаются у ВИЧ-инфицированных пациентов. Эти формы опухолей часто предвещают неблагоприятный прогноз течения заболевания. Вирус Эпштейн-Барр является одной из причин возникновения таких лимфом. У ВИЧ-инфицированных пациентов лимфомы часто возникают в необычных местах, например, в ЖКТ[42]. В случае диагностики саркомы Капоши и агрессивной В-клеточной лимфомы у ВИЧ-инфицированного больного ставится диагноз СПИД. Инвазивный рак шейки матки, вызванный папилломавирусом человека, у ВИЧ-инфицированных женщин также указывает на развитие СПИДа[43].
У ВИЧ-инфицированных пациентов также часто возникают другие опухоли, например, болезнь Ходжкина (лимфогранулематоз), анальный рак и ректальная карцинома, гепатоклеточная карцинома, рак головы и шеи, рак лёгких. Перечисленные заболевания могут быть вызваны вирусами (вирус Эпштейна-Барр, папилломавирус человека, вирусный гепатит В и С), либо другими факторами, в том числе контактом с канцерогенами, например, с табачным дымом в случае рака лёгких.
Примечательно, что частота развития многих опухолей, например, рака груди или рака прямой кишки, не повышается у ВИЧ-инфицированных пациентов. В странах, где высокоактивная антиретровирусная терапия интенсивно используется для лечения ВИЧ-инфекции, число СПИД-связанных новообразований снижается, в то же время раковые опухоли являются основной причиной смерти ВИЧ-инфицированных пациентов[44]. В последние годы растёт количество смертей от форм опухолей, не связанных со СПИДом.
Другие инфекции[править | править код]
У пациентов с диагнозом СПИД часто развиваются оппортунистические инфекции, которые имеют неспецифические симптомы, например, лихорадку и снижение веса. Такие инфекции могут быть вызваны внутриклеточной Mycobacterium avium и цитомегаловирусом. Цитомегаловирус может вызывать колиты и воспаление сетчатки.
Пенициллоз, вызванный Penicillium marneffei, является третьей по частоте формой оппортунистических инфекций (после внелёгочного туберкулёза и криптококкоза), которая проявляется у ВИЧ-положительных лиц в эндемичном районе Юго-Восточной Азии[45].
У пациентов с диагнозом СПИД часто бывает нераспознанной инфекция парвовирусом В19. Одним из наиболее частых последствий является анемия, которую тяжело отличить от анемии, вызванной антиретровирусными лекарствами для лечения СПИДа[46].

Разрушение CD4+ лимфоцитов является главной причиной прогрессивного ослабления иммунной системы при ВИЧ-инфекции, которая приводит в конечном счёте к развитию синдрома приобретённого иммунодефицита[47].
На стадии СПИДа развиваются бактериальные, грибковые, вирусные, протозойные инфекции (оппортунистические инфекции) и неинфекционные заболевания как проявление катастрофы иммунной системы в результате падения числа CD4+ лимфоцитов ниже определённого уровня. По классификации CDC диагноз СПИД может выставляться при положительных тестах на ВИЧ и количестве CD4+ лимфоцитов ниже 200 клеток/мкл — категории А3, В3 и определённых патологических состояниях, включённых в категорию С.
Критериями перехода ВИЧ-инфекции на стадию СПИД для взрослых и подростков, согласно протоколам ВОЗ[48] 2006 года и классификации CDC[49], являются:
Бактериальные инфекции[править | править код]
- Лёгочный и внелёгочный туберкулёз.
- Тяжёлые бактериальные или рецидивирующие пневмонии (два или более эпизода в течение 6 месяцев).
- Инфекция, вызванная атипичными микобактериями (Mycobacterium avium), диссеминированная микобактеримия.
Грибковые инфекции[править | править код]
Вирусные инфекции[править | править код]
Протозойные инфекции[править | править код]
Другие заболевания[править | править код]
| Количество CD4 | Инфекционные | Неинфекционные |
|---|---|---|
| < 200 мкл−1 | Пневмоцистная пневмония Диссеминированный гистоплазмоз и кокцидиоидомикоз Милиарный, внелёгочный туберкулёз Прогрессирующая многоочаговая лейкоэнцефалопатия | Истощение Периферическая нейропатия ВИЧ-деменция Кардиомиопатия Вакуолярная миелопатия Неходжкинская лимфома |
| < 150 мкл−1 | Диссеминированная инфекция, вызванная вирусом простого герпеса Токсоплазмоз Криптококкоз Криптоспоридиоз, хронический Микроспоридиоз Кандидозный эзофагит | |
| < 50 мкл−1 | Диссеминированная цитомегаловирусная инфекция Диссеминированная МАК-инфекция (комплексом Mycobacterium avium) | Лимфома ЦНС |
Лечение ВИЧ/СПИДа можно разделить на антиретровирусную терапию и симптоматическую терапию оппортунистических инфекций. На терминальной стадии ВИЧ-инфекции — СПИД — лечение оппортунистических инфекций играет не меньшую роль, чем ВААРТ. Одной из целей антиретровирусной терапии на стадии СПИДа является снижение оппортунистических инфекций путём повышения числа CD4-клеток[52].
ВИЧ-инфицированные, имеющие число CD4-клеток выше 500 на 1 мм3, не находятся в зоне риска возникновения оппортунистических инфекций. Лица с содержанием CD4 от 500 до 200 клеток в 1 мм3 крови часто подвержены кандидозу и саркоме Капоши. При падении числа CD4-лимфоцитов от 200 до 100 клеток в 1 мм3 возникают пневмоцистная пневмония, гистоплазмоз, кокцидиомикоз и прогрессирующая мультифокальная лейкоэнцефалопатия. При снижении числа клеток от 100 до 50 на 1 мм3 появляются токсоплазмоз, криптоспоридиоз, и криптококкоз, цитомегаловирусная инфекция[52]. Из перечисленных выше оппортунистических инфекций, согласно данным французских исследователей, профилактика пневмоцистной пневмонии, токсоплазмоза и микобактериальной инфекции является более эффективной по соотношению результат/затраты, в то время как профилактика грибковой и цитомегаловирусной инфекции менее эффективна, чем другая терапия ВИЧ-инфекции, в том числе, ВААРТ, и должна иметь более низкий приоритет[53].
История вопроса[править | править код]
- В 1985 году препарат зидовудин (Retrovir, ZDV, AZT) прошёл клинические испытания для лечения ВИЧ-инфекции. Широко применяется в антиретровирусной терапии с 1987 года. Синтезирован в 1964 году для борьбы с раком[54].
- 1991—1994 годы — появились зальцитабин, диданозин и ставудин. Примерно в это же время начинают применять триметоприм/сульфаметоксазол, пентамидин, ганцикловир, фоскарнет и флуконазол, которые используются для борьбы с оппортунистическими инфекциями.
- Декабрь 1995 года — март 1996 года — появились первые ингибиторы протеазы: саквинавир, ритонавир, индинавир, применение которых привело к сокращению смертности с 38 % до 22 %[55].
- В 1996 году разработан первый ненуклеозидный ингибитор обратной транскриптазы — невирапин и ингибитор протеазы — нелфинавир.
- С 1994 по 1997 год доля больных в Европе, получающих ВААРТ, возросла с 2 % до 64 %[56], а с 1994 по 1998 год заболеваемость СПИДом упала с 30,7 % до 2,5 %[57].
- В 1998 году появилось понятие липодистрофия, как осложнение терапии, в 1999 году появились сообщения, что она, возможно, обусловлена токсическим действием препаратов на митохондрии.
- В 2000 году вышли исследования Harrington и Carpenter об избирательности терапии в зависимости от числа CD4 лимфоцитов[58].
- С 2005 по 2016 год смертность от СПИДа в мире сократилась почти вдвое — с 1,9 миллиона до 1 млн человек в год[59].
Начало терапии[править | править код]
Рекомендации ВОЗ для начала антиретровирусной терапии[60]
| Клиническая стадия ВОЗ | число CD4 клеток | Рекомендации |
|---|---|---|
| первая | < 200/mm³ | Лечение |
| 200–350/мм³ | Рассмотреть А и В | |
| вторая | < 200/мм³ | Лечение |
| 200–350/мм³ | Рассмотреть А и В | |
| третья | 200—350/мм³ | Лечение |
| четвёртая | 200—350/мм³ | Лечение |
- А — Если уровень лимфоцитов CD4 составляет около 350 клеток, начать переговоры с пациентом о необходимости начала АРТ и подготовка для её начала.
- В — Если вирусная нагрузка > 100 000 копий/мл, то рекомендуется начинать АРТ при CD4 в 350/мм³.
Заключение о начале терапии должно быть принято после двух разных подсчётов CD4 в промежутке 14—28 дней друг от друга, для исключения лабораторных ошибок и других заболеваний.
Без лечения средний период выживаемости после инфицирования ВИЧ составляет от 9 до 11 лет и зависит от подтипа ВИЧ[61], а продолжительность жизни после постановки диагноза СПИД в отсутствие терапии составляет, по результатам разных исследований, от 6 до 19 месяцев[62]. В регионах, в которых доступна ВААРТ, смертность от ВИЧ-инфекции и СПИДа снижается на 85,1—99,3 % в зависимости от того, насколько своевременно диагностировано заболевание и начато лечение. Продолжительность жизни после диагностики на ранней стадии ВИЧ-инфекции составляет 20—50 лет[63][64][65][66][67][68]. Если лечение начато на поздних стадиях, прогноз менее благоприятный: например, после постановки диагноза СПИД ожидаемая продолжительность жизни составляет 10—40 лет[69][63]. Стоимость лечения может составлять от 385 до 619 тысяч долларов США[70].
Продолжительность жизни ВИЧ-инфицированных пациентов со временем может изменяться по двум причинам: постоянно разрабатываются новые лекарственные средства и методы лечения, а ВИЧ, в свою очередь, вырабатывает устойчивость к лекарствам. В отсутствие антиретровирусной терапии смерть пациента наступает в течение одного года с момента постановки диагноза СПИД[71]. Считается, что ВИЧ-инфицированный, получающий ВААРТ, может прожить несколько десятилетий без развития СПИДа. Значительное влияние на качество и продолжительность жизни оказывают побочные эффекты от приёма лекарственных препаратов. Особенности развития ВИЧ-инфекции зависят от многих факторов, в том числе: от количества CD4 лимфоцитов и числа копий вирусной РНК на момент начала лечения, возраста пациента, уровня доступной медицинской помощи, приверженности больного лечению и появления резистентных штаммов вируса.
Большинство пациентов умирают от оппортунистических инфекций или опухолей, связанных с нарушением работы иммунной системы[72]. Клинические симптомы значительно отличаются между пациентами и зависят от многих факторов, среди которых: восприимчивость организма хозяина к инфекции, иммунный статус пациента[73][74][75], качество оказываемой медицинской помощи, сопутствующие инфекции[71][72], а также штамм вируса, которым инфицирован пациент[76][77][78].
Даже пациенты, получающие антиретровирусную терапию в течение длительного периода, могут иметь сопутствующие заболевания: нейрокогнитивные расстройства (комплексная СПИД-деменция), остеопороз, нейропатию, злокачественные опухоли, нефропатию, а также сердечно-сосудистые заболевания. Не всегда чётко понятно, являются эти сопутствующие заболевания следствием ВИЧ-инфекции, осложнений или побочными эффектами лечения[79][80][81][40][41][82][83][84].
Основной причиной смертности от СПИДа в настоящее время является сопутствующий туберкулёз. В Африке ВИЧ-инфекция является основной причиной распространения туберкулёза с 1990 года[85].
В следующей таблице показана зависимость ответа ВИЧ на антиретровирусную терапию от степени соблюдения пациентом режима лечения[86].
| Отношение числа назначенных доз к числу принятых доз | Частота, с которой вирусная нагрузка через 6 месяцев составила менее 400 копий/мл |
|---|---|
| > 95% | 78% |
| 90—95% | 45% |
| 80—90% | 33% |
| 70—80% | 29% |
| < 70% | 18% |
В исследованиях, проведённых среди больных СПИДом Нью-Йорка и умерших в 1999—2004 годах, отмечается значительное увеличение (на 33 %) причин смерти, не связанных с инфекцией и соответственно уменьшение причин смерти, связанных с ВИЧ, что может говорить о хорошей эффективности терапии. Частота смертей, не связанных с ВИЧ, за этот период составила 25 %[87]. Более 75 % причин смерти, не связанных с ВИЧ-инфекцией, составили сердечно-сосудистые патологии, онкопатологии, злоупотребление наркотиками[88].
Каждый год около 70 000 детей становятся сиротами из-за потери родителей, умерших от данной патологии[89]. Таким образом, к 2025 году сиротами СПИД станут примерно 40 миллионов детей[90].

- В Киеве, возле Киево-Печерской Лавры, в 2000-х годах установлен памятник жертвам СПИДа.
- В Кишинёве, в центральном парке имени Штефана чел Маре, был установлен памятник жертвам СПИДа, представляющий собой парковую скамейку из гаек и 1756 болтов — по количеству умерших от СПИДа в Молдове.
- Памятник жителям канадской провинции Квебек, умершим от СПИДа, установлен на улице Sainte-Catherine — центральной улице Gay Village (весёлой деревни) города Монреаль[91].
- Памятник жертвам СПИДа в Риге — своеобразная дорожка из камней, выложенная на пятачке между улицами Марияс и Сатеклес. Возглавляет дорожку каменный столб, а на булыжниках выбиты имена Фредди Меркьюри, Рудольфа Нуриева, Энтони Перкинса и других известных жертв чумы XX века.
СПИД и ВИЧ-инфекция: история распространения и симптомы. Справка
В 1969 году в США среди проституток были зафиксированы первые случаи болезни, протекавшей с симптомами СПИДа. Тогда медики не обратили на них особого внимания, посчитав редкой формой пневмонии.
В 1978 году у гомосексуалистов в США и Швеции, а также среди гетеросексуальных мужчин в Танзании и на Гаити были обнаружены симптомы одного и того же заболевания.
В 1981 году Центр по контролю и профилактике болезней (CDC) сообщил о выявлении у молодых гомосексуалистов в Лос‑Анджелесе и Нью‑Йорке новой болезни. В США было выявлено около 440 носителей вируса ВИЧ. Около 200 из этих людей умерли. Так как большинство больных были гомосексуалистами, новая болезнь получила название «Иммунодефицит, передаваемый гомосексуалистами» (Gay Related Immuno Deficiency ‑ GRID) или «Рак гомосексуалистов» (A Gay Cancer).
5 июня 1981 года американский ученый из Центра по контролю над заболеваниями Майкл Готлиб впервые описал новое заболевание, протекающее с глубоким поражением иммунной системы. Тщательный анализ привел американских исследователей к выводу о наличии неизвестного ранее синдрома, получившего в 1982 году название Aquired Immune Deficience Syndrom (AIDS) ‑ синдром приобретенного иммунодефицита (СПИД). Тогда же СПИД назвали болезнью четырех «эйч» («Н»), по заглавным буквам английских слов ‑ гомосексуалисты, больные гемофилией, гаитяне и героин, выделив этим самым группы риска для новой болезни.
Дефицит иммунитета, от которого страдали заболевшие СПИДом, ранее встречался только как врожденный порок недоношенных новорожденных детей. Врачи установили, что у этих больных снижение иммунитета не было врожденным, но было приобретено в зрелом возрасте.
В 1983 году французским ученым Монтанье была установлена вирусная природа болезни. Он обнаружил в удаленном у больного СПИДом лимфатическом узле вирус, назвав его LAV (lymphadenopathy associated virus). А 24 апреля 1984 года директор Института вирусологии человека Мэрилендского университета доктор Роберт Галло объявил о том, что он нашел истинную причину СПИДа. Ему удалось выделить вирус из периферической крови больных СПИДом. Он изолировал ретровирус, получивший название HTLV‑III (Human T‑lymphotropic virus type III). Эти два вируса оказались идентичными.
В 1985 году было установлено, что ВИЧ передается через жидкие среды тела: кровь, сперму, материнское молоко. В том же году был разработан первый тест на ВИЧ, на основе которого в США и Японии начали проверять на ВИЧ донорскую кровь и ее препараты.
В 1986 году группа Монтанье объявила об открытии нового вируса, который получил название HIV‑2 (ВИЧ‑2). Сравнительное изучение геномов ВИЧ‑1 и ВИЧ‑2 показало, что в эволюционном плане ВИЧ‑2 далеко отстоит от ВИЧ‑1. Авторы высказали предположение, что оба вируса существовали задолго до возникновения современной эпидемии СПИДа.
ВИЧ‑2 был впервые выделен в 1985 году от больных СПИДом в Гвинее‑Биссау и Островах Зеленого Мыса. Исследования показали, что обусловленные ВИЧ‑2 и ВИЧ‑1 заболевания являются самостоятельными инфекциями, так как имеются различия в особенностях возбудителей, клинике и эпидемиологии.
В 1987 году Всемирная организация здравоохранения утвердила название возбудителя СПИД – «вирус иммунодефицита человека» (ВИЧ, или в английской аббревиатуре HIV). В том же году была учреждена Глобальная программа ВОЗ по СПИДу, а Всемирной ассамблеей здравоохранения принята глобальная стратегия борьбы со СПИДом. В этом же году в ряде стран внедряется в лечение больных первый противовирусный препарат ‑ азидотимидин (зидовудин, ретровир).
Стоит отметить, что ВИЧ и СПИД не синонимы. СПИД ‑ понятие более широкое и означает дефицит иммунитета. Такое состояние может возникнуть в результате самых различных причин: при хронических истощающих заболеваниях, воздействии лучевой энергии, у детей с дефектами иммунной системы и у больных старческого возраста с инволюцией иммунной защиты, некоторых медикаментозных и гормональных препаратов. В настоящее время название СПИД применяется для обозначения только одной из стадий ВИЧ‑инфекции.
ВИЧ‑инфекция ‑ новое инфекционное заболевание, называвшееся до открытия ее возбудителя как синдром СПИДа. ВИЧ‑инфекция ‑ прогрессирующее антропонозное инфекционное заболевание, с кровоконтактным механизмом заражения, характеризующееся специфическим поражением иммунной системы с развитием тяжелого иммунодефицита, который проявляется вторичными инфекциями, злокачественными новообразованиями и аутоиммунными процессами.
Источником ВИЧ‑инфекции является больной СПИДом человек или носитель вируса, не имеющий явных симптомов заболевания. Болезнь передается при половых контактах, особенно гомосексуальных; от инфицированной матери к ребенку в период беременности через плаценту, во время родов, при грудном вскармливании от матери к плоду; через бритвенные приборы и другие колюще‑режущие предметы, зубные щетки и т. п. Эпидемиологи ВИЧ не допускают существования воздушно‑капельного и фекально‑орального путей передачи, так как выделение ВИЧ с мокротой, мочой и калом весьма незначительно, а также незначительно и число восприимчивых клеток в желудочно‑кишечном тракте и дыхательных путях.
Существует и искусственный путь передачи: при лечебно‑диагностических манипуляциях путем проникновения вируса через поврежденную кожу, слизистые оболочки (трансфузии крови и ее препаратов, трансплантации органов и тканей, инъекции, операции, эндоскопические процедуры и т. п.), искусственном оплодотворении, при внутривенном введении наркотических веществ, выполнении различного рода татуировок.
В группу риска входят пассивные гомосексуалисты и проститутки, среди женщин основную группу риска составляют наркоманки, вводящие наркотики внутривенно. Среди больных детей 4/5 составляют дети, матери которых больны СПИДом, инфицированы ВИЧ или принадлежат к известным группам риска. Второе по частоте заболеваемости место занимают дети, которым производили гемотрансфузии, третье ‑ больные гемофилией, медицинский персонал, имеющий профессиональный контакт с кровью и другими биологическими жидкостями ВИЧ‑инфицированных пациентов.
Вирус иммунодефицита может существовать в организме человека в течение десяти ‑ двенадцати лет, никак себя не проявляя. А на начальные признаки его проявления многие люди не обращают должного внимания, принимая их за симптомы других, на первый взгляд не опасных заболеваний. Если вовремя не начать процесс лечения, наступает конечная стадия ВИЧ ‑ СПИД. Вирус иммунодефицита может стать базой для развития других болезней, носящих инфекционный характер. Наряду с риском развития СПИДа повышается и риск появления других инфекционных заболеваний.
Симптомы: лихорадка более 1 месяца, диарея более 1 месяца, необъяснимая потеря массы тела на 10% и более, пневмонии затяжные, рецидивирующие или не поддающиеся стандартной терапии, постоянный кашель более 1 месяца, затяжные, рецидивирующие вирусные, бактериальные, паразитарные болезни, сепсис, увеличение лимфоузлов двух и более групп свыше 1 месяца, подострый энцефалит, слабоумие у ранее здоровых людей.
Последняя стадия ‑ СПИД ‑ протекает в трех клинических формах: онко‑СПИД, нейро‑СПИД и инфекто ‑ СПИД.
Онко‑СПИД проявляется саркомой Капоши и лимфомой головного мозга. Нейро‑СПИД характеризуется разнообразными поражениями ЦНС и периферических нервов. Что касается инфекто‑СПИДа, то он проявляется многочисленными инфекциями.
При переходе ВИЧ в заключающую стадию ‑ СПИД симптомы заболевания становятся более явными. Человека все чаще и чаще начинают поражать различные заболевания, такие как пневмония, туберкулез легких, вирус герпеса и другие заболевания, получившие название оппортунистические инфекции. Именно они и ведут к самым тяжелым последствиям. В это время вирус иммунодефицита становится тяжелейшим заболеванием.
Диагностика
Основным методом лабораторной диагностики ВИЧ‑инфекции является обнаружение антител к вирусу с помощью иммуноферментного анализа.
Лечение
На современном этапе развития медицины лекарства, способного полностью вылечить это заболевание не существует. Однако, при своевременном начале лечения ВИЧ можно надолго отодвинуть момент перехода вируса иммунодефицита в развитие СПИДа, а следовательно и продлить жизнь больному.
Схемы лечения, которые могут существенно замедлить развитие заболевания уже разработаны и продолжают совершенствоваться.
Статистика
ВИЧ ‑ инфекция географически распространена повсеместно и в настоящее время официально зарегистрирована почти во всех странах мира. Среди регионов, наиболее пораженных ВИЧ‑инфекцией ‑ Центральная Африка и Карибские острова.
По данным заместителя исполнительного директора Объединенной программы ООН по ВИЧ/СПИДу Мишеля Сидиби, эпидемия ВИЧ/СПИДа в мире пошла на спад, если еще пять лет назад количество людей, больных ВИЧ/СПИДом, составляло 39 миллионов человек, то сейчас эта цифра равняется 33 миллионам. Ежедневно на планете инфекция поражает 7 тысяч человек, каждый день регистрируется 6 тысяч смертей от СПИДа. В лечении нуждаются 7 миллионов ВИЧ‑инфицированных.
В России первый случай ВИЧ‑инфекции был выявлен в 1986 году, к концу 1998 года ВИЧ ‑ инфекция регистрировалась почти на всей территории России. По данным Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека на 2008 год, количество ВИЧ‑инфицированных в России не превышает 430 тысяч человек. За последние 20 лет в России была зарегистрирована 21 тысяча погибших от этой болезни. Как минимум 40 тысяч россиян нуждаются в постоянном приеме препаратов для лечения ВИЧ‑инфекции.
Материал подготовлен на основе информации открытых источников
О ВИЧ-инфекции
Из истории: Первые групповые вспышки новой вирусной инфекции были отмечены в 70 годах ХХ века.
5 июня 1981 года Американский Центр контроля над заболеваниями зарегистрировал новую болезнь – СПИД (Синдром приобретенного иммунодефицита). Это заболевание несет серьезную угрозу человечеству и об этом сегодня знает каждый.
Ежегодно 1 декабря, начиная с 1988 года, во всем мире отмечается День борьбы со СПИДом (World AIDS Day). Во многих сообществах организуется ряд мероприятий, проводимых в течение недель и дней до и после официального дня празднования.
19 мая 2019 года проводится ежегодный Международный день памяти умерших от СПИДа.
Весной 1991 года появился символ понимания и борьбы со СПИДом. Им стала красная ленточка.
В 1996 г. ООН создала союз шести всемирных организаций. Этот союз был назван Совместной программой Объединенных Наций по проблемам ВИЧ/СПИДа (Joint United Nations Programme on HIV/AIDS, UNAIDS). Спонсорами этого совместного проекта являются: Детский фонд ООН, Программа ООН по развитию, Фонд ООН по вопросам народонаселения, Организацию ООН по вопросам образования, науке и культуре (ЮНЕСКО), Всемирная организация здравоохранения (ВОЗ) и Всемирный банк.
Ситуация по ВИЧ:
С начала эпидемии ВИЧ-инфекции в мире зарегистрировано 77,3 млн. случаев ВИЧ-инфекции.
По последним данным во всем мире ВИЧ – инфекцией заражены примерно 36,9 миллиона человек.
Согласно данным государственной статистики за 2018 год, в Российской Федерации общее число зарегистрированных случаев ВИЧ-инфекции составило 896 075. По персонифицированным данным по состоянию на декабрь 2018 г. в России проживало 1 007 369 человек с диагнозом ВИЧ-инфекция.
История болезни
Часть ученых винит в возникновении ВИЧ обезьяну, которая заразила этим страшным вирусом человека еще в 20-х годах прошлого столетия. В результате научных исследований было выяснено, что очагом возникновения инфекции стала Западная Африка. В 1959 году от СПИДа умер первый человек. Носителем вируса оказался житель Конго. Через 10 лет в США у женщин легкого поведения были выявлены симптомы заболевания. В то время врачи не придали этому значения, решив, что все эти женщины больны пневмонией. Спустя еще 9 лет, были зафиксированы очаги этой эпидемии по всему миру. И уже через 3 года профильным Центром, занимающимся профилактикой болезней, было дано официальное признание о существовании ВИЧ и СПИДа.
Вирусное происхождение заболевания было открыто ученым из Франции – Монтанье. В 1983 году в лимфатических узлах страдающего СПИДом человека был найден вирус.
В 1985г. ученые пришли к выводу, что вирус иммунодефицита передается человеку через кровь, грудное молоко и половым путем. Был разработан тест, благодаря которому донорскую кровь начали проверять на наличие вируса.
ВИЧ – вирус иммунодефицита человека
ВИЧ-вирус иммунодефицита человека — вирус, вызывающий СПИД (синдром приобретенного иммунодефицита)
Пути передачи ВИЧ
Главным путем проникновения вируса в организм является кровь. Также вирус содержится в сперме.
ВИЧ-инфекцией можно заразиться при:
-
Половом контакте с ВИЧ-инфицированным. Половые контакты без презерватива – самый частый путь передачи ВИЧ. Заболевания, передаваемые половым путем, повышают риск заражения ВИЧ.
-
При гомосексуальных контактах.
-
При анальных половых контактах.
-
При переливании инфицированной крови (заражение возможно при искусственном оплодотворении, трансплантации кожи и органов).
-
При использовании игл, шприцев, которые использовал ВИЧ-инфицированный (особенно потребителями инъекционных наркотиков).
-
От матери ребенку (во время беременности, родов, при кормлении грудью).
-
Вероятность передачи ВИЧ-инфекции повышается при наличии поврежденных кожных покровов (травмы, ссадины, заболевания десен).
-
При нестерильных медицинских манипуляциях (татуировки, пирсинг, маникюр, педикюр).
От больных к медперсоналу, который имеет контакт с кровью и прочими жидкостями больных ВИЧ или СПИДом, при не соблюдении ими санитарно-гигиенических правил.
ВИЧ не передается:
-
Контактно-бытовым путем.
-
Москитами, комарами, пчелами, осами, блохами.
-
Через слюну и слезную жидкость, не содержащие кровь.
-
Через общие стаканы, вилки, фрукты, бутерброды.
-
Во время чихания и кашля.
-
Через поцелуй.
-
Через одежду
-
При пользовании ванной, туалетом
Кто находится в группе повышенного риска?
-
Лица, употребляющие инъекционные наркотики
-
Мужчины нетрадиционной сексуальной ориентации
-
Люди, у которых не один половой партнер
-
Лица, практикующие незащищенный анальный секс
-
Лица, практикующие незащищенный вагинальный секс
-
Лица, практикующие незащищенный оральный секс
-
Лица, которым сделали переливание непроверенной донорской крови
-
Больные, которым необходим гемодиализ
-
Дети, матери которых инфицированы
-
Больные другими венерическими заболеваниям
-
Женщины легкого поведения и их клиенты
Группы риска в профессиональной деятельности:
Существует круг профессий, представители которых имеют высокий риск заражения ВИЧ — инфекцией.
Основная группа риска в этой категории – это медицинские работники. Заражение происходит, как правило, при несоблюдении санитарно-гигиенических правил.
В эту группу риска входят хирурги. Если операция срочная и счет идет на минуты, провести анализ на ВИЧ-инфекцию просто нет возможности. Обязательной проверке на ВИЧ-инфекцию подлежат только плановые больные.
Помимо хирургов в группе риска медицинский персонал, осуществляющий забор и проверку крови, а также стоматологи.
Ситуации, во время которых может произойти заражение:
• порез или укол кожи инструментом, на котором могла остаться инфицированная кровь или другие биологические жидкости пациента;
• попадание крови/другой биологической жидкости пациента, содержащих кровь (рвотные массы, слюна с видимой кровью), на открытые участки кожи, слизистые оболочки медработника.
Еще одной группой риска инфицирования, связанного с профессиональной деятельностью, являются сотрудники салонов красоты — косметологи, мастера маникюра, татуажа. Как известно, в 50 % случаев мастер получает случайные порезы кожи или во время процедуры или при переносе инструментария в помещении в мягкой таре. Заражение происходит при попадании капель крови инфицированного человека с инструмента на раневую поверхность мастера во время травмы.
Третья группа риска – это сотрудники правоохранительных органов и уголовно-исполнительной системы. Во время задержания преступника сотрудники полиции подвергаются риску заражения, связанному с агрессивным поведением задерживаемого. Во время задержания преступник может инициировать драку, нанести ранения, укусы, в процессе которых в случае наличия у него инфекции ее распространение будет неизбежным.
Вирус иммунодефицита человека (ВИЧ) является внутриклеточным паразитом. Он отдает предпочтение иммунным клеткам. Разрушение этих клеток ведет к иммунодефициту. Инфекция распространяется очень быстро и вызывает острую нехватку иммунитета, который, в свою очередь, провоцирует злокачественные новообразования, другие инфекции и вторичные заболевания. Иммунная система ослабевает до такой степени, что становится неспособной противостоять болезням и инфекциям, атакующим организм. Вследствие ухудшения состояния здоровья человека, ему ставят диагноз СПИД. СПИД является конечной стадией ВИЧ-инфекции. Продолжительность течения ВИЧ-инфекции колеблется от нескольких месяцев до 15-20 лет.
В течении болезни выделяют 3 стадии:
-
Острая инфекция
-
Латентный период
-
Терминальная стадия (СПИД)
Примерно через 3-6 недель от момента заражения наступает острая лихорадочная фаза. Эта фаза происходит не у всех. Примерно у 50-70% инфицированных. У остальных больных после инкубационного периода наступает бессимптомная фаза.
Острая лихорадочная фаза (острая инфекция) проявляется следующими симптомами:
-
Лихорадка. Температура тела повышается до 37,5о
-
Боли в горле
-
Лимфоузлы в подмышках, в паху и на шее увеличиваются, образуя припухлость
-
Боли в области головы и глаз
-
Снижение массы тела
-
Снижение аппетита, сонливость
-
Рвота, тошнота, диарея
-
Кожные высыпания
Острая фаза длится о нескольких недель, далее ее сменяет бессимптомная фаза.
При бессимптомной фазе клинические проявления болезни могут отсутствовать. Примерно у 50% ВИЧ-инфицированных эта стадия может длиться до 10 лет.
Терминальная стадия (СПИД). Длительность данной стадии 1-2 года. Масса тела больного уменьшается больше чем на 10% по отношении к исходной. Развиваются присоединяющиеся инфекции:
- Туберкулез
-
Сальмонеллез
-
Легионеллез
-
Гриппа. Герпес
-
Кандидоз
-
Злокачественные опухоли
-
Саркома Капоши
-
Лимфомы
-
Пневмоцистная пневмония
В раннем детском возрасте ВИЧ-инфекция способствует задержке физического и психомоторного развития. У детей намного чаще происходит рецидивирование бактериальных инфекций.
Лечение
До настоящего времени нет такого лечения, которое могло бы устранить ВИЧ из организма.
Современное лечение ВИЧ-инфекции — высокоактивная антиретровирусная терапия — замедляет и практически останавливает прогрессирование ВИЧ-инфекции и ее переход в стадию СПИДа, позволяя ВИЧ-инфицированному человеку жить полноценной жизнью.
Оппортунистические инфекции лечат в соответствии с правилами терапии против вызвавших их возбудителей (антибактериальные, противогрибковые, противовирусные средства).
Меры профилактики ВИЧ-инфекции. Как избежать заражения?
— Информационные сообщения: предупреждения в СМИ о риске заражения, пропаганда здорового образа жизни и межполовых отношений.
Зная основные пути передачи ВИЧ-инфекции человек должен:
-Использовать личные средства гигиены – бритву, маникюрные принадлежности и др.
-при прокалывании ушей использовать только стерильные инструменты
-не пробовать наркотические вещества
— Барьерная контрацепция. Следует всегда при себе иметь барьерные средства контрацепции (презервативы). Не вступать в незащищенные половые отношения, в ранние половые отношения
Инфицированным женщинам не рекомендуется иметь детей, так как риск передачи инфекции младенцу очень высок, и врачи не всегда могут спасти его от заражения.
-
Организация диспансерного наблюдения за ВИЧ-инфицированными.
-
Своевременное выявление и установление диагноза ВИЧ
-
Обследование доноров крови
-
Профилактическая работа с уязвимыми группами населения
-
Гигиеническое воспитание населения (предоставление информации о методах профилактики, о симптомах заболевания)
-
В ЛПУ должны иметь для больных и посетителей специальную наглядную агитацию по предупреждению заражения ВИЧ, информацию о деятельности медицинских учреждений и общественных организаций, оказывающих помощь инфицированным ВИЧ.
-
Учебные программы образовательных учреждений (школы, вузы) должны включать вопросы профилактики ВИЧ.
-
В рамках Всемирного дня по борьбе со СПИДом в учебных учреждений должны проводиться классные часы, внеклассные мероприятия по данной теме.
Профилактика профессионального заражения ВИЧ у медработников
Особенно актуальна профилактика ВИЧ-инфекции в хирургии и стоматологии, где повышен риск заражения.
Меры предосторожности:
-
Необходимо безопасно оборудовать место по работе с пробами крови, инструментами
-
Использовать тщательно продезинфицированные приспособления
-
Работать только в одноразовых медицинских перчатках
В каких случаях необходимо подозревать ВИЧ-инфекцию?
Кому необходимо пройти обследование на ВИЧ?
- Лихорадка по неизвестным причинам, длится уже более 7 дней
-
Увеличение всех групп лимфатических узлов на протяжении нескольких недель по неизвестной причине
-
Непрекращающаяся диарея на протяжении нескольких недель
-
Признаки кандидоза (молочницы) в ротовой полости
-
Обширные герпетические высыпания с нехарактерной локализацией
-
Резкое снижение массы тела
-
Если имел место незащищенный половой контакт с новым партнером или если порвался презерватив
-
Если человек подвергся сексуальному насилию
-
Если постоянный половой партнер имел половые контакты с другим человеком
-
Если прошлый или настоящий половой партнер инфицирован ВИЧ
-
Если для создания пирсинга или татуировок были использованы иглы, уже бывшие в употреблении
Цели проведения Всемирного дня борьбы со СПИДом, а также Международного дня памяти умерших от СПИДа:
В эти памятные даты все организации предоставляют информацию о данном заболевании населению.
Цели проведения мероприятия:
-
Повысить глобальную осведомленность о ВИЧ/СПИД
-
Усилить общественную профилактику программ профилактики ВИЧ/СПИДа
-
Остановить распространение ВИЧ/СПИДа, положить начало тенденции к сокращению уровня заболеваемости
-
Обеспечить всеобщий доступ к лечению ВИЧ/СПИДа для тех, кто в этом нуждается
-
Организовать обучение и предоставление информации по всем аспектам ВИЧ/СПИД
-
Содействовать прогрессу в профилактике и лечении ВИЧ/СПИД, а также в уходе за больными людьми в странах с высокой распространенностью этой болезни во всем мире
-
Научить людей как избежать заражения и что предпринять при первых его симптомах
-
Объяснить людям почему при соблюдении некоторых правил не стоит бояться людей больных СПИДом.
-
При проведении мероприятий в школах и вузах – привлечь внимание учащихся к проблеме СПИДа. Познакомить с путями передачи заболевания. Сформировать навыки бережного и внимательного отношения к своему здоровью.
Виды мероприятий, проводимых в рамках
Всемирного дня по борьбе со СПИДом:
-
Манифестации и шествия со свечами
-
Театральные представления
-
Поэтические чтения
-
Общественные дискуссии
-
Художественные фотовыставки
-
Марафонские забеги, велогонки
-
Конкурсы плакатов
-
Профилактические кампании в печати
-
Семинары для представителей средств массовой информации
-
Концерты с участием звезд культуры
-
Концерты
-
В школах –проведение классных часов, посвященных теме ВИЧ/СПИД
-
В институтах — лекции
|
Информация для родителей: Перед вами стоит цель донести до ребенка информацию о ВИЧ/СПИДе и защитить его. Не стоит думать, что этот вопрос решится сам собой. Расскажите ребенку о проблеме ВИЧ спокойно, доступным для понимания ребенка языком. |
Стратегия:
В мае 2011 года 64-я сессия Всемирной ассамблеи здравоохранения определила общую концепцию и стратегические направления борьбы с ВИЧ- инфекцией. Цель стратегии по ВИЧ — к 2030 году положить конец эпидемии СПИДа как угрозе здоровью населения в контексте обеспечения здоровой жизни и благополучия для всех людей всех возрастов.
На Совещании высокого уровня Генеральной ассамблеи ООН по ВИЧ/СПИДу 8 июня 2016 года государства-члены ООН утвердили план по активизации усилий для прекращения эпидемии ВИЧ-инфекции к 2030 году (Политическая декларация «Ускоренными темпами к активизации борьбы с ВИЧ и прекращению эпидемии к 2030 году»), отметив необходимость значительного наращивания усилий в направлении достижения цели обеспечения всеобщего доступа к программам профилактики, лечения, ухода и поддержки при ВИЧ-инфекции.
Проблема распространения ВИЧ-инфекции является актуальной на протяжении 30 лет. Несмотря на предпринимаемые усилия переломить ход развития эпидемии пока не удалось.
СПИД стал «чумой» не только XX, но и XXI века.
ЛЮБОЙ ЖЕЛАЮЩИЙ МОЖЕТ ПРОЙТИ БЕСПЛАТНО АНОНИМНОЕ ОБСЛЕДОВАНИЕ НА ВИЧ-ИНФЕКЦИЮ В ЛЮБОМ МЕДИЦИНСКОМ УЧРЕЖДЕНИИ.