Апластическая анемия — Википедия
Апласти́ческая анеми́я — заболевание кроветворной системы, характеризуется угнетением кроветворной функции костного мозга и проявляется недостаточным образованием эритроцитов, лейкоцитов и тромбоцитов (пангемоцитопенией) или только одних эритроцитов (парциальная гипопластическая анемия, синонимы: апластическая анемия, арегенераторная анемия, геморрагическая алейкия, миелопарез, миелофтиз, панмиелофтиз, прогрессирующая гипоцитемия). Для апластических анемий характерна выраженная панцитопения — анемия, лейкопения, тромбоцитопения и лимфопения[3].
Впервые это заболевание было описано Паулем Эрлихом в 1888 году у 21-летней женщины. Термин «апластическая анемия» был предложен Чауфордом в 1904 году. Апластическая анемия — одно из самых тяжёлых расстройств гемопоэза. Без лечения больные тяжёлыми формами апластической анемии погибают в течение нескольких месяцев. При своевременном адекватном лечении прогноз достаточно хороший. Длительный период времени апластическая (гипопластическая) анемия рассматривалась как синдром, объединяющий патологические состояния костного мозга протекающие с выраженной гипоплазией кроветворения. Современная медицина относит апластическую анемию к арегенераторному виду анемий (гипо-, апластические анемии)
Причинами апластической анемии могут быть:
- Химические вещества (мышьяк, ароматические углеводороды, в частности бензол, соли тяжёлых металлов).
- Ионизирующее излучение (см. Мария Склодовская-Кюри)
- Лекарственные препараты (НПВС, цитостатики, мерказолил, анальгин, левомицетин).
- Инфекционные агенты (вирусы, м/о).
- Аутоиммунные процессы (СКВ, синдром Шегрена).
Апластическая анемия может развиться при воздействии ряда миелотоксических факторов: ионизирующего излучения, химических веществ — бензола, солей золота, мышьяка; лекарственных средств — хлорамфеникола (левомицетина), фенилбутазона (бутадион), хлорпромазина (аминазин), мепробамата, дилантина, антиметаболитов (6-меркаптопурина, метотрексата), алкилирующих (циклофосфана, хлорбутина) и некоторых других средств. Миелотоксический эффект от воздействия одних факторов (ионизирующее излучение, антиметаболиты) возникает всегда при достаточно большой дозе, других — проявляется индивидуально. Причина индивидуальной чувствительности, в частности к некоторым лекарственным средствам не всегда ясна, но может быть связана с генетическими дефектами кроветворных клеток. Это относится, например, к хлорамфениколу и фенилбутазону, которые вызывают супрессию (в зависимости от дозы) эритропоэза с частотой соответственно 1:24000 и 1:40000 лиц, их принимающих. Наследственный характер индивидуальной чувствительности эритропоэтических клеток к данным лекарственным веществам подтверждается развитием аплазии костного мозга у разных членов одной семьи и у однояйцевых близнецов. В других случаях вероятна связь индуцированного лекарственными веществами угнетения кроветворения с иммунными механизмами появлением антител к эритроцитарным предшественникам. Описаны случаи возникновения апластической анемии после острого вирусного гепатита (возможно, вследствие способности вируса гепатита изменять кариотип клеток, что было прослежено на культуре лейкоцитов), перенесенной инфекции вирусом Эпштейна — Барр, парвовирусом.
Существует и наследственная форма апластической анемии — анемия Фанкони.
Более чем у половины больных не удается выявить какие-либо причинные факторы — это так называемая идиопатическая апластическая анемия. Механизмы, лежащие в основе идиопатической формы анемии, неясны. Возможен аутоиммунный механизм, связанный с воздействием на клетки костного мозга аутоантител при участии иммунных лимфоцитов. Показано, что лимфоциты (Т-супрессоры) больных тормозят образование эритроцитных колоний костного мозга донора и могут нарушать дифференциацию и пролиферацию гематопоэтических предшественников.
Предполагают также, что основой апластической анемии может быть поражение (внутренний дефект) стволовой клетки, о чём свидетельствует восстановление кроветворения у больных после трансплантации им аллогенного костного мозга, содержащего нормальные стволовые клетки. Существуют экспериментальные данные, свидетельствующие о значении для развития апластического процесса и нарушений микроокружения — первичного дефекта стромальных клеток костного мозга. Однако суть этих клеточных дефектов остается неясной, так же как и их первичность. Возможно, что при разных формах апластической анемии патогенетические механизмы неодинаковы.
- Анемический синдром (головокружение, снижение работоспособности, утомляемость, бледность кожных покровов и слизистых, сердцебиение, непереносимость длительных физических нагрузок и т. д.)
- Геморрагический синдром (кровоточивость, склонность к диапедезам, геморрагии)
- Инфекционные осложнения.
Картина периферической крови представлена трицитопенией. Снижение гемоглобина значительно и может достигать критического уровня 20 — 30 г/л. Цветовой показатель обычно равен единице, но в ряде случаев может быть гиперхромия и макроцитоз эритроцитов. Количество ретикулоцитов резко снижено. Характерна выраженная лейкопения (агранулоцитоз). Абсолютное содержание лимфоцитов не изменено или снижено. Количество тромбоцитов всегда снижено, в некоторых случаях не удается обнаружить их вообще. В большинстве случаев увеличивается СОЭ (до 40 — 60 мм/час).
Клиническая картина заболевания позволяет сформировать первичное представление о патологии системы крови. Отправной точкой диагностического поиска является клиническое исследование крови с подсчетом количества ретикулоцитов и тромбоцитов. Выявление би- или трицитопении при исследовании периферической крови служит основанием для выполнения морфологического исследования костного мозга.
Диагноз АА устанавливают на основании типичной гистологической картины костного мозга, получаемого методом трепанобиопсии гребня подвздошной кости. Для получения качественного (информативного) биоптата используются трепаны, выпускаемые промышленным способом (Sherwood medical).
При гистологическом исследовании костного мозга обнаруживается большое количество жировой ткани, содержание которой может достигать 90 %. Среди доминирующей жировой ткани встречаются стромальные и лимфоидные элементы. Гематогенные клетки представлены крайне скудно: в небольшом количестве встречаются эритроидные и гранулоцитарные предшественники. Мегакариоциты отсутствуют.
Лечение апластической анемии представляет собой очень сложную задачу.
- Лечение с глюкокортикоидами эффективно, если болезнь обусловлена аутоиммунными механизмами, появлением антител против клеток крови.
- Лечение анаболическими препаратами стимулируют кроветворение.
- Лечение андрогенами обладает анаболическим эффектом и стимулируют эритропоэз.
- Лечение цитостатиками (иммунодепресантами) — назначается лишь при отсутствии эффекта от других методов лечение у больных с аутоиммунной формой, в том числе при парциальной красноклеточной аплазии.
- Спленэктомия
- Лечение антилимфоцитарным глобулином рекомендуется при отсутствии эффекта от спленэктомии и других методов лечения.
- Лечение циклоспорином. Циклоспорин А (сандиммун) обладает иммунодепрессантным эффектом, селективно ингибирует транскрипцию гена интерлейкина-2 в Т-лимфоцитах, подавляет продукцию Гамма интерферона и альфа фактора некроза опухоли.
- Трансплантация костного мозга.
Основным и единственным патогенетическим методом лечения апластической анемии, позволяющим рассчитывать на спасение жизни больного, является трансплантация костного мозга от совместимого донора. При невозможности подобрать донора проводится паллиативная терапия. В качестве базисного препарата используется иммунодепрессант циклоспорин А. У больных нетяжёлой апластической анемией использование данного препарата позволяет рассчитывать в ряде случаев на успех. Кроме того использование циклоспорина А целесообразно и с тех позиций, что глюкокортикоиды, андрогены и антилимфоцитарный глобулин способны улучшить состояние гемопоэза у больных нетяжёлой апластической анемией, но, однако, при этом следует принимать во внимание повышенный риск развития в последующем клональных заболеваний костного мозга. Применение циклоспорина А сводит такой риск к минимуму. Следует также отметить, что у части больных нетяжёлой апластической анемией, преодолевших 6-месячный порог выживаемости, может наступить спонтанное улучшение даже если им не проводилось никакой иммуносупрессивной терапии. Эффект от иммуносупрессивной терапии у больных тяжёлой и крайне тяжелой апластической анемией сомнителен.
- Лечение колониестимулирующими факторами или миелоидными факторами роста — эти гликопротеиды, стимулирующие пролиферацию и дифференциацию клеток-предшественниц гемопоэза различных типов.
- Трансфузии эритроцитов; показания: выраженная анемия, гипоксия мозга, гемодинамические нарушения.
Все больные апластической анемией нуждаются в заместительной трансфузионной терапии эритроцитарной и/или тромбоцитарной массой. Объём трансфузионной терапии определяется показателями периферической крови и клиническими проявлениями заболевания. Кроме того, проводится антибактериальная и микостатическая терапия с целью профилактики или лечения инфекционных осложнений.
Ремиссию удаётся получить примерно у половины больных. Прогноз несколько лучше у детей, чем у взрослых. Наличие большого количества жира в костном мозге не говорит о необратимости процесса. Бывают случаи, когда и у таких больных наступает полная ремиссия и полная репарация костномозгового кроветворения. Прогноз лучше, когда увеличено содержание ретикулоцитов, когда в костном мозге имеется более полиморфная картина, когда имеется небольшое увеличение размеров селезёнки и хотя бы небольшой, но чёткий эффект от кортикостероидных гормонов. В этих случаях спленэктомия оказывает чаще хороший эффект вплоть до полного выздоровления. У части больных апластический синдром является началом острого лейкоза. Иногда признаки гемобластоза выявляются лишь через несколько лет от начала болезни.
Что такое угнетение костного мозга
Заболевание костного мозга: причины и симптомы
Костный мозг — это один из важных кроветворных органов человеческого организма, от состояния которого во многом зависит и иммунитет, сопротивляемость различным заболеваниям. В костном мозге вырабатываются клетки крови, которые затем будут циркулировать по всему организму.
Любое нарушение работы костного мозга грозит отсутствием обновления крови, ведь выработка новых клеток и замена ими отмирающих, старых, может быть замедлена или существенно сокращена. Из-за этого кровь обедняется, и организм начинает страдать. Также сам костный мозг может быть заражен вредоносными раковыми клетками, которые могут быть разнесены током крови по всем органам человеческого организма, включая и этот важный орган.
Какие бывают заболевания костного мозга
Рак костного мозга – опасное онкологическое заболевание
В крупных и средних трубчатых, то есть полых костях организма человека содержится особая рыхлая ткань красноватого цвета. Это костный мозг, играющий огромную роль в здоровье человеческого организма. С возрастом человека красная ткань постепенно становится желтой, так как замещается жировыми клетками. С этим процессом постепенно приходит старость, организм все хуже и медленнее обновляется, возникают разнообразные заболевание костного мозга, симптомы которых вначале напоминают простуду с лихорадкой, а затем становятся более выраженными и характерными.
Так как в костном мозге формируются новые клетки, то имеется возможность возникновения их мутаций. Образующиеся дефектные клетки становятся причиной злокачественных новообразований, а также вытесняют нормально функционирующие здоровые клетки.
В результате человек заболевает опаснейшим из существующих заболеваний — раком.
Существует множество различных заболеваний костного мозга, из которых более других распространены следующие:
Анемии достаточно распространены и могут неплохо поддаваться терапии. Лейкоз, или рак белых кровяных телец, несет огромную угрозу не только здоровью, но и жизни пациента. Однако при современном уровне медицины и ранней диагностики есть возможность не только максимально продлить жизнь больному, но и полностью излечить заболевание.
Причины и симптомы
Симптомы заболевания костного мозга зависят от стадии и формы болезни
Заболевание костного мозга, симптомы которого достаточно разнообразны, возникает по разным причинам. Огромное значение играет образ жизни человека, наличие вредных привычек, постоянные или острые стрессы, слабое здоровье и отягощенная наследственность. Особенный риск для здоровья несет наличие внутри семьи заболеваний кроветворных органов, а также наследственная склонность к онкологическим заболеваниям.
Первичный рак костного мозга диагностируется крайне редко. В основном онкологические заболевания этого органа являются метастазами, которые переносятся током крови из раковых опухолей в легких и эндокринных железах человека. Некоторые ученые считают, что есть возможность развития рака костного мозга из-за первичного очага в толстом кишечнике больного.
Симптомы заболевания достаточно характерны:
- Анемия.
- Сильная слабость, быстрая утомляемость.
- Снижение свертывания крови, что приводит к частым носовым и другим кровотечениям, а также к возникновению синяков и кровоподтеков на теле от малейшего прикосновения. У больного могут сильно кровоточить десны даже при полном здоровье зубов.
- Постоянная сонливость, человек не чувствует себя выспавшимся даже при длительном сне.
- Головные боли.
- Снижение зрения.
- Боли в кишечнике.
- Проблемы со стулом.
- Тошнота, рвота.
- Сильная жажда.
- Боли в мышцах ног.
- Боли в костях.
- Повышенная хрупкость костной ткани и как следствие — частые трещины и переломы при минимальном воздействии.
- Деформация позвоночника.
- Снижение массы тела.
- Склонность к инфекционным заболеваниям из-за очень слабого иммунитета.
Такие симптомы несколько расплывчаты и не указывают на конкретное заболевание или его локализацию, однако являются настоящим тревожным сигналом, требующим неотложного визита к врачу.
Больше информации о пересадке костного мозга можно узнать из видео:
Читайте: Опухоль Беркитта: признаки и методика лечения лимфомыСамое страшное заболевание костного мозга
Апластическая анемия — симптомы идиопатической анемии, лечение, что это за болезнь
Апластическая (гипопластическая) анемия – тяжелое заболевание крови, которое часто может приводить к летальному исходу. Несмотря на серьезность патологии, в последнее время были разработаны методы лечения апластической анемии, которые увеличили количество выживших пациентов.
Механизм развития анемии
Анемия – синдром, характеризующийся резким уменьшением количества гемоглобина в крови. Как известно, благодаря гемоглобину происходит перенос кислорода от легким к тканям. Гемоглобин, в свою очередь, входит в состав красных кровяных телец – эритроцитов, синтезирующихся в костном мозге из гемопоэтических стволовых клеток.
При апластической анемии костный мозг прекращает производство новых эритроцитов или резко снижает их выработку. Связано это с уменьшением количества гемопоэтических стволовых клеток или с нарушением их функциональности.
Обычно снижается выработка не только эритроцитов, но и иммунных клеток – лейкоцитов, а также тромбоцитов, отвечающих за свертывание крови. Возникает состояние, которое называется пангемоцитопенией. Таким образом, при апластической анемии прекращается или серьезно снижается выработка всех основных клеток крови, что представляет серьезную угрозу для жизни. Ведь эритроциты живут в крови всего три месяца, тромбоциты – 1-2 недели, а лейкоциты – не больше дня.
Эпидемиология
Апластическая анемия – редкое заболевание. В среднем заболевает 1 человек из 500 тысяч в год. Анемия может поразить человека в любом возрасте. Но основная часть заболевших – дети и молодые люди (от 10 до 25 лет) или пожилые люди старше 60 лет. Женщины и мужчины болеют с одинаковой частотой.
Разновидности
Апластическая анемия подразделяется на врожденную (появившуюся с рождения) и приобретенную. Если причины апластической анемии неизвестны, то речь идет об идиопатической анемии. Такая ситуация наблюдается у половины больных. Иногда останавливается только синтез новых эритроцитов, а другие клетки крови синтезируются в прежнем объеме. Этот тип заболевания называется парциальной гипопластической анемией.
Одной из разновидностей врожденной апластической анемии является анемия Фанкони. Она проявляется уже в детском возрасте и обусловлена генетическими отклонениями. Кроме анемии, у детей с такими отклонениями наблюдаются недоразвитость конечностей, микроцефалия, небольшой рост, нарушения слуха и другие дефекты развития. Другие врожденные апластические анемии – анемия Эстрена-Дамешека и анемия Даймонда-Блекфена.
В зависимости от длительности течения анемия делится на острую (до 1 месяца), подострую (1-6 месяцев) и хроническую (более 6 месяцев) формы.
Пара слов о приобретенной апластической анемии
Эта апластическая анемия встречается чаще, чем врожденная. От этой страшной болезни не застрахован никто. Причем часто причины ее появления не удается установить. В других случаях причиной приобретенной анемии могут быть отравления токсинами, облучение.
Не исключено, что за возникновением приобретенной апластической анемии стоят аутоиммунные процессы. Например, вирусная инфекция приводит к тому, что иммунные клетки атакуют вместо вирусов клетки костного мозга, В результате происходит угнетение функций этого органа. Некоторые исследования возлагают ответственн
что это такое, симптомы, причины и лечение
Апластическая анемия — это частный случай нарушения синтеза эритроцитов, сопровождается падением концентрации гемоглобина в результате отклонения в работе костного мозга.
В отличие от прочих форм нарушения, например железодефицитной, мегалобластной, патология куда сложнее излечивается, имеет худшие прогнозы.
Клиническая картина сама крайне опасна, несет большую угрозу для существования организма. Процесс дает кровотечения различной локализации, которые трудно остановить.
Диагностика представляет определенные сложности по причине отсутствия специфических клинических признаков, если проводить исследование рутинными способами.
Лечение строго стационарное. Длительность его неопределенно высокая, зависит от тяжести патологического процесса, характера его течения, агрессивности, стадии, также индивидуальных особенностей организма человека, первичной причины становления нарушения.
Механизм становления нарушения
В основе патогенеза расстройства лежит группа патогенетических факторов. Можно назвать четыре основных момента, которые и играют роль в формировании диагноза.
Прием некоторых лекарственных препаратов
Искусственное угнетение синтеза эритроцитов и незрелых клеток-предшественников.
Работу костного мозга нарушает группа медикаментов. Таким эффектом обладают цитостатики, которые активно применяются в лечении опухолей, особенно злокачественных.
Иммунодепрессанты, противосудорожные средства, лекарства для борьбы с малярией, некоторые гормональные медикаменты, а также фармакологические наименования для коррекции работы щитовидной железы.
Так или иначе побочный эффект не может длиться долго, но гипопластическая анемия протекает остро, достаточно и одного эпизода, чтобы создать большие риски для жизни. Отмена медикаментов становится первым шагом на пути к выздоровлению.
Вирусные поражения
Угнетать работу костного мозга могут и некоторые инфекционные структуры. В частности такой способностью обладают агенты гепатита, цитомегаловирус, штамм герпеса четвертого типа (Эпштейна-Барр). В том числе микобактерии туберкулеза.
При остром течении названных патологий апластической анемии может и не быть. Однако резко вырастают риски развития в ближайшем будущем.
Взаимодействие с химическими отравляющими компонентами
Гербицидами, средствами на основе ртути, мышьяка, бензола, органических спиртов, также прочих веществ, щелочных металлов, синильной кислоты.
Восстановление в таком случае требует исключения влияния отравляющего соединения на организм человека.
Воздействие ионизирующего излучения
Радиация сказывается на состоянии костного мозга в большей степени, что и провоцирует возможные кровотечения у пораженных людей. По мере выздоровления апластическая анемия постепенно отходит.
Названные этиологические факторы — это провокаторы, они выступают виновниками начала расстройства.
Далее же отклонение движется по одному выверенному сценарию.
Угнетается работа красного костного мозга и процесс кроветворения. Он перестает генерировать незрелые клетки, предшественники форменных, полноценных.
Отсюда снижение концентрации эритроцитов, а значит и гемоглобина, который участвует в перемещении кислорода по тканям и органам через кровеносное русло. Происходит замещение красного костного мозга — желтым, что только усугубляет аплазию.
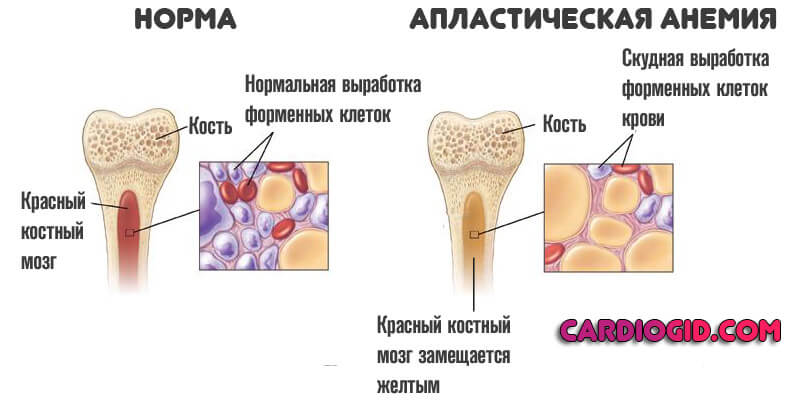
Недостаточная транспортировка кислорода вызывает гипоксию. Клетки не могут дышать. Страдают все ткани организма.
Падает концентрация тромбоцитов, повышается текучесть крови, растут риски летальных кровотечений.
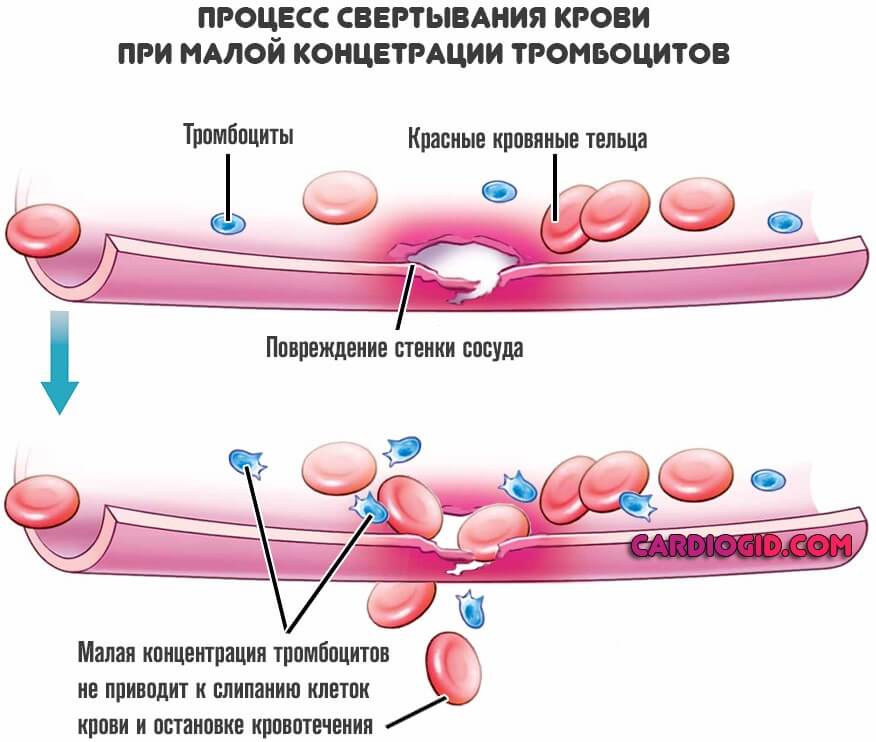
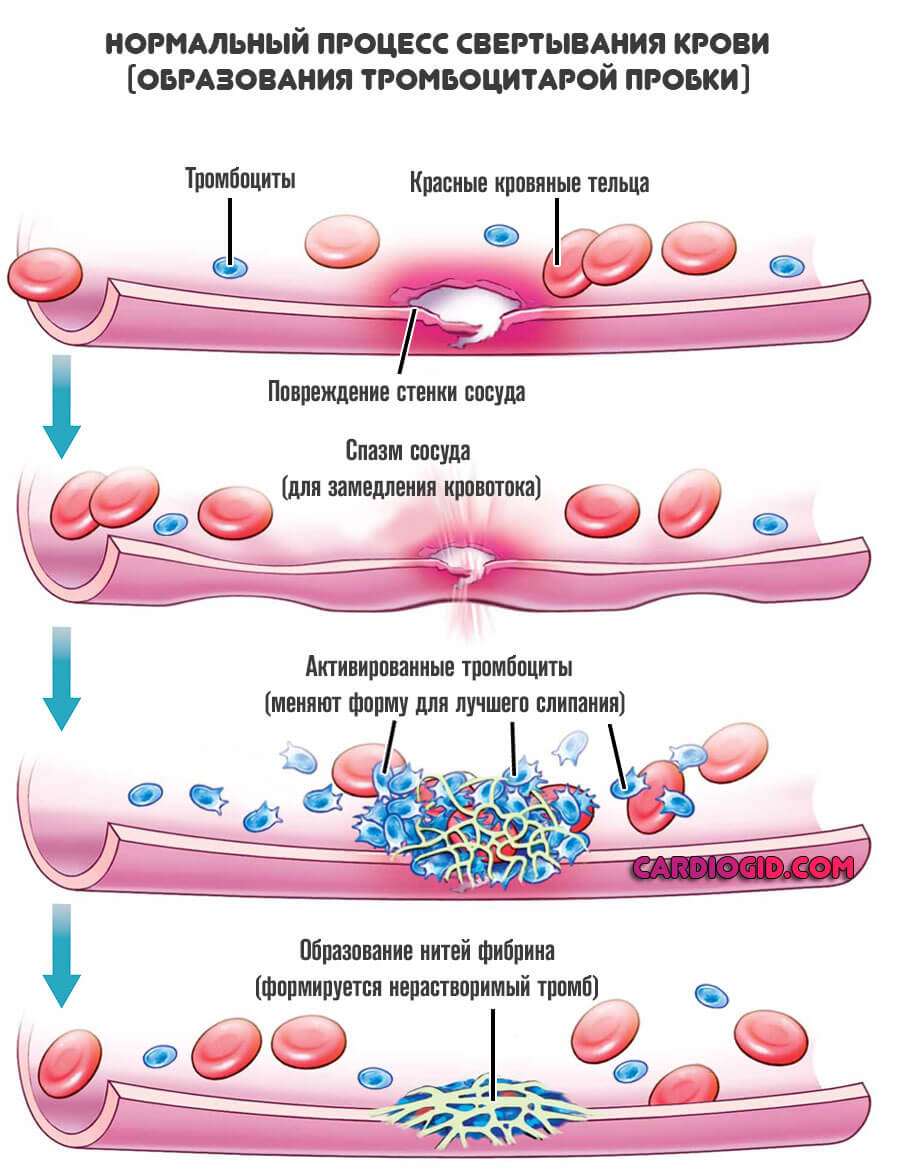
Восстановление заключается в избавлении от причины проблемы. Только так можно рассчитывать на излечение. Для грамотного терапевтического влияния требуется знать точный механизм.
Классификация
Типизацию проводят по степени тяжести апластической анемии. По этому критерию выделяют три основных формы болезни.
- Легкая. Сопровождается минимальными изменениями синтеза клеток. Возникает избыточная выработка некоторых химических веществ. Однако на этой стадии человек пока не замечает симптомов.
В редких случаях возможно образование на коже небольших язв, красных пятен. Кроме того, возникают носовые кровотечения. Обнаруживаются базовые анемические симптомы: головная боль, слабость, тошнота, прочие, в том числе снижение работоспособности. Это идеальный момент для начала лечения.
- Средняя степень. Дает уже выраженную клинику, которую трудно не заметить. Присутствуют полные геморрагические и анемические проявления. Качество жизни серьезно снижается. Летальные риски отмечаются, но пока сравнительно низкие. Показатели тромбо- и гранулоцитов находятся в пределах умеренного снижения.
- Тяжелая степень. Клиника полная, есть реальные риски смерти.
Это крайняя фаза, она же терминальная. Наблюдаются массивные нарушения работы организма, критические осложнения влекут за собой смерть пациента. Не всегда эффект дают даже полные лечебные мероприятия.
Второй способ классификации — по характеру заболевания.
Выделяют:
- Врожденную форму. Часто обнаруживаются генетические дефекты в качестве непосредственного фактора-виновника нарушения. У детей и молодых людей до 25 лет манифестация диагноза наблюдается наиболее часто. Второй пик приходится на период после 50, но уже гораздо реже.
- Приобретенную форму апластической анемии. Встречается почти в 80% случаев. Становится результатом заболеваний. В том числе онкологических, эндокринных расстройств и других возможных.
Используется классификация по агрессивности и характеру течения:
- Острая форма. Сопровождается резким падением количества форменных клеток крови, выраженной клинической картиной. Наиболее часто встречается именно этот тип процесса. О нем говорят в том случае, если симптоматический комплекс наблюдается в течении до 1 месяца.
- Подострая форма. От 30 дней до полугода. Сопровождается относительно вялой клинической картиной. Однако опасность от этого меньше не становится.
- Хронический тип. Длительность свыше 6 месяцев.
Наконец, классифицировать заболевание можно по происхождению, этиологии.
Соответственно называют:
- Первичное расстройство. Обусловлено генетическими дефектами. Присутствует с человеком явно или скрыто с самого рождения.
- Вторичная форма. Встречается в результате перенесенных прочих отклонений.
Не всегда врач с ходу и даже после тщательной диагностики может обнаружить причины патологического процесса, в такой ситуации говорят об идиопатической апластической анемии.
По мере дальнейшего обследования возможен пересмотр диагноза. В зависимости от итогов диагностики.
Симптомы
Клиническая картина определяется двумя основными синдромами. Первый — собственно анемический. Результат недостаточного питания тканей организма, также кислородного голодания.
Проявления таковы:
- Слабость. Астенические явления — это симптомы апластической анемии, которые присутствуют на протяжении всего периода течения патологического процесса. Восстановление спонтанное.
- Одышка. После незначительной физической нагрузки. Также в состоянии полного покоя.
- Тахикардия. Увеличение частоты сердечных сокращений до 120-150 ударов в минуту. Независимо от текущего положения тела, характера активности (или ее отсутствия).
- Тошнота, рвота. Временные явления. Переносятся пациентом тяжело. Возникают периодически.
- Головная боль. Интенсивность может быть самой разной. Локализация также. Сопровождается прочими неврологическими проявлениями. В том числе со стороны органов зрения.
- Мерцание мушек в глазах. Фотопсии. Ложное ощущение света в поле видимости. Результат раздражения затылочной доли мозга, ирритации коры и недостаточного кислородного обеспечения.
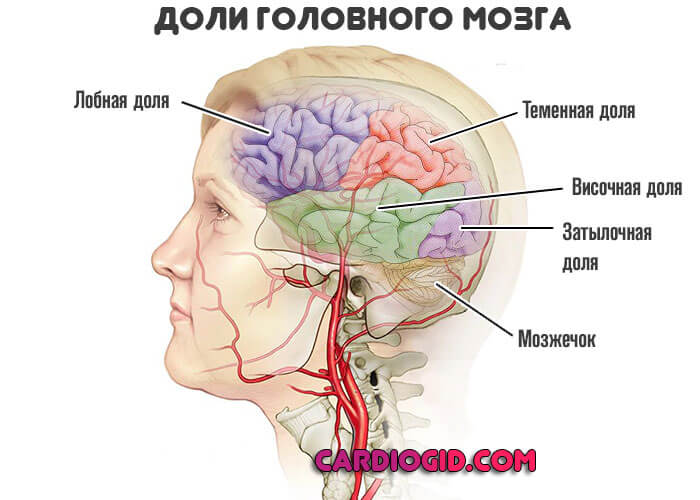
- Головокружение. Нарушение нормальной ориентации в пространстве, также координации движений.
- Сонливость. В течение дня. Независимо от количества часов отдыха в сутки. В ночное время возможен обратный эффект.
- Общее снижение работоспособности.
- Когнитивные нарушения. Падение качества и скорости мышления, памяти. Временное расстройство.
- Обморочные состояния. Особенно после вставания с места и перемены положения тела в пространстве.
Второй синдром в рамках диагноза — геморрагический. Сопровождается типичными признаками:
- Частые инфекционные поражения. В результате нарушения работы защитных сил организма. Регулярно возникают острые респираторные заболевания. Кроме того, повышаются риски приобретения опасных расстройств по типу ВИЧ, туберкулеза. Сопротивляемость существенно падает.
- Носовые кровотечения. В результате снижения концентрации тромбоцитов, которые ответственны за нормальную свертываемость. Повышается проницаемость капилляров, их ломкость.
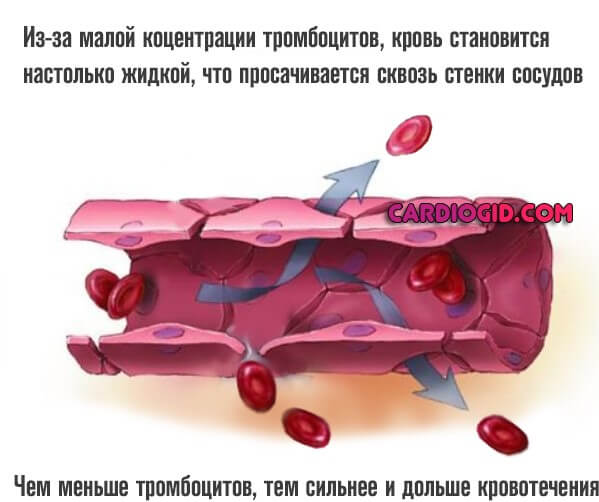
- Меноррагия. Расстройство менструального цикла. Обильные месячные возникают у каждой второй больной женщины. В том числе возможны и вне циклических изменений. Спонтанно.
- Стоматиты. Нарушения целостности слизистых оболочек органов, полости рта, носа. Образование язв, прочих дефектов.
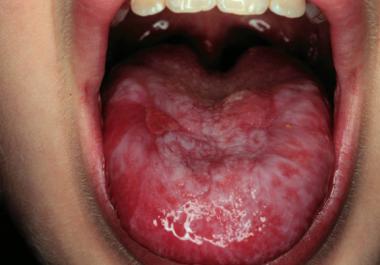
- Увеличение размеров селезенки. Вплоть до критического состояния с разрывом органа, массивным кровотечением и потенциальной вероятностью гибели пациента от осложнений. Сепсиса.
- Общее снижение иммунитета. Сказывается инфекционными поражениями, прочими состояниями.
- Высыпания на коже. Петехии (небольшие красные пятна), сосудистые звезды, гематомы, синяки — характерные признаки апластической анемии. Возникают из за малой концентрации тромбоцитов в крови.
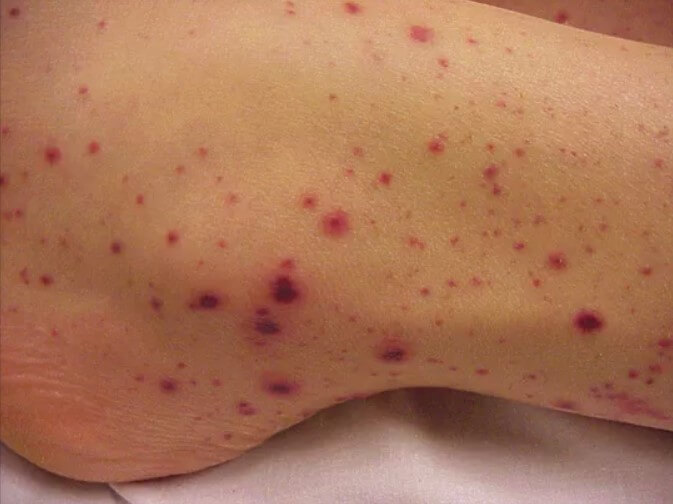
Аплазия костного мозга потенциально смертельное расстройство, симптоматика нарастает постоянно, по мере прогрессирования патологического процесса. Восстановление должно быть срочным.
Причины
Факторы становления множественны. Среди непосредственных виновников можно назвать:
- Перенесенные инфекционные расстройства. Гепатит разных видов, туберкулез, поражение герпетическими агентами.
- Применение некоторых лекарственных средств, как уже было сказано ранее.
- Облучение радиацией. В том числе при длительном воздействии небольших некритичных доз. Особенно подвержены этому расстройству работники АЭС, служащие на подлодках, прочие категории.
- Врожденные генетические аномалии.
- Доказана связь с беременностью. Однако специалисты пока не могут сказать, является ли гестация непосредственной причиной начала аномальных изменений в организме или же выступает провокатором манифестации расстройства.
- Заболевания лимфатической системы.
- Опухоли, особенно злокачественные.
Несмотря на всю эффективность диагностики, причины можно обнаружить не всегда. Примерно в 50% случаев речь идет об идиопатической разновидности анемии. Когда провокатора найти невозможно. По крайней мере, в момент выставления диагноза и его верификации.
Потребуется еще не одна неделя, а то и месяцы работы в этом направлении, динамическое наблюдение за состоянием больного.
Диагностика
Обследование представляет довольно серьезные трудности, поскольку надежных критериев пока нет, также врачи ограничены в выборе методик. Задача ложится на плечи гематолога.
Среди возможных мероприятий:
- Устный опрос больного. Нужно установить все присутствующие жалобы, чтобы составить полную клиническую картину. Это важно, поскольку позволяет выдвинуть гипотезы относительно состояния человека.
- Сбор анамнеза. Перенесенные ранее болезни, момент развития, начала симптоматических проявлений, вредные привычки, образ жизни, особенно важно установить семейную историю болезней.
- Общий анализ крови. Лабораторное исследование используется для оценки концентрации форменных клеток (эритроцитов), уровня гемоглобина, прочих показателей. Довольно информативная методика несмотря на простоту.
- Обязательно проводится исследование биохимическое. Оценке подлежат печеночные пробы, уровни специфических веществ: билирубина, щелочной фосфатазы.
- Хорошей методикой ранней диагностики и верификации диагноза выступает пункция костного мозга для забора материала (биопсия). Используется наиболее часто в качестве крайней меры. Ввиду инвазивности (травматичности) применяется не всегда.
- Возможно назначение консультации генетика. По показаниям.
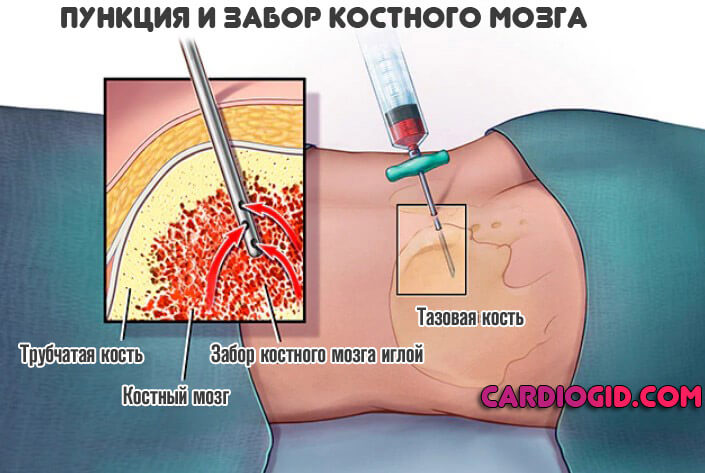
Диагностика требует терпения, хотя время на полное обследование есть не всегда. По мере дальнейшего или повторного курса возможен пересмотр изначально установленного заболевания.
Лечение
Эффективных медикаментозных методик практически нет. Основная задача — борьба с первопричиной, это может потребовать больших усилий.
Терапия в обязательном порядке проходит в стационаре. Пациента помещают в практически стерильные условия. Изолируют, чтобы не спровоцировать инфекционного поражения.
Практикуется несколько методов терапии анемии апластического типа:
- Влияние на иммунитет. Применяются препараты для коррекции работы защитных сил организма, обычно это иммуносупрессоры параллельно с гормонами.
- Переливание крови, а именно форменных клеток — тромбоцитарной и эритроцитарной массы. Мера временная, позволяющая восполнить дефицит этих телец. Переливание не делают при аутоиммунных заболеваниях.
- Возможно проведение плазмафереза. Очищения жидкой фракции крови, чтобы не провоцировать осложнения и замедлить прогрессирование патологического процесса.
Наиболее эффективный и, пожалуй, единственно действенный способ лечения апластической анемии в долгосрочной перспективе, это пересадка костного мозга. Ввиду малого количества совместимых доноров, велика вероятность длительного ожидания.
Речь идет о годах. Потому применение столь эффективной методики практикуется сравнительно редко.
На весь период лечения необходимо отказаться от курения, спиртного, прочих вредных привычек.
В целом же, устранение причины апластической анемии, ее симптомов — крупная проблема гематологии, задача восстановления решается с большим трудом.
Прогноз
Перспективы довольно туманны. Заболевание слишком серьезно для того, чтобы давать усредненные выкладки по прогнозу жизни. На вероятность выздоровления влияет группа факторов:
- Тяжесть патологического процесса, его агрессивности.
- Характер и длительность течения расстройства.
- Скорость прогрессирования.
- Семейная история.
- Возраст. Чем старше пациент, тем хуже в целом прогнозы. Хотя возможны и исключения.
- Наличие геморрагического синдрома.
- Присутствие и степень инфекционных осложнений.
Чем больше негативных факторов присутствует, тем меньше шансы на успешное восстановление.
В то же время нужно иметь в виду, что трансплантация костного мозга позволяет добиться положительного исхода почти в 90% случаев. Вопрос только в подборе донора.
Возможные осложнения
Среди последствия, с которыми встречаются пациенты:
- Выраженные массивные кровотечения. Потенциально летальные.
- Разрыв селезенки.
- Инвалидность, смертельный исход.
При остром течении прогнозы существенно хуже, меньше времени на реагирование, диагностику, помощь. Риски больше.
Угнетение костномозгового кроветворения (аплазия) провоцирует анемию, нарушение снабжения тканей организма, кислородом. Помимо этого, изменяются реологические свойства крови и присутствуют реальные угрозы смерти от осложнений.
Важно провести качественное лечение в условиях стационара. Основная проблема заключается в малом арсенале методик восстановления, курации.
Однако даже без возможности сиюминутной трансплантации есть все шансы устранения основных проявлений заболевания, поддержки организма. Это позволяет «протянуть» до подбора донора и коррекции.
Костномозговое кроветворение
Единственным кроветворным органом человека является костный мозг. Кроветворный костный мозг располагается в губчатых костях скелета и в эпифизах трубчатых костей. Кроветворный, или красный, костный мозг отличается обильной васкуляризацией. Его сосудистая сеть образуется двумя источниками: центральной артерией кости и множественными кортикальными артериями. Концевые капилляры этих двух сосудистых систем, соединяясь, образуют костномозговые синусы. Кроветворение происходит на костномозговых балках вне сосудистых синусов. Для проникновения в циркуляцию созревшие клетки крови должны преодолеть естественную преграду — стенку синуса, являющуюся барьером между кроветворным костным мозгом и циркуляцией.
Итак, единственным «домом» кроветворных клеток в организме человека является костный мозг. В том, что это так, убеждает весь опыт по пересадке костного мозга: введенные в вену кроветворные клетки донора в условиях приживления осаждаются и дают клоны кроветворных клеток только в костном мозге. Этот «эффект дома» обеспечивается так называемым стромалъным микроокружением кроветворного костного мозга. В морфологическом плане стромой костного мозга является выстилка костномозговых балок, на которой и располагаются островки кроветворных клеток. Состоит строма из клеток (фибробласты, жировые клетки, макрофаги и эндотелиальные клетки) и экстрацеллюлярного матрикса — продукта экскреции клеток стромы (фибронектин, коллаген, тромбоспондин, витронектин, ламинин, глюкозаминогликаны).
Экстрацеллюлярный матрикс обеспечивает прилипание кроветворных клеток, является средой их обитания. Стромальные клетки выделяют большое количество специфических регулирующих факторов, без которых невозможна пролиферация стволовых клеток, дальнейшая пролиферация, дифференцировка и функционирование их потомков. Индуктивная функция стромалъного микроокружения обеспечивается, по мнению одних авторов, клеточной кооперацией составляющих его элементов, по мнению других исследователей, ведущая роль в этом принадлежит фибробластам.
Кроветворение в костном мозге происходит островками, состоящими из клеток определенного вида. Рассмотрим и мы каждый росток кроветворения в отдельности.
В гранулоцитарном ростке способностью к делению обладают миелобласты, промиелоциты и миелоциты. В процессе созревания миелобласта в миелоцит клет-
ка проходит 4-6 митотических циклов, образует 16-64 миелоцита. Именно поэтому в костном мозге зрелых генераций закономерно больше, чем молодых.
Миелоцит обладает резервом «пролиферативной мощности». При обычном запросе на гранулоциты миелоцит до выхода из пролиферативного пула проходит 2 митотических цикла, но при повышенных требованиях (например, инфекция) число митозов в этой стадии дифференцировки может увеличиться до 4-х, что и создает дополнительную продукцию гранулоцитов. Кроме того, обычно часть миелоцитов выходит измитотического цикла в фазу временного покоя Go, создавая миелоцитарный костномозговой резерв. При повышении митотической стимуляции значительная часть этого резерва может снова вернуться в митотический цикл и, тем самым, быстро увеличить продукцию гранулоцитов.
Непролиферативный пул гранулоцитов имеет свои кинетические особенности: превратившись в палочко- и сегментоядерные элементы, они не спешат покинуть костный мозг, задерживаясь в нем на 5-7 дней. Зрелые гранулоциты костного мозга составляют так называемый гранулоцитарный костномозговой резерв, их число довольно значительно, в 2-3 раза превышает число молодых клеток и почти в 30 раз число циркулирующих. Этот резерв самый мощный и лабильный в организме. Быстрое развитие нейтрофилеза при бактериальных инфекциях (пневмония, аппендицит и др.) обусловлено быстрой мобилизацией костномозгового резерва. Нарастание сдвига формулы нейтрофи-лов периферической крови влево, особенно в сочетании с лейкопенией, является неблагоприятным прогностическим признаком, свидетельствующим об истощении этого резерва.
Основным событием эритропоэза является синтез гемоглобина, который начинается уже на стадии базофильного нормобласта. Количество гемоглобина контролирует синтез ДНК: чем больше гемоглобина в цитоплазме нормобласта, тем медленнее происходит синтез ДНК, который прекращается при содержании гемоглобина 27 пг в расчете на клетку. При нормобластическом эритро-поэзе содержание гемоглобина достигает 27 пг обычно на стадии оксифильно-го нормобласта, синтез ДНК прекращается, ядро становится пикнотичным, маленьким, выталкивается из клетки, после чего клетка переходит в следующую стадию — ретикулоцит. Таким образом полихроматофильные нормобласты — последняя генерация в эритропоэтическом ростке, способная к делению.
В нормальном эритропоэзе работает и другой механизм: в небольшом проценте клеток (около 5%) нарушается синхронизм в синтезе гемоглобина и ДНК, синтез ДНК происходит медленно, в результате чего клетка подходит к митозу
с содержанием гемоглобина, равным 27 пг, что блокирует митоз. Эти клетки не способны к дальнейшему нормальному развитию, обречены на гибель или образуют мегалоциты — гигантские эритроциты с резко укороченной продолжительностью жизни. Это явление получило название неэффективного эритропоэза, физиологическое значение его до конца неясно. Однако при дефиците витамина В12 и/или фолиевой кислоты удельный вес неэффективного эритропоэза резко увеличивается, красный росток становится мегалобластическим.
Тромбоцитопоэз отличается от образования других элементов крови. Мегака-риоцит — уникальная клетка, развивающаяся по эндомитотическому пути, т.е. митоз ядра не сопровождается разделением цитоплазмы. В результате такого эндо-митотического пути развития образуются клетки гигантского размера, многоядерные и полиплоидные (16-128 п), из их цитоплазмы образуются тромбоциты.
Итак, созрев в костном мозге, клетки должны проникнуть в циркуляцию. Как говорилось выше, кроветворение происходит вне костномозговых синусов, и, чтобы проникнуть внутрь, клетки крови должны преодолеть барьер в виде стенки сосудистого синуса. Эта преграда состоит из трех слоев: с внутренней стороны синуса — слой эндотелиальных клеток, затем базальная мембрана, к ним снаружи вплотную примыкают адвентициальные клетки и мегакариоциты. Под давлением растущих островков кроветворной ткани в эндотелиальных клетках временно образуются так называемые миграционные поры — узкие отверстия диаметром 1,0-1,2 мкм, через которые зрелые клетки проникают внутрь синусов. Для прохождения через такие узкие отверстия клетки должны обладать эластичной мембраной, способностью к деформации без повреждения и быстрому восстановлению формы. По-видимому, наличие этих свойств определяет зрелость клетки и избирательную способность к выходу ее из костного мозга. На пути к эн-дотелиальной стенке клеткам крови приходится проходить иногда и сквозь другие клеточные элементы, например, мегакариоциты. Такое прохождение одних клеточных элементов сквозь другие получило название эмпириополизиса. Физиологический смысл его пока еще изучен мало, не исключено, что в процессе эмпириополизиса клетки обмениваются некими сигналами, необходимыми для их метаболизма. Особое значение этот процесс имеет для эритропоэза. Зафиксировано, что в ряде случаев, именно во время эмпириополизиса оксифильных нормобластов через мегакариоциты и эндотелиальные клетки происходит их обезъядривание. Следует иметь ввиду, что образование тромбоцитов происходит внутри синусов при проникновении «псевдоподии» цитоплазмы мегакарио-цита через эндотелиальную стенку.
Судьба клеток, попавших в периферическую кровь, различна. Эритроциты осуществляют свои функции в циркуляции и заканчивают жизнь спустя 100-120 дней в ретикулогистиоцитарной системе преимущественно селезенки, подвергаясь фагоцитозу. Тромбоциты также живут и работают в русле крови.
Иная судьба у гранулоцитов и моноцитов. Функции этих клеток, основной из которых является фагоцитоз, связаны с пребыванием в тканях. По образному выражению Картрайта, они рождены в костном мозге, чтобы умереть в тканях. Периферическая кровь осуществляет их транспорт к тканям, пребывание их в циркуляции краткосрочно (от нескольких часов до 2-3 суток), выход из кровеносного русла случаен. В циркуляции гранулоцитов есть своя особенность: они разделены на 2 равных по объему пула — собственно циркулирующий и краевой пул,- между которыми происходит постоянный обмен.
Моноциты образуются из общего с гранулоцитами предшественника, но живут значительно дольше последних. Попадая в ткани, они превращаются в тканевые макрофаги, к которым, в частности, относятся свободные и фиксированные макрофаги лимфоузлов, селезенки и костного мозга, гистиоциты соединительной ткани, купферовские клетки печени, альвеолярные макрофаги легких, клетки Лангерганса кожи, остеокласты костной ткани, мик-роглия нервной ткани, дендритические клетки, плевральные и перитонеаль-ные макрофаги и др.
Т-лимфоциты окончательно созревают в тимусе. Зрелые Т- и В-лимфоциты расселяются соответственно по Т- и В-зависимым зонам лимфатических органов, периодически рециркулируют в крови и лимфе. Встретившись с антигеном, при взаимодействии с макрофагами и Т-хелперами, лимфоциты претерпевают процесс бласттрансформации, превращаются в иммунобласты, многократно делятся, созревают и превращаются в клетки-эффекторы иммунного ответа (Т-лимфоциты, которые осуществляют клеточный иммунитет, и плазматические клетки, обеспечивающие гуморальный иммунитет), а также клетки памяти. Продолжительность жизни В-лимфоцитов измеряется неделями, Т-лимфоцитов -месяцами, а клеток памяти — годами и десятками лет.
Таким образом клетки крови, образуясь в общем доме — костном мозге, имеют разную судьбу, различную длительность жизни и кинетику. При этом систему крови в целом характеризует большая лабильность при сохранении постоянства количественного и качественного состава ее отдельных звеньев. Это осуществляется путем четкой регуляции, основанной на принципах обратной связи: увеличение клеток в одном из звеньев гемопоэза приводит к адекватному сокращению их числа на предыдущем этапе. Регуляция пролиферации кле-
ток в костном мозге, их пребывания в костномозговом хранилище, выхода в циркуляцию, а оттуда в ткани происходит гуморальным путем.
В эритропоэзе универсальным регулятором является эритропоэтин, выделяемый почечной тканью, усиление его образования вызывается тканевой гипоксией. В тромбоцитопоэзе таким фактором является тромбопоэтин. В грануло-цитопоэзе регуляция изучена лучше, известны как стимуляторы пролиферации и активного функционирования лейкоцитов (колониестимулирующие факторы), так и ингибиторы их образования, выделение которых контролируется числом клеток в циркуляции.
Динамическое равновесие, характеризующее систему крови в целом, позволяет судить о её состоянии по исследованию количественного и качественного состава одного из звеньев. Наиболее доступным и простым для изучения является состав периферической крови (таблица 2). Без анализа крови не обходится ни одно обследование больного, ни один диагноз, это первый и необходимый шаг для оценки кроветворения. При обнаружении каких-либо изменений состава крови, наводящих на мысль о нарушении кроветворения, необходимо исследование пунктата костного мозга.
Апластическая анемия — причины, симптомы, диагностика и лечение

Апластическая анемия – угнетение функции кроветворения красного костного мозга (эритроцитопоэза, лейкопоэза и тромбоцитопоэза), приводящее к пангемоцитопении. К основным клиническим проявлениям гематологического синдрома принадлежат головокружение, слабость, обмороки, одышка, покалывание в груди, кожные геморрагии, кровотечения, склонность к развитию инфекционно-воспалительных и гнойных процессов. Заболевание диагностируется на основании характерных изменений гемограммы, миелограммы и гистологического исследования трепанобиоптата. Лечение патологии включает проведение гемотрансфузий, иммуносупрессивной терапии, миелотрансплантации.
Общие сведения
Апластическая (гипопластическая) анемия – тяжелое расстройство гемопоэза (чаще всех его звеньев), сопровождающееся развитием анемического, геморрагического синдромов и инфекционных осложнений. Развивается в среднем у 2 человек на 1 млн. населения в год. Приблизительно с одинаковой частотой патология поражает мужчин и женщин. Возрастные пики заболеваемости приходятся на возраст 10–25 и старше 50 лет. При данной патологии в костном мозге чаще нарушается образование всех трех типов клеточных элементов крови (эритроцитов, лейкоцитов и тромбоцитов), иногда — только одних эритроцитов; в зависимости от этого различают истинную и парциальную апластическую анемию. В гематологии данный вид анемии относится к числу потенциально фатальных заболеваний, приводящих к гибели 2/3 заболевших.

Апластическая анемия
Причины
По происхождению апластическая анемия может быть врожденной (связанной с хромосомными аберрациями) и приобретенной (развившейся в течение жизни). Принято считать, что угнетение миелопоэза связано с появлением в красном костном мозге и крови цитотоксических T-лимфоцитов, производящих фактор некроза опухолей и γ-интерферон, которые в свою очередь подавляют ростки кроветворения. Запускать этот механизм могут различные внешнесредовые (химические соединения, физические явления, лекарственные вещества), а также эндогенные факторы (вирусы, аутоиммунные реакции). К числу наиболее значимых причин относят:
- Прием миелотоксических препаратов. Достоверно установлена связь анемии с приемом некоторых противоопухолевых, противосудорожных, антибактериальных, антитиреоидных, противомалярийных препаратов, транквилизаторов, препаратов золота и др., обладающих потенциальным миелотоксическим эффектом. Лекарственные вещества могут вызывать как прямое повреждение стволовых кроветворных клеток, так и опосредованное — через аутоиммунные реакции. Анемии, связанные с таким механизмом развития, называются лекарственными.
- Контакт с химическими и физическими агентами. Супрессию костного мозга может вызывать взаимодействие с органическими растворителями, соединениями мышьяка, бензольными соединениями, пестицидами, облучение всего тела. В некоторых случаях недостаточность гемопоэза является временной и обратимой — главными факторами здесь являются концентрация/доза вещества и время контакта. супрессию костного мозга.
- Вирусные инфекции. Из вирусных агентов наибольшее значение уделяется возбудителям гепатитов В, С и D. В этом случае гипопластическая анемия обычно развивается в течение полугода после перенесенного вирусного гепатита. При изучении патогенеза было замечено, что репликация вируса происходит в мононуклеарах крови и костного мозга, а также в иммунных клетках. Предполагается, что подавление миелопоэза в этом случае является своеобразным иммунным ответом, возникающим против клеток, несущих на своей поверхности вирусные антигены. Такой вид анемии выделяется в отдельную форму – постгепатитную. Среди других вирусных инфекций называются ЦМВ, инфекционный мононуклеоз, грипп.
Также описаны случаи панцитопении, вызванные инфицированием туберкулезом, интоксикацией, лучевой болезнью, лимфопролиферативными заболеваниями (тимомой, лимфомой, хроническим лимфобластным лейкозом), беременностью. Почти в половине наблюдений причину анемии выявить не удается — такие случаи относят к идиопатической форме.
Патогенез
В основе апластической анемии может лежать либо первичное повреждение гемопоэтических стволовых клеток, либо нарушение их эффективной дифференцировки. При наследственных анемиях недостаточность гемопоэза опосредована кариотипическими аберрациями, приводящими к нарушению репарации ДНК и невозможности репликации стволовых клеток костного мозга. В случае приобретенной анемии под влиянием этиофакторов наблюдается активация Т-клеток, которые начинают продуцировать цитокины (интерферон-гамма, ФНО), поражающие клетки-предшественники гемопоэза. В стволовых клетках костного мозга повышается экспрессия генов, отвечающих за апоптоз и активизацию клеточной гибели. Основные клинические проявления обусловлены пангемоцитопенией – снижением в составе крови всех ее форменных элементов (эритроцитов, лейкоцитов, тромбоцитов).
Классификация
Кроме различных этиологических вариантов (лекарственного, постгепатитного, идиопатического), различают острую (до 1 мес. течения), подострую (от 1 до 6 мес.) и хроническую (более 6 мес.) форму заболевания. Анемию, протекающую с избирательным угнетением эритропоэза, называют парциальной красноклеточной аплазией. На основании выраженности тромбо- и гранулоцитопении данная форма анемии подразделяется на 3 степени тяжести:
- очень тяжелую (тромбоцитов менее 20,0х109/л; гранулоцитов менее 0,2х109/л)
- тяжелую (тромбоцитов менее 20,0х109/л; гранулоцитов менее 0,5х109/л), по данным трепанобиопсии – низкая клеточность костного мозга (менее 30% от нормы)
- умеренную (тромбоцитов более 20,0х109/л; гранулоцитов более 0,5х109/л)
Симптомы апластической анемии
Поражение трех гемопоэтических ростков (эритро-, тромбоцито- и лейкопоэза) обусловливает развитие анемического и геморрагического синдромов, инфекционных осложнений. Дебют апластической анемии обычно происходит остро. Анемический синдром сопровождается общей слабостью и утомляемостью, бледностью кожи и видимых слизистых, шумом в ушах, головокружением, покалыванием в груди, одышкой при нагрузке.
Основным проявлением тромбоцитопении выступает геморрагический синдром. Больные отмечают появление петехий и экхимозов на коже, повышенную кровоточивость десен, спонтанные носовые кровотечения, меноррагии. Возможно возникновение гематурии, маточных и желудочно-кишечных кровотечений. Следствием лейкопении и агранулоцитоза служит частое развитие инфекционных процессов – стоматитов, пневмоний, инфекций кожи и мочевыводящих путей. Для апластической анемий нехарактерны похудание, лимфаденопатия, гепато- и спленомегалия – при этих признаках следует искать другую причину пангемоцитопении.
Врожденная апластическая анемия (синдром Фанкони) обычно развивается у детей в возрасте до 10 лет и кроме аплазии костного мозга характеризуется другими нарушениями: микроцефалией, гипоплазией почек, низкорослостью, аномалиями развития верхних конечностей (гипоплазией первой пястной и лучевой кости), гипоспадией, гиперпигментацией кожи, крайней степенью тугоухости и др. При наследственной анемии Эстрена-Дамешека отмечается тотальное поражение кроветворения и панцитопения при отсутствии врожденных аномалий развития. Для анемии Даймонда-Блекфена или парциальной красноклеточной аплазии характерно только снижение количества эритроцитов.
Осложнения
Летальный исход может быть обусловлен кровоизлияниями во внутренние органы, массивными кровотечениями, инфекционными осложнениями, анемической комой. Наиболее грозное из геморрагических осложнений – кровоизлияние в головной мозг (геморрагический инсульт). Больные склонны к частым и тяжело протекающим вирусным и бактериальным инфекциям респираторного тракта. Значительное или стремительное снижение уровня красных кровяных телец может привести к анемической коме. При молниеносной форме крайне быстро развиваются тяжелейшая анемия, иммунодефицит, коагулопатии, имеющие фатальные последствия.
Диагностика
Оценка гематологического статуса включает внимательный клинический осмотр и проведение тщательной лабораторной диагностики. При физикальном обследовании выявляется выраженная бледность или желтушность кожи, артериальная гипотония, тахикардия. Основу диагностического алгоритма составляет проведение общего и биохимического анализа крови, стернальной пункции, трепанобиопсии:
- Исследования крови. Для гемограммы при гипопластической анемии типичны эритро-, лейкоцито- и тромбоцитопения, нейтропения и относительный лимфоцитоз. Оценка биохимических показателей (печеночных проб, нефрологического комплекса, сывороточного железа, билирубина) информативна для исключения других анемий.
- Исследование пунктата костного мозга. В миелограмме обнаруживается уменьшение количества миелокариоцитов и мегакариоцитов, снижение клеточности. В трепанобиоптате определяется замещение красного костного мозга жировым (желтым).
В рамках диагностического поиска апластическую анемию необходимо дифференцировать с мегабластными (В12-дефицитными, фолиеводефицитными) анемиями, идиопатической тромбоцитопенической пурпурой, пароксизмальной ночной гемоглобинурией, острым лейкозом.
Лечение апластической анемии
Больные с апластической анемией госпитализируются в специализированные отделения. Им обеспечиваются полная изоляция и асептические условия для предупреждения возможных инфекционных осложнений. Проведение эффективного лечения является сложной проблемой практической гематологии. В зависимости от уровня цитопении используются следующие лечебные подходы:
- Иммуносупрессиная терапия. При умеренной цитопении назначается фармакотерапия, включающая комбинацию антитимоцитарного иммуноглобулина и циклоспорина А. Поддерживающая терапия проводится анаболическими стероидами или их сочетанием с циклоспоринами.
- Гемотрансфузии. В комплексе с курсом иммуносупрессивной терапии при низких показателях красной крови показано проведение заместительной гемотрансфузионной терапии (переливание тромбоцитов и эритроцитарной массы), плазмафереза. Данная мера не оказывает воздействия на патогенетическое звено заболевания, но позволяет восполнить дефицит кровяных телец, не вырабатываемых костным мозгом.
- Трансплантация КМ и СК. Наиболее благоприятные прогнозы на долгосрочную выживаемость оказывает выполнение аллогенной трансплантации костного мозга. Однако ввиду сложности подбора иммунологически совместимого донора процедура используется ограниченно. В качестве экспериментальных подходов рассматриваются аутологичные трансплантации, пересадка стволовых клеток периферической крови. Больным с нетяжелой формой анемии может быть показано проведение спленэктомии, эндоваскулярной окклюзии селезеночной артерии.
Прогноз и профилактика
Прогноз определяется этиологической формой, тяжестью и остротой течения анемии. Критериями неблагоприятного исхода служат быстрое прогрессирование заболевания, тяжелый геморрагический синдром и инфекционные осложнения. После трансплантации костного мозга ремиссии удается достичь у 75–90% пациентов. Первичная профилактика данной разновидности анемии предполагает исключение влияния неблагоприятных внешнесредовых факторов, необоснованного применения лекарственных препаратов, предупреждение инфекционной заболеваемости и др. Пациентам с уже развившимся заболеванием требуется диспансерное наблюдение гематолога, систематическое обследование и длительная поддерживающая терапия.
113.Средства, угнетающие кроветворение.
Средства, угнетающие эритропоэз: Раствор натрия фосфата, меченного фосфором-32
Средства, угнетающие эритропоэз, используют при полицитемии (эритремии). Одним из таких средств является раствор натрия фосфата, меченного фосфором-32 (Na2h42P04). Применение его приводит к снижению числа эритроцитов, тромбоцитов. Вводят препарат внутрь или внутривенно. Дозируют в милликюри (мКи).
Средства, угнетающие лейкопоэз: Новэмбихин Меркаптопурин Допан Тиофосфамид. Средства, угнетающие лейкопоэз, применяют при лейкозах и лимфогранулематозе.
МИЕЛОСАН Оказывает угнетающее влияние на миелоидную ткань. Избирательно угнетает гранулоцитопоэз и дает антилейкемический эффект при хроническом миелолейкозе. Действие препарата проявляется преимущественно в уменьшении количества незрелых гранулоцитов.
114.Гемостатические средства.
ГЕМОСТАТИЧЕСКИЕ.
1)Коагулятны
1.1.Прямого действия: Тромбин, фибриноген, губка гемостатическая, губка антисептическая с канамицином, желпластан, кальция хлорид, кальция глюконат, протамин сульфат.
1.2.Непрямого дей-я: Викасол
2)Ингибиторы фибринолиза
2.1Спецефические: Контрикал=Гордокс
2.2.Неспецефические: Амбен= Е-аминокопроновая к-та
3)Агреганты: Серотонина адипинат, Хлорид Са
4)Повышающие вязкость крови: Желатиноль
5)Снижающие проницаемость сосудов
5.1.Синтетического происхождения: Дицинон, Вит С, Вит Р
5.2. Растительного происхождения: Трава лагохилуса опьяняющего, Листья крапивы, Трава тысячелистника, Кора калины, Цветки арники.
Для остановки или профилактики кровотечений используют также
•средство, повышающее вязкость крови — желатин- продукт гидролиза коллагена хрящей и костей животных, повышает вязкость и замедляет ток крови, способствует образованию тромбов
•Препараты аскорбиновой кислоты и рутина.
•Растения, обладающие гемостатнческим действием: зайцегуб опьяняющий, крапива, тысячелистник, водяной перец, кора калины, трава горца почечуйного, цветы арники.
•Для остановки кровотечений используют гемостатические губки с различными наполнителями:
1.Губка гемостатическая: нативная плазма + тромбопластин.
2.Губка коллагеновая: масса коллагеновая, р-р коллагена, борная кислота, левомицетин.
3.Губкаижелатиновая: обработанный желатин + фурациллин.
Прямые коагулянты
Тромбин — протеолитический фермент, получаемый из плазмы допоров.
•отщепляет от фибриногена боковые пептиды, превращая его в фибрин-мономер на поврежденной поверхности сосуда, а затем в фибрин-полимер.
•активирует ХШ фактор, превращающий полимер фибрина в стабильный фибриновый тромб.
ЭР-эритроциты
ФДЭ-фосфодиэстераза
•Активирует агрегацию Тр.
Применяют для остановки кровотечения местно при поверхностных, паренхиматозных геморрагиях, внутрь при желудочных кровотечениях, ингаляционно при кровотечении из дыхательных путей.
Следует исключить попадание в системный кровоток (распространенный тромбоз).
Хорошо сочетается с АКК и адроксоном.
Фибриноген — белок свертывающей системы, получают из донорской крови.
•под влиянием тромбина превращается в фибрин, составляющий основу тромба. Применяют
•местно в виде пленки для остановки! Кровотечения Можно вводить в системный кровоток (в/в)
•при гипо- и афибриногенемнн,
•во 2-3 стадию ДВС-снндрома
•для остановки кровотечения в хирургической, гинекологической практике
•профилактически подготовки больных с гипофибриногенемией к операции
Противопоказан при тромбозах, увеличении свертываемости крови, инфаркте миокарда.
Местно — на гнойных ранах и глубоких ожогах.
Коагулянты непрямого действия
Витамин К — объединенное название для группы производных нафтохинона.
Витамин К1-филлохинон содержится в зеленых частях растений: шпинат, цветная капуста, плоды шиповника, хвоя, корки апельсинов, зеленые томаты.
Витамин К2-менахинон. содержится в животной пище, синтезируется кишечной микрофлорой. В качестве лекарства применяют бисульфитное производное синтетического витамина КЗ- растворимое в воде — викасол (менадион), из него в печени образуются витамины КI и К2.
Фитомеиадион -синтетический аналог витамина К1.
Механизм действия: витамин К вызывает эффект только и организме, где существует в виде переходящих друг в друга гидрохинона, эпоксида и хинона. при переходе гидрохиноновой формы в эпоксидную витамин К активирует карбоксилазу, которая карбоксилирует остатки глутаминовой кислоты прокоагулянтов: II (протромбина), VII (проконвертина), IX, X факторов свертывания крови в эндоплазматической сети гепатоцитов. Только после карбоксилирования глютаминовой кислоты названные белки начинают функционировать. Без витамина К синтезируются неактивные белки, т.п. акарбокси факторы (акарбокси П является антагонистом активного протромбина).
Витамин К обладает антнгипоксантной активностью, облегчает синтез ЛТФ в митохондриях. стимулирует синтез альбуминов, миофибриллярных белков, фактора пластичности сосудов
Фармакокинетика. Викасол водорастворим, всасывается медленно, жир для всасывания не нужен. Эффект оказывает не сам викасол, а образующий из него витамин K1 и 2, поэтому эффект наступает позднее (через 24 часа), чем от фитоменадиона (через 10 час). Викасол вводят внутрь. в/в. и м. Фитоменадион назначают внутрь, всасывается быстро, для всасывания нужны жиры и желчь, назначают 3-4 раза в день.
Показания к применению.
•С профилактической целью викасол, фитоменадион назначают всем новорожденным (ГБН). Это понижает количество неврологических осложнении и летальных исходов, связанных с геморрагическими явлениями, т.к. у многих новорожденных, даже доношенных имеется дефицит витамина К.
•после заменного переливания консервированной крови,
•геморрагический синдром связанный с дефицитом витамина К, (обструкция желчных путей и нарушение всасывания витамина К, диарея),
•псевдогемофилия (врожденный дефицит П и УП факторов)
•для устранения кровотечении, связанных с применением АСК, химиотерапевтических средств, угнетающих микрофлору в кишечнике, непрямых антикоагулянтов
• мышечная слабость, атония кишечника. СН, вызванные применением антагонистов вит К: рахит.
Нежелательные эффекты:
• гемолиз эритроцитов (производные нафтохинона обладают выраженными окисляющими свойствами)
• образование метгемоглобина ( викасол не вводят более 3-х дней новорожденным.
• дисфункция тромбоцитов.
Викасол не назначают при гемолитической желтухе, тромбоцитопении. У Фитоменадиона этих осложнений нет.
Ингибиторы фибринолиза
АКК, амбен.
1.Эпсилон-аминокапроновая кислота — производное аминокислоты лизин, который содержится в молекуле фибриногена и фибрина, с ним взаимодействует плазминоген и плазмин, подвергая их гидролизу: АКК взаимодействуете активными центрами плазмина и плазминогена, устраняя их действие.
2.Блокирует активатор профибринолизина и нарушает его превращение в фибринолизин (плазмин). Это способствует сохранению фибринных тромбов, экономии белков ССК и остановке кровотечения, особенно при повышении активности системы фибринолиза, в условиях дефицита ССК.
3.Стимулирует тромбоцитопоэз, повышает чувствительность их рецепторов к агрегантам. В высоких дозах -дезагрегация.
4.АКК обладает также противошоковым действием (ингибирует протеолитические ферменты, стимулирует обезвреживающую функцию печени).
5.Ингибирует систему комплимента и может применяться при заболеваниях, связанных с образованием иммунных комплексов (гломерулонефрит), оказывает противоаллергическое, противовоспалительное, противовирусное действия.
Показания: применяется для остановки кровотечения при операционных вмешательствах, усилении активности фибринолитической системы, после операций на легких, предстательной, поджелудочной, щитовидной железах, преждевременном отслоении плаценты, заболеваниях печени, панкреатитах, переливании крови, внутрь при желудочных кровотечениях.
Нежелательные эффекты АКК(амокриновая кис-та):
• аллергические реакции (першение в горле, заложенность носа, сыпь)
• головокружение при быстром введении, ортостатическая гипотония, аритмия
• Тошнота, понос
• тромбозы, эмболии
• миопатии
Противопоказания к применению АКК: Склонность к тромбозам, заболевание почек. Амбен по ФД похож на АКК, активнее в 3-7 раз.
Фармакокинетика: вводят внутрь, предварительно растворив в сладкой воде, в/в капельно. в/м 4 раза в сутки. Хорошо всасывается в ЖКТ. Действие на фибринолиз сохраняется 1-3 дня. Хорошо сочетаем с тромбином и адроксоном, фибриногеном.
Ингибиторы протеаз природного происхождения.
Контрикал, пантрипин, нигитрил, гордокс — содержат апротинин, антиферментные препараты, полипептидной природы, получаемые из поджелудочной железы, легких убойного скота. Ингибирует активность трипсина, химотрипсина, калликреина, плазмина и других протеаз. в т.ч. гепарин. Поливалентная антипротеазная активность позволяет применять эти препараты при панкреатите, панкреонекрозе, для профилактики фибринолитических кровотечений ж/кишечных. И водят в/в канельно или струйно.
Нежелательные эффекты: Аллергические реакции, снижение АД, бронхоспазм, нарушения МК.
Средства, стимулирующие агрегацию и адгезию тромбоцитов.
Серотонин стимулирует серотониновые рецепторы на поверхности Т’Р, увеличивает приток Са+ и одновременно стимулирует агрегацию тромбоцитов, способствует набуханию тканей вокруг сосуда и его сдавление. Повышается реакции Тр на другие агреганты. Используется при геморрагиях. связанных с Гр-пен ней.
Нежелательные эффекты: Бронхоспазм, боли в животе, повышение АД, понос, головная боль.
Адроксон — метаболит адреналина, не стимулирует адренорецепторы в сосудах н повышает АД. Повышается плотность сосудистой стенки, стимулирует агрегацию тромбоцитов, взаимодействуя с адренорецепторами на поверхности TP, увеличивает концентрацию кальция, что, в конечном счете, активирует сократительный аппарат TP и способствует выделению агрегантов. Применяют местно, внутрь, п/к, при Тр-цитопенической пурпуре, паренхиматозных и капиллярных кровотечениях, кишечных кровотечениях, кожных геморрагиях.
Этамзилат (дицинон)- производное диоксибензола, ингибирует эффекты простациклина и увеличивает агрегацию ТР. уменьшает проницаемость сосудов, трансудацию и эксудацию жидкой части плазмы, уплотняет базальные мембраны, способствует полимерации гиалуроновой кислоты.
Способствует увеличению образования тромбопластина, повышает агрегацию тромбоцитов. Эффективен при капиллярном кровотечении, понижает опасность внутричерепного кровотечения, способствуя сохранению целостности сосуда. При повреждении сосудов не эффективен.