Синдром гиперкортицизма — Википедия
Синдро́м гиперкортици́зма (синдром Ице́нко — Ку́шинга, кушинго́ид, синдром Ку́шинга, англ. Cushing’s syndrome) — предклиническое состояние, при котором происходит длительное хроническое воздействие на организм избыточного количества гормонов коры надпочечников, независимо от причины, которая вызвала повышение количества этих гормонов в крови.
Синдромом Кушинга называют предклиническое состоянием с повышенным уровнем эндогенного кортизона. При дальнейшем повышении уровня секреции кортизона диагностируется болезнь Кушинга[1].
Синдром гиперкортицизма сопровождается следующими типичными проявлениями:
- нарушается обмен белков, жиров и углеводов;
- активируется распад белков, образуется избыточное количество свободных жиров в крови, повышается количество глюкозы в крови пациента, что может привести к развитию стероидного сахарного диабета.
Проявления и синдрома, и болезни Кушинга обусловлены избыточной секрецией гормонов коры надпочечников, прежде всего глюкокортикоидов.
Один из видов синдрома, циклический синдром Кушинга или синдром периодического гиперкортицизма, характеризуется периодическим повышением уровня выработки кортизона и встречается чрезвычайно редко. Он диагностируется при обнаружении не менее трёх пиков секреции кортизона с промежуточными спадами. Это состояние сопровождается повышенным уровнем секреции адренокортикотропный гормона гипофизом[2].
Избыточная секреция кортизона нередко приводит к ожирению[2].
История[править | править код]
В 1912 году этот синдром описан американским врачом Харви Кушингом, который назвал его англ. polyglandular syndrome[3], и независимо от него в 1924-м одесским неврологом Николаем Михайловичем Иценко. Просуммировав свои наблюдения в 1932 году, Кушинг опубликовал работу «Базофильные аденомы гипофиза и их клинические проявления»
Причиной синдрома Кушинга могут быть различные состояния. Чаще всего синдром гиперкортицизма (избыточное образование гормонов коры надпочечников) бывает обусловлен повышенной выработкой адренокортикотропного гормона гипофиза (болезнь Иценко — Кушинга). Этот гормон может вырабатываться микроаденомой гипофиза или эктопированной (расположенной не на обычном месте) кортикотропиномой. Эктопированная злокачественная кортикотропинома может располагаться в бронхах, яичках, яичниках.
Реже синдром Кушинга возникает при первичном поражении коры надпочечников (доброкачественные или злокачественные опухоли коры надпочечников, гиперплазия коры надпочечников). Гормонально-активная опухоль коры надпочечника называется кортикостерома. Она продуцирует в кровь избыточное количество глюкокортикоидов. При этом из-за избыточного количества глюкокортикоидов в крови снижается количество адренокортикотропного гормона гипофиза и оставшаяся ткань надпочечников подвергается атрофическим изменениям.
Синдром гиперкортицизма может возникнуть при поступлении глюкокортикоидов в организм извне, например, при длительном лечении различных заболеваний при помощи глюкокортикоидов, а также инъекциях глюкокортикоидных препаратов в область суставов и нервов, использовании некоторых кремов для кожи (включая отбеливающие), растительных препаратов, “тоников”, применении мегестрола ацетата (синтетического производного прогестерона с глюкокортикоидной активностью)
В основе патогенеза патологических изменений, которые развиваются при синдроме Кушинга со стороны большинства органов и систем, лежит в первую очередь гиперпродукция кортизола. Кортизол в нефизиологических концентрациях оказывает действие на белковые структуры и матрицы большинства тканей и структур (кости, мышцы, в том числе гладкие и миокард, кожа, внутренние органы и т. п.), в которых постепенно развиваются выраженные дистрофические и атрофические изменения. Нарушения углеводного обмена заключаются в стойкой стимуляции глюконеогенеза и гликогенолиза в мышцах и печени, что приводит к гипергликемии (стероидный диабет). Сложным образом меняется жировой обмен: на одних участках тела происходит избыточное отложение, а на других — атрофия жировой клетчатки, что объясняется разной чувствительностью отдельных жировых отделов к глюкокортикоидам. Важным компонентом патогенеза синдрома Кушинга являются электролитные расстройства (гипокалиемия, гипернатриемия), которые обусловлены влиянием избытка кортизола на почки. Прямым следствием этих электролитных сдвигов является артериальная гипертензия и усугубление миопатии, в первую очередь кардиомиопатии, которая приводит к развитию сердечной недостаточности и аритмиям. Иммуносупрессивное действие глюкокортикоидов обусловливает склонность к инфекциям.
Наиболее частым вариантом синдрома Кушинга, с которым сталкиваются врачи большинства специальностей, является экзогенный синдром Кушинга, который развивается на фоне терапии глюкокортикоидами.
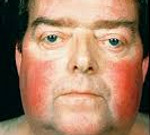
Наиболее ранним признаком болезни является ожирение, с типичным отложением жировой клетчатки в области лица, шеи, груди, живота. Лицо при этом выглядит округлым, лунообразным. На щеках появляется пурпурный румянец.
Глюкокортикоиды вызывают повышение аппетита и изменяют обмен веществ, увеличивая уровень глюкозы в крови и усиленное отложение жира. Конечности наоборот становятся тонкими из-за уменьшения массы мышечной ткани.
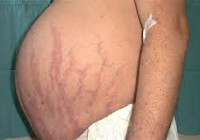
На коже в области живота, плечевого пояса, ягодиц и бедер появляются багрово-синюшные полосы растяжения — стрии. Это результат растяжения кожи при избыточном отложении жиров и нарушения обмена белка, из-за чего кожа истончается и легко растягивается. На коже появляются угревые высыпания. Раны и порезы заживают медленно.
В местах трения в области воротника на шее, в области живота, локтей возникает усиленная окраска кожных покровов. В этих местах откладывается меланин, количество которого увеличивается вместе с количеством адренокортикотропного гормона.
У женщин возникает гирсутизм (избыточное оволосение). Появляются волосы на верхней губе, подбородке, груди. Избыточный рост волос у женщин обусловлен усилением продукции мужских половых гормонов андрогенов корой надпочечников, что у женщин вызывает также нарушения менструального цикла. У мужчин возникает импотенция.
Вначале появляется периодическое, затем постоянное повышение артериального давления. Постепенно развивается разрежение костной ткани — остеопороз, который проявляется сначала болями в костях и суставах, затем могут возникнуть спонтанные переломы ребер, конечностей. Избыток глюкокортикоидов как вызывает нарушение образования белковой основы костей, так и усиливает выход кальция из костной ткани.
Пациенты жалуются на слабость, головные боли, увеличение массы тела. Иногда у больных болезнью с гиперкортицизмом возникают нарушения психики. Появляются депрессия, различные нарушения сна, психозы.
Цель лечения — нормализация уровня гормонов коры надпочечников в крови. Применяются препараты, снижающие продукцию гормонов в коре надпочечников — кетоконазол, мамомит — в течение длительного времени.
В некоторых случаях применяется дексаметазон с целью угнетения функции коры надпочечников[2].
Проводится симптоматическое лечение, направленное на коррекцию нарушений белкового и углеводного обмена, нормализацию уровня артериального давления, лечение сердечной недостаточности. При наличии у пациента кортикостеромы, производится одностороннее удаление надпочечника (односторонняя адреналэктомия).
- ↑ 1 2 The diagnosis of Cushing’s syndrome : an Endocrine Society Clinical Practice Guideline // The Journal of Clinical Endocrinology and Metabolism. |volume=93 |issue=5 |pages=1526—1540 |pmid=18334580 |pmc=2386281 |doi=10.1210/jc.2008-0125 |язык=en |автор=Nieman |автор имя=L. K. |автор2=Biller |автор2 имя=B. M. |автор3=Findling |автор3 имя=J. W. |автор4=Newell-Price |автор4 имя=J. |автор5= M. O. Savage, P. M. Stewart, V. M. Montori |месяц=5 |год=2008}}
- ↑ 1 2 3 M. Alberich, Ruano. Cyclic Cushing’s syndrome due to occult ectoric ACTH secretion : [англ.] / Ruano M. Alberich, M. Boronat Cortés, C. Rodriguez Perez … [] // Endocrine Abstracts. — 2012. — Vol. 29. — P. 359. — ISSN 1479-6848.
- ↑ The Pituitary Body and its Disorders. Clinical States produced by Disorders of the Hypophysis Cerebri. Philadelphia, J. B. Lippincott, 1912.
- ↑ Papers Relating to the Pituitary Body, Hypothalamus and Parasympathetic Nervous System. Springfield Illinois, C. C. Thomas, 1932
- ↑ Cushing Syndrome (англ.). NORD. National Organization for Rare Disorders (2017). Дата обращения 10 ноября 2019.
- ↑ Kinns, H. Munchausen syndrome and factitious disorder : the role of the laboratory in its detection and diagnosis : [англ.] / H. Kinns, D, Housley, D. B. Freedman // Annals of Clinical Biochemistry (англ.)русск.. — 2013. — Vol. 50, no. Pt. 3 (May). — P. 194—203. — doi:10.1177/0004563212473280. — PMID 23592802.
- ↑ Синдром Кушинга | Эндокринология — aorta.ru | заболевания, медицина, здоровье, болезни, секс
| Нозологии |
| ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Гормоны и медиаторы | Белковые гормоны: Пептидные гормоны: АКТГ, СТГ, Меланоцитостимулирующий гормон, Пролактин, Паратгормон, Кальцитонин, Инсулин, Глюкагон;
| ||||||||||||||||||
классификация, причины, симптомы, диагностика, лечение заболевания и его профилактика
Гиперкортицизм — эндокринное заболевание, характеризующееся достаточно долгим воздействием на организм человека сверхнормативного количества кортизола — гормона синтезируемого надпочечниковой корой, либо злоупотреблением глюкокортиокидами. Другое название гиперкортицизма — синдром Иценко Кушинга.
Женщины в 10 раз чаще мужчин страдают гиперкортицизмом, и, в основном, в возрасте от 25 до 40 лет.
Гиперкотицизм проявляется тем, что кортизол в больших количествах замедляет выработку глюкозы, которая очень необходима нашим клеткам. В результате этого, функциональность многих клеток падает и наблюдается атрофирование тканей.
Гиперкортицизм: причины
Причин, вызывающих гиперкортицизм, несколько и самой распространенной из них является болезнь Иценко Кушинга (не путать с одноименным синдромом).
В этом случае происходит сверхнормативное продуцирование АКТГ (адренокортикотропного гормона), который, активизирует секретирование кортизола. Этим характеризуется эндогенный гиперкортицизм.
Экзогенный гиперкортицизм возникает вследствие длительного применения глюкокортикоидов для терапии какого-нибудь системного заболевания, к примеру, ревматоидного артрита, либо астмы.
Иногда возникает, так называемый, псевдо-синдром Кушинга, который проявляет все признаки гиперкортицизма, но на самом деле, таковым не является. Причинами таких патологических проявлений могут являться:
— ожирение;
— алкогольная интоксикация;
— стресс и депрессия;
— беременность…
Гиперкортицизм: симптомы
У 90% больных гиперкортицизмом наблюдается ожирение по кушингоидному типу: неравномерные жировые отложения на лице (лицо лунообразное), плечах, шее, животе на фоне худых конечностей — этот тип ожирения ни с каким другим не спутаешь.
На плечевом поясе и особенно на ногах заметна атрофия мышц и это сопровождается постоянной слабостью и быстрой утомляемостью. На фоне ожирения, мышечная атрофия создает больному гиперкортицизмом большие трудности в процессе любых физических нагрузок.
У женщин гиперкортицизм проявляется:
— гирсутизмом;
— вирилизацией;
— гипертрихозом;
— сбоем менструальных циклов;
— аминореей и бесплодием.
Мужской гиперкортицизм проявляется проблемами в половой системе: снижением потенции и либидо, атрофией яичек и гинекомастией.
Так же, гиперкотицизм может проявить себя сбоями нервной и сердечно-сосудистой систем.
«Нервные» симптомы:
— психозы и стрессы;
— смена эйфорического состояния депрессией;
— заторможенность;
— суициидальные попытки.
Сердечно-сосудистые симптомы:
— аритмия сердца;
— артериальная гипертония;
— сердечная недостаточность.
Явным симптомом гиперкортицизма является «мраморность» кожи, ее сухость и наличие стрий, через кожу становится хорошо виден «рисунок» сосудов, часто появляются высыпания и кровоизлияния.
Гиперкортицизм: осложнения
Одним из самых опасных осложнений гиперкортицизма является адренолиновый криз, который проявляется:
— нарушением сознания;
— рвотой и высоким давлением;
— гиперкалиемией;
— гипонатриемией;
— гипогликемией;
— болями в животе;
— метаболическим ацидозом.
Так же, гиперкортицизм вызывает осложнения в сердечно-сосудистой системе и в функциональности почек, что нередко приводит к летальным исходам:
— декомпенсация сердечной деятельности;
— ишемический инсульт;
— почечная недостаточность;
— тяжелый пиелонефрит;
— сепсис;
— остеопороз;
— мочекаменная болезнь.
Кроме всего прочего, гиперкортицизм бывает причиной преждевременного прерывания беременности (выкидыш), вызывает проблемы с кожей (грибки, нагноения, фурункулы), а так же стероидный сахарный диабет (без повреждения поджелудочной железы).
Гиперкортицизм: диагностика
При диагностике гиперкортицизма, в первую очередь, проводят скрининговые тесты — определяют уровень кортизола в моче в течение суток. Если этот уровень выше нормы в 3-4 раза, то это показатель болезни Иценко Кушинга или гиперкортицизма.
Малая дексаметазоновая проба показывает, что если при приеме дексаметазона происходит снижение уровня кортизола более, чем в половину, то это — норма, а если этого снижения не наблюдается, то это говорит о наличии гиперкортицизма.
Для дифференциации болезни Иценко Кушинга и гиперкортицизма проводят большую дексаметозную пробу: при болезни происходит снижение уровня кортизола более чем в 2 раза, а при гиперкортицизме этого не происходит.
Для обнаружения источника патологии прибегают к инструментальной диагностике. Для этого случая самыми эффективными диагностическими методами являются магнитно-резонансная и компьютерная томографии гипофиза и надпочечников.
Для выявления осложнений гиперкортицизма применяют:
— рентгенографию;
— биохимический анализ крови.
Гиперкортицизм: лечение
Выбор метода лечения этой патологии зависит от многих факторов: от причины ее возникновения, иммунного статуса пациента…
При обнаружении опухолей надпочечников, легких, гипофиза, как правило, прибегают к их удалению хирургическим методом, либо к лучевой терапии.
При лекарственной природе гиперкортицизма постепенно заменяют применение глюкокортикоидов на другие лечебные препараты иммунодепрессивного действия.
При эндогенной (внутренней природе) заболевания применяют препараты, которые подавляют стероидогенез:
— кетоконазол;
— хлодитан;
— митотан;
— аминоглютетимид.
Для лечения симптоматики гиперкортицизма применяют различные мочегонные препараты, сердечные гликозиды, сахароснижающие средства, антидепрессанты…
Внимание!
Все эти методы лечения гиперкортицизма имеют один очень большой недостаток: они подавляют иммунную систему человека, вызывают достаточно тяжелые побочные эффекты, которые так же негативно сказываются на иммунитете человека. А ведь иммунная система — это единственный «фундамент», на который может опереться организм при борьбе с различными заболеваниями и именно ее сбои лежат в основе любой патологии. И поэтому лечащий врач всегда сталкивается с очень непростой задачей: как вылечить человека и при этом «не потерять» его иммунный статус, иначе все результаты терапии, в конечном итоге, станут бесполезными.
Для решения этой важнейшей задачи, в комплексной терапии гиперкортицизма применяют иммунный препарат Трансфер фактор.
Основу этого препарата составляют одноименные иммунные молекулы, которые, попадая в организм, выполняют три функции:
— устраняют сбои эндокринной и иммунной систем, и способствует их дальнейшему нормальному развитию и формированию;
— являясь информационными частицами (той же природы, что и ДНК), трансферфакторы «записывают и хранят» всю информацию о чужеродных агентах — возбудителях различных заболеваний, которые (агенты) вторгаются в организм, и при повторном их вторжении, «передают» эту информацию иммунной системе, которая нейтрализует эти антигены;
— устраняют все побочные явления, вызываемые применением других лекарственных препаратов одновременно усиливая их терапевтический эффект.
Имеется целая линейка этого иммуномодулятора, из которой Трансфер фактор Эдванс и Трансфер фактор Глюкоуч используются в программе «Эндокринная система» для профилактики и комплексного лечения эндокринных заболеваний, в т.ч. и гиперкортицизма.
Что это такое гиперкортицизм — причины, дигностика, симптомы, лечение у женщин, мужчин, детей
Общая информация
Клиническая картина заболевания была описана одновременно двумя учеными — Николаем Иценко и Харви Кушингом, благодаря чему патология получила название «болезнь, или синдром, Иценко-–Кушинга».
Гиперкортицизм — широкое понятие, в которое входит комплекс различных состояний. Наиболее распространенными являются болезнь и синдром Иценко-–Кушинга. В первом случае патология обусловлена нарушениями в гипоталамо-гипофизарной системе. Чаще всего это аденома гипофиза — небольшая, доброкачественная опухоль, продуцирующая адренокортикотропный гормон. Во втором — изменения касаются непосредственно надпочечников. Чаще всего это аденомы и аденокарциномы.
В 1–2% случаев нозология провоцируется АКТГ-эктопированным синдромом — гормонально активной опухолью, локализованной в легких, тимусе, яичниках и яичках, железах внутренней секреции, поджелудочной и предстательной железе.
Лекарственная гиперкортицизм — патология, вызваная неправильным или нецелесообразным назначением кортикотропных гормонов.
Механизм развития болезни
В основе развития гиперкортицизма лежит повышенная секреция кортизола. Данный гормон провоцирует распад белков костей, мышц, кожи и внутренних органов. Со временем это приводит к дистрофии и атрофии тканей. Усиленная выработка глюкозы приводит к развитию стероидной формы диабета. Нарушение жирового обмена сопровождается характерным отложением жира в определенных зонах. Избыточная концентрация кортизола влияет и на почки. Как результат — в плазме крови повышается уровень натрия и снижается концентрация калия. Такие пациенты страдают от повышенного артериального давления, а в мышечной ткани усиливаются дистрофические процессы.
Сильнее всего при гиперкортицизме страдает миокард. Внешне это проявляется нарушением сердечного ритма, сердечной недостаточностью, кардиомиопатией.
Кроме того, кортизол угнетающе действует на иммунную систему. В результате пациенты становятся очень чувствительными к различного вида инфекциям.
Клиническая картина
Наиболее типичный симптом гиперкортицизма — ожирение. Этот признак выявляют у более чем 90% больных. Как правило, жир откладывается на лице, животе и спине. Конечности при этом остаются относительно худыми. Такое ожирение называют кушингоидным.
Лицо пациента по форме становится лунообразным, красного цвета с синюшным оттенком. Жир, отложенный в области седьмого шейного позвонка, создает так называемый бычий горб. Кожа тыльной стороны ладони становится истонченной, почти прозрачной.
Из-за атрофических процессов в мышцах развивается дисгормональная миопатия. Пациенты жалуются на снижение силы мышц, мышечную слабость, боль в мышцах. Характерными признаками болезни являются так называемые скошенные ягодицы и лягушачий живот, обусловленные гипотрофией мышц живота, бедер и ягодиц.
Кожа больных имеет специфический так называемый мраморный оттенок, склонна к шелушению и сухости. Сосудистый рисунок хорошо заметен. На плечах, в области груди, живота, ягодиц и бедер образуются багровые стрии — растяжки. Средняя их длина — 8 см, ширина — до 2 см. Отдельные участки кожи гиперпигментированы, наблюдаются акне, подкожные кровоизлияния.
Остеопороз — также частый симптом при гиперкортицизме. Костная ткань истончается, становится менее плотной, что приводит к сильному болевому синдрому, патологическим переломам, искривлению позвоночника. Из-за деформации позвоночного столба и сдавливания позвонков пациенты становятся сутулыми и ниже ростом.
Со стороны сердечной мышцы чаще всего наблюдается экстрасистолии, артериальная гипертензия, фибрилляция предсердий. Из-за атрофических процессов в миокарде развивается сердечная недостаточность. Это довольно серьезные нарушения, способные привести к летальному исходу.
При синдроме Иценко-–Кушинга страдает и центральная нервная система. Пациенты страдают от депрессии, стероидных психозов, делают попытки суицида.
Примерно у каждого десятого больного синдромом Иценко-–Кушинга развивается сахарный диабет, связанный с атрофическими процессами в поджелудочной железе. Характерная черта такого диабета — легкое течение. Длительное время у больных наблюдается нормальный уровень инсулина, а сама болезнь хорошо компенсируется диетой и препаратами, снижающими уровень сахара в крови.
У женщин может развиваться гиперандрогения — синдром, вызванный повышенным содержанием мужских половых гормонов. Она характеризуется нарушением менструального цикла, бесплодием, формирование вторичных половых признаков по мужскому типу.
![]() Узнайте экспертное мнение
Узнайте экспертное мнение
Оставьте свой e-mail и мы расскажем, как правильно обследоваться и приступить к лечению
Диагностика
Первое, что нужно сделать при появлении у больного признаков гиперкортицизма — подтвердить или опровергнуть повышенную продукцию кортизола надпочечниками. Для этого используют малую дексаметазоновую пробу.
Чаще всего ее выполняют по такому алгоритму:
- утром первого дня пациенту определяют уровень кортизола в сыворотке крови;
- в этот же день, в 24.00 больной принимает 1 мг дексаметазона внутрь;
- повторная проверка концентрации кортизола в сыворотке крови больного (утром следующего дня).
У здоровых лиц уровень кортизола снижается более чем в два раза, чего не происходит при гиперкортицизме.
Большая дексаметазоновая проба проводится в тех случаях, когда при малой не зафиксировалось должного подавления уровня кортизола, а также при необходимости провести дифференциальную диагностику между болезнью Иценко-–Кушинга и кортикостеромой, а также АКТГ-синдромом.
Способ проведения большой дексаметазоновой пробы отличается от малой только дозировкой препарата — вместо 1 мг больному советуют принять 8 мг препарата. При болезни Иценко-–Кушинга введения лекарства провоцирует снижение концентрации кортизола в сыворотке плазмы на 50%. При кортикостероме или АКТГ-синдроме показатель остается прежним. Это объясняется особенностями работы гипоталамуса и гипофиза.
Для выявления аденомы гипофиза проводят МРТ головного мозга. Кроме того, при подозрении на патологию показано КТ или МРТ надпочечников — на патологию указывает их двусторонняя гиперплазия. Эти же методы применяются для визуализации кортикостеромы, расположенной во внутренних органах.
Для диагностики осложнений болезни показаны биохимические исследования, рентгенография позвоночника и другие методики. Объем исследований определяется индивидуально, в зависимости от состояния пациента.
Лечение
Для лечения болезни применяются как консервативные, так и оперативные методы. Прежде всего, пациенту назначают средства, угнетающие синтез стероидов. Они эффективны при эндогенном характере заболевания.
Если при проведении магнитно-резонансной томографии удается четко визуализировать аденому гипофиза, показано ее оперативное удаление. В таком случае устойчивая ремиссия развивается у девяти из десяти больных. Если аденома не просматривается, пациенту рекомендуют протонотерапию на область гипофиза.
Основной метод лечение кортикостеромы — адреналэктомия. Иногда, особенно при тяжелом протекании болезни, проводится одностороннее удаление надпочечника. Это позволяет уменьшить выраженность симптомов заболевания.
Особую роль при данной патологии играет симптоматическое лечение. Как правило, больным рекомендуют лекарственные средства, снижающие АД, сахароснижающие, и медикаменты, предназначенные для терапии остеопороза. Для нормализации электролитного обмена назначают препараты калия.
Прогноз и профилактика
Прогноз при синдроме Иценко-–Кушинга зависит от таких факторов:
- своевременность диагностики и начала лечения;
- возраста пациента;
- индивидуальной реакции на терапию;
- первопричины заболевания.
При отсутствии адекватной терапии или неправильном лечении показатель смертности в первые пять лет с момента диагностики заболевания достигает 50%. Наиболее высока вероятность хорошего клинического исхода при кортикостероме, несмотря на то, что функция второго надпочечника восстанавливается только у восьми из 10 пациентов.
При злокачественной кортикостероме средний коэффициент пятилетней выживаемости не превышает 25%. Средняя продолжительность жизни при отсутствии лечения — один год и два месяца. Своевременная диагностика и ранее лечение значительно улучшают прогноз для жизни и здоровья больного.
Синдром Иценко-Кушинга (гиперкортицизм) — причины, симптомы, диагностика и лечение
Синдром Иценко-Кушинга – патологический симптомокомплекс, возникающий вследствие гиперкортицизма, т. е. повышенного выделения корой надпочечников гормона кортизола либо длительного лечения глюкокортикоидами. Следует отличать синдром Иценко-Кушинга от болезни Иценко-Кушинга, под которой понимают вторичный гиперкортицизм, развивающийся при патологии гипоталамо-гипофизарной системы. Диагностика синдрома Иценко–Кушинга включает исследование уровня кортизола и гипофизарных гормонов, дексаметазоновую пробу, МРТ, КТ и сцинтиграфию надпочечников. Лечение синдрома Иценко–Кушинга зависит от его причины и может заключатся в отмене глюкокортикоидной терапии, назначении ингибиторов стероидогенеза, оперативном удалении опухоли надпочечников.
Общие сведения
Синдром Иценко-Кушинга – патологический симптомокомплекс, возникающий вследствие гиперкортицизма, т. е. повышенного выделения корой надпочечников гормона кортизола либо длительного лечения глюкокортикоидами. Глюкокортикоидные гормоны участвуют в регуляции всех видов обмена веществ и многих физиологических функций. Работу надпочечников регулирует гипофиз путем секреции АКТГ — адренокортикотропного гормона, активизирующего синтез кортизола и кортикостерона. Деятельностью гипофиза управляют гормоны гипоталамуса — статины и либерины.
Такая многоступенчатая регуляция необходима для обеспечения слаженности функций организма и обменных процессов. Нарушение одного из звеньев этой цепи может вызвать гиперсекрецию глюкокортикоидных гормонов корой надпочечников и привести к развитию синдрома Иценко-Кушинга. У женщин синдром Иценко-Кушинга встречается в 10 раз чаще, чем у мужчин, развиваясь, преимущественно, в возрасте 25-40 лет.
Различают синдром и болезнь Иценко-Кушинга: последняя клинически проявляется той же симптоматикой, но в ее основе лежит первичное поражение гипоталамо-гипофизарной системы, а гиперфункция коры надпочечников развивается вторично. У пациентов, страдающих алкоголизмом или тяжелыми депрессивными расстройствами, иногда развивается псевдо-синдром Иценко-Кушинга.
Синдром Иценко-Кушинга (гиперкортицизм)
Причины и механизм развития синдрома Иценко-Кушинга
Синдром Иценко-Кушинга – широкое понятие, включающее комплекс различных состояний, характеризующихся гиперкортицизмом. Согласно современным исследования в области эндокринологии более 80% случаев развития синдрома Иценко-Кушинга связано с повышенной секрецией АКТГ микроаденомой гипофиза (болезнь Иценко-Кушинга). Микроаденома гипофиза представляет небольшую (не более 2 см), чаще доброкачественную, железистую опухоль, продуцирующую адренокортикотропный гормон.
У 14-18% пациентов причиной синдрома Иценко-Кушинга является первичное поражение коры надпочечников в результате гиперпластических опухолевых образований коры надпочечников – аденомы, аденоматоза, аденокарциномы.
1-2% заболевания вызывается АКТГ-эктопированным или кортиколиберин-эктопированным синдромом – опухолью, секретирующей кортикотропный гормон (кортикотропиномой). АКТГ-эктопированный синдром может вызываться опухолями различных органов: легких, яичек, яичников, тимуса, околощитовидных, щитовидной, поджелудочной, предстательной железы. Частота развития лекарственного синдром Иценко-Кушинга зависит от правильности применения глюкокортикоидов в лечении пациентов с системными заболеваниями.
Гиперсекреция кортизола при синдроме Иценко-Кушинга вызывает катаболический эффект — распад белковых структур костей, мышц (в том числе и сердечной), кожи, внутренних органов и т. д., со временем приводя к дистрофии и атрофии тканей. Усиление глюкогенеза и всасывания в кишечнике глюкозы вызывает развитие стероидной формы диабета. Нарушения жирового обмена при синдроме Иценко-Кушинга характеризуется избыточным отложением жира на одних участках тела и атрофией на других ввиду их разной чувствительности к глюкокортикоидам. Влияние избыточного уровня кортизола на почки проявляется электролитными расстройствами – гипокалиемией и гипернатриемией и, как следствие, повышением артериального давления и усугублением дистрофических процессов в мышечной ткани.
В наибольшей степени от гиперкортицизма страдает сердечная мышца, что проявляется в развитии кардиомиопатии, сердечной недостаточности и аритмий. Кортизол оказывает угнетающее действие на иммунитет, вызывая у пациентов с синдромом Иценко-Кушинга склонность к инфекциям. Течение синдрома Иценко-Кушинга может быть легкой, средней и тяжелой формы; прогрессирующим (с развитием всего симптомокомплекса за 6-12 месяцев) или постепенным (с нарастанием в течение 2-10 лет).
Симптомы синдрома Иценко-Кушинга
Наиболее характерным признаком синдрома Иценко-Кушинга служит ожирение, выявляемое у пациентов более чем в 90% случаев. Перераспределение жира носит неравномерный характер, по кушингоидному типу. Жировые отложения наблюдаются на лице, шее, груди, животе, спине при относительно худых конечностях («колосс на глиняных ногах»). Лицо становится лунообразным, красно-багрового цвета с цианотичным оттенком («матронизм»). Отложение жира в области VII шейного позвонка создает, так называемый, «климактерический» или «бизоний» горб. При синдроме Иценко-Кушинга ожирение отличает истонченная, почти прозрачная кожа на тыльных сторонах ладоней.
Со стороны мышечной системы наблюдается атрофия мышц, снижение тонуса и силы мускулатуры, что проявляется мышечной слабостью (миопатией). Типичными признаками, сопровождающими синдром Иценко-Кушинга, являются «скошенные ягодицы» (уменьшение объема бедренных и ягодичных мышц), «лягушачий живот» (гипотрофия мышц живота), грыжи белой линии живота.
Кожа у пациентов с синдромом Иценко-Кушинга имеет характерный «мраморный» оттенок с хорошо заметным сосудистым рисунком, склонна к шелушению, сухости, перемежается с участками потливости. На коже плечевого пояса, молочных желез, живота, ягодиц и бедер образуются полосы растяжения кожи – стрии багровой или цианотичной окраски, длиной от нескольких миллиметров до 8 см и шириной до 2 см. Наблюдаются кожные высыпания (акне), подкожные кровоизлияния, сосудистые звездочки, гиперпигментация отдельных участков кожи.
При гиперкортицизме нередко развивается истончение и повреждение костной ткани — остеопороз, ведущий к сильным болезненным ощущениям, деформации и переломам костей, кифосколиозу и сколиозу, более выраженных в поясничном и грудном отделах позвоночника. За счет компрессии позвонков пациенты становятся сутулыми и меньше ростом. У детей с синдромом Иценко-Кушинга наблюдается отставание в росте, вызванное замедлением развития эпифизарных хрящей.
Нарушения со стороны сердечной мышцы проявляются в развитии кардиомиопатии, сопровождающейся аритмиями (фибрилляцией предсердий, экстрасистолией), артериальной гипертензией и симптомами сердечной недостаточности. Эти грозные осложнения способны привести к гибели пациентов. При синдроме Иценко-Кушинга страдает нервная система, что выражается в ее нестабильной работе: заторможенности, депрессиях, эйфории, стероидных психозах, суицидальных попытках.
В 10-20% случаев в ходе заболевания развивается стероидный сахарный диабет, не связанный с поражениями поджелудочной железы. Протекает такой диабет довольно легко, с длительным нормальным уровнем инсулина в крови, быстро компенсируется индивидуальной диетой и сахароснижающими препаратами. Иногда развиваются поли- и никтурия, периферические отеки.
Гиперандрогения у женщин, сопровождающая синдром Иценко-Кушинга, вызывает развитие вирилизации, гирсутизма, гипертрихоза, нарушений менструального цикла, аменореи, бесплодия. У пациентов-мужчин наблюдаются признаки феминизации, атрофия яичек, снижение потенции и либидо, гинекомастия.
Осложнения синдрома Иценко-Кушинга
Хроническое, прогрессирующее течение синдрома Иценко-Кушинга с нарастающей симптоматикой может приводить к гибели пациентов в результате осложнений, несовместимых с жизнью: декомпенсации сердечной деятельности, инсультов, сепсиса, тяжелого пиелонефрита, хронической почечной недостаточности, остеопороза с множественными переломами позвоночника и ребер.
Неотложным состоянием при синдроме Иценко-Кушинга является адреналовый (надпочечниковый) криз, проявляющийся нарушением сознания, артериальной гипотензией, рвотой, болями в животе, гипогликемией, гипонатриемией, гиперкалиемией и метаболическим ацидозом.
В результате снижения резистентности к инфекциям у пациентов с синдромом Иценко-Кушинга нередко развиваются фурункулез, флегмоны, нагноительные и грибковые заболевания кожи. Развитие мочекаменной болезни связано с остеопорозом костей и выделением с мочой избытка кальция и фосфатов, приводящих к образованию оксалатных и фосфатных камней в почках. Беременность у женщин с гиперкортицизмом часто заканчивается выкидышем или осложненными родами.
Диагностика синдрома Иценко-Кушинга
При подозрении у пациента синдрома Иценко-Кушинга на основании амнестических и физикальных данных и исключении экзогенного источника поступления глюкокортикоидов (в т. ч. ингаляционного и внутрисуставного), в первую очередь выясняется причина гиперкортицизма. Для этого используется скрининговые тесты:
- определение экскреции кортизола в суточной моче: повышение кортизола в 3–4 раза и более свидетельствует о достоверности диагноза синдрома или болезни Иценко–Кушинга.
- малую дексаметазоновую пробу: в норме прием дексаметазона снижает уровень кортизола более чем в половину, а при синдроме Иценко-Кушинга снижения не происходит.
Дифференциальную диагностику между болезнью и синдромом Иценко-Кушинга позволяет провести большая дексаметазоновая проба. При болезни Иценко-Кушинга прием дексаметазона приводит к снижению концентрации кортизола более чем в 2 раза от исходного; при синдроме снижения кортизола не происходит.
В моче повышено содержание 11-ОКС (11-оксикетостероидов) и снижено 17-КС. В крови гипокалиемия, увеличение количества гемоглобина, эритроцитов и холестерина. Для определения источника гиперкортицизма (двусторонняя гиперплазия надпочечников, аденома гипофиза, кортикостерома) проводится МРТ или КТ надпочечников и гипофиза, сцинтиграфия надпочечников. С целью диагностики осложнений синдрома Иценко-Кушинга (остеопороза, компрессионных переломов позвонков, перелома ребер и т. д.) проводится рентгенография и КТ позвоночника, грудной клетки. Биохимическое исследование показателей крови диагностирует электролитные нарушения, стероидный сахарный диабет и др.
Лечение синдрома Иценко-Кушинга
При ятрогенной (лекарственной) природе синдрома Иценко-Кушинга необходима постепенная отмена глюкокортикоидов и замена их на другие иммунодепрессанты. При эндогенной природе гиперкортицизма назначаются препараты, подавляющие стероидогенез (аминоглютетимид, митотан).
При наличии опухолевого поражения надпочечников, гипофиза, легких проводится хирургическое удаление новообразований, а при невозможности – одно- или двусторонняя адреналэктомия (удаление надпочечника) или лучевая терапия гипоталамо-гипофизарной области. Лучевую терапию часто проводят в комбинации с хирургическим или медикаментозным лечением для усиления и закрепления эффекта.
Симптоматическое лечение при синдроме Иценко-Кушинга включает применение гипотензивных, мочегонных, сахароснижающих препаратов, сердечных гликозидов, биостимуляторов и иммуномодуляторов, антидепрессантов или седативных средств, витаминотерапию, лекарственную терапию остеопороза. Проводится компенсация белкового, минерального и углеводного обмена. Послеоперационное лечение пациентов с хронической надпочечниковой недостаточностью, перенесших адреналэктомию, состоит в постоянной заместительной гормональной терапии.
Прогноз синдрома Иценко-Кушинга
При игнорировании лечения синдрома Иценко-Кушинга развиваются необратимые изменения, приводящие к летальному исходу у 40-50% пациентов. Если причиной синдрома явилась доброкачественная кортикостерома, прогноз удовлетворительный, хотя функции здорового надпочечника восстанавливаются только у 80% пациентов. При диагностике злокачественных кортикостером прогноз пятилетней выживаемости – 20-25% (в среднем 14 месяцев). При хронической надпочечниковой недостаточности показана пожизненная заместительная терапия минерало- и глюкокортикоидами.
В целом прогноз синдрома Иценко-Кушинга определяется своевременностью диагностики и лечения, причинами, наличием и степенью выраженности осложнений, возможностью и эффективностью оперативного вмешательства. Пациенты с синдромом Иценко-Кушинга находятся на динамическом наблюдении у эндокринолога, им не рекомендуются тяжелые физические нагрузки, ночные смены на производстве.
Синдром гиперкортицизма, и что его вызывает
Синдром Кушинга (он же «синдром гиперкортицизма» или «синдром Иценко-Кушинга») — это состояние, при котором ваш организм по той или иной причине вырабатывает слишком много кортизола. Последствия такого дисбаланса могут быть очень неприятными и включать в себя нарушение обменных процессов и высокие риски развития диабета.
Мы расскажем, почему так происходит, как понять, что вы не в порядке, и объясним, чем отличается синдром Кушинга от одноименной болезни.
Причины
Кора ваших надпочечников умеет вырабатывать несколько очень важных гормонов, и один из них — кортизол. Сочетание ряда факторов может привести к высокому уровню этого гормона и проявлению соответствующих симптомов. Причины могут показаться немного запутанными, но мы постараемся все прояснить.
Болезнь Кушинга
Одной из основных причин синдрома Кушинга является болезнь Кушинга (на нее приходится семь случаев из десяти). Это редкое состояние возникает, когда аденома гипофиза избыточно продуцирует адренокортикотропный гормон (АКТГ). Он, в свою очередь гиперстимулирует кору надпочечников, что вызывает синдром.
Врачи не знают точно, почему возникает аденома гипофиза, но предполагают генетическую предрасположенность. Также существует определенная связь между появлением аденомы, травмами головы и воспалительными процессами в мозге. Женщин среди больных 70%, и у них заболевание часто диагностируется после родов.
Синдром Кушинга
Иногда причиной синдрома гиперкортицизма является не болезнь, а прием стероидных лекарственных препаратов, влияющих на гормональные уровни. Иногда на уровень кортизола влияют опухоли надпочечников и некоторые гормонопродуцирующие виды рака.
Синдром псевдо-Кушинга
Иногда симптомы показывают на синдром Кушинга, но причины состояния другие. Такое случается при избыточном потреблении алкоголя, ожирении, постоянно повышенном уровне глюкозы крови, при беременности и даже депрессии.
Как это работает?
Наша эндокринная система довольно сложная. Она включает в себя надпочечники, гипофиз, поджелудочную, щитовидную и паращитовидные железы, яичники и яички. Одни гормоны влияют на выработку других, те — на продуцирование третьих, и так далее.
Гормон кортизол, производимый надпочечниками, регулирует то, как наше тело превращает белки, жиры и углеводы из пищи в энергию. Он также отвечает за кровяное давление, уровень глюкозы, работу иммунной системы и нашу реакцию на стресс. Если уровень кортизола слишком высок, меняется аппетит, сахара в крови становится слишком много, а жир откладывается в усиленном режиме.
Какой бывает синдром Кушинга?
Экзогенный
Само это слово подразумевает, что причина состояния находится вне организма, и, в данном случае, это длительный прием кортикостероидных лекарств, по функционалу родственных кортизолу. Вот эти препараты:
- преднизолон
- дексаметазон
- метилпреднизолон
Такие лекарства обычно принимают люди с ревматоидным артритом, волчанкой, астмой, с болями в суставах и спине. Высокие дозы кортикостероидов назначают также после пересадки органов.
Не все стероидные лекарства несут с собой риски. Если вы лечите экзему кремами или используете ингалятор от астмы, опасности развития синдрома Кушинга для вас нет.
Эндогенный
Такой тип синдрома предполагает, что причина внутри организма, и надпочечники безобразничают по собственной воле. Мы уже рассказывали о болезни Кушинга, но причины могут быть и в опухолевых образованиях других органов.
Симптомы
У разных людей могут проявляться различные симптомы, и вариативность сильно зависит от причин, вызвавших синдром Кушинга.
Ключевой симптом — это увеличение веса. Высокий уровень кортизола приводит к перераспределению жира, особенно в области груди и живота.
Лицо округляется, щеки пылают румянцем. Руки и ноги нередко остаются тонкими, а жировая ткань скапливается на плечах и задней части шеи.
Другие общие признаки и симптомы:
- истончение кожи
- возникновение свежих растяжек на коже, розовых или фиолетовых
- легкость образования синяков
- высокое кровяное давление
- остеопороз и повышенная хрупкость костей
- мышечная слабость
- изменение или прекращение менструального цикла
- проблемы с фертильностью
Синдром Кушинга отображается и на состоянии кожи:
- на лице и теле появляется угревая сыпь
- кожа на шее, животе и локтях может потемнеть из-за повышенной выработки мелатонина
- тело становится более отечным
- царапины и ссадины заживают медленно, даже незначительные
- у женщин может появиться чрезмерное оволосение на теле и лице, а голос грубеет
Также могут появиться изменения в психическом состоянии:
- тревога и депрессия
- раздражительность
- потеря контроля над эмоциями
- экстремальные перепады настроения
- панические атаки
- суицидальные мысли
Иногда могут возникнуть и сексуальные проблемы: сниженное (или, наоборот, повышенное) влечение и возможная эректильная дисфункция.
Осложнения
Кортизол — очень «ответственный» гормон с широкими полномочиями, поэтому последствия его переизбытка могут быть самыми серьезными:
- высокое кровяное давление
- повышенное тромбообразование, риски инсульта и сердечного приступа
- повышение уровня холестерина
- сахарный диабет 2 типа и инсулинорезистентность
- повышенная жажда, более частое мочеиспускание и обильное потоотделение
- повышенная уязвимость перед инфекциями, в том числе и экзотическими
- камни в почках
- потеря мышечной массы и силы
- у детей синдром Кушинга может замедлять рост и провоцировать ожирение
Диагностика
Диагностировать или исключить синдром Кушинга может только врач, особенно учитывая, каким разным и многоликим бывает это состояние. Для установления диагноза и поиска причин используются анализы крови и мочи, а также исследования с помощью МРТ или томографии.
Важно помнить, что уровень кортизола зависит от стресса, времени суток и фазы менструального цикла. Поэтому за три дня до анализа откажитесь от спортивных и нервных нагрузок, за день — от жирной острой пищи и курения, за восемь часов до анализа — от еды. Постарайтесь не полуночничать неделю перед сдачей анализов и следовать традиционным суточным ритмам. Рекомендованная фаза менструального цикла для оценки уровня кортизола — 3−7 день, но врач может уточнить для вас сроки.
Если вы принимаете гормональные препараты, и не можете от них отказаться на две недели перед сдачей крови на анализ, сообщите об этом вашему эндокринологу и в лаборатории, для корректной расшифровки результатов.
Как лечить синдром Кушинга?
Лечение синдрома направлено, прежде всего, на снижение избытка кортизола в организме специальными лекарствами, в основном, кетоконазолом и мамомитом. Реже используется дексаметазон, чтобы снизить активность коры надпочечников. Если это не работает, то иногда врачи рекомендуют удалить один из надпочечников.
Специфика терапии зависит также от причины возникновения этого состояния. При болезни Кушинга может потребоваться хирургическая операция по удалению опухоли гипофиза (нередко это делают через нос). Если причина в других опухолях, то их находят и удаляют.
При слишком большой дозе кортикостероидов врач может снизить объем препаратов или заменить их на нестероидные. Важно не заниматься самолечением и не пытаться самостоятельно снизить дозировку: это может быть опасно для жизни, если уровень кортизола упадет слишком сильно.
И, разумеется, необходима терапия осложнений, вызванных синдромом Кушинга — белкового и углеводного обмена, повышенного артериального давления и т. д.
Синдром Кушинга, как и болезнь Кушинга — это серьезные состояния, и без лечения они могут оказаться смертельными. Однако, при своевременной диагностике, хирургическое лечение или лекарственная терапия помогают восстановить здоровье и вернуться к активной жизни. После постановки диагноза и коррекции состояния важно продолжать наблюдение за своим самочувствием. Берегите себя.
Читайте также: Почему вы не можете сбросить лишний вес? 8 неочевидных причин
Баланс нарушен: 9 признаков того, что с вашим гормональным фоном не все в порядке
Источник
причины, виды и способы лечения патологии
Надпочечники относятся к органам эндокринной системы, которые участвуют в регуляции всех видов обмена веществ. Одним из наиболее серьезных заболеваний, требующих тщательной диагностики и соответствующего лечения, является гиперкортицизм.
Причины и классификация заболевания

Гиперкортицизм (код по МКБ-10 — Е24) — это патология, которая развивается вследствие повышенной продукции глюкокортикостероидов надпочечниками.
Наиболее часто наблюдается избыточная секреция кортизола.
В зависимости от причины, вызвавшей увеличение количества гормонов надпочечников в крови, выделяют экзогенный и эндогенный гиперкортицизм. Рассмотрим отдельно каждую форму патологии.
Эндогенный гиперкортицизм развивается вследствие избыточной продукции гормонов непосредственно надпочечниками. Корковое их вещество вырабатывает минералокортикоиды (альдостерон), глюкокортикоиды (кортизол) и стероидные гормоны (эстрогены и андрогены).
Мозговое вещество отвечает за секрецию катехоламинов, или гормонов стресса — адреналина и норадреналина. Следует отметить, что синдром гиперкортицизма характеризуется чрезмерным количеством преимущественно кортизола. Остальные гормоны повышаются незначительно.
Эндогенныйгиперкортицизм делится на следующие виды:
- Первичный. Данная форма гиперкортицизма возникает на фоне гиперплазии либо гормонально активных опухолей надпочечников (аденом). Данные нарушения нередко генетически детерминированы. При первичном гиперкортицизме уровень адренокортикотропного гормона (АКТГ) в пределах нормы. Второе название этого вида — синдром Иценко-Кушинга.
- Вторичный. Он считается АКТГ-зависимым. При этом наблюдается избыточная продукция АКТГ в передней доле гипофиза, который, в свою очередь, воздействует на надпочечники и стимулирует чрезмерное выделение его гормонов.Вторичныйгиперкортицизм называется болезнь Иценко-Кушинга. Наиболее часто он возникает из-за доброкачественных новообразований гипофиза (аденом).
Экзогенный гиперкортицизм развивается вследствие приема высоких доз глюкокортикоидов при медикаментозном лечении. Это могут быть гормонсодержащие таблетки, мази, аэрозоли. В данном случае выделение гормонов надпочечников не увеличивается, а наоборот, иногда даже уменьшается. Однако из-за лекарственных препаратов количество биологически активных веществ в крови существенно повышается, а работа эндокринных органов частично угнетается.
Отдельно выделяют субклинический гиперкортицизм. Чаще всего его диагностируют случайно при обнаружении односторонней аденомы надпочечника, которая тормозит деятельность здорового. При этом уровень гормонов будет повышен незначительно. Клинические проявления будут умеренно выражены. В основном из симптомов присутствует избыточный вес и повышенное давление.

Гиперкортицизм: клинические проявления
Клиника гиперкортицизма очень характерна. Ее тяжело спутать с проявлениями других заболеваний. Больного с синдромом Кушинга можно узнать только по внешнему виду.

Гиперкортицизму присущи следующие признаки:
- Ожирение. Для людей с гиперкортицизмом характерен абдоминальный, или кушнгоидный тип ожирения. При этом лишние килограммы откладываются преимущественно в верхней половине туловища — на плечевом поясе, груди, животе и лице. Лицо становится лунообразным с синевато-красным цветом щек (это называется «матронизм»). На спине вырастает т. н. «климактерический» горбик. Характерным признаком является истончение кожи и подкожной жировой клетчатки на тыльной стороне кистей. Ноги при этом выглядят достаточно худыми. Соответственно, происходит неравномерное перераспределение отложений. Особенно сильно ожирение выражено у детей. Нередко оно является единственным симптомом заболевания.
- Мышечная атрофия. Ее особенно хорошо видно на ногах и в области пояса верхних конечностей. Человеку будет тяжело присесть, а затем встать на ноги из-за атрофии мышц ягодиц и бедра. При этом характерен внешний вид «скошенных ягодиц». Атрофии подвергаются также мышцы живота, а особенно — белой линии, из-за чего могут появляться грыжи. Из-за ослабления мышечного каркаса возникает «лягушачий живот».
- Истончение кожи. На фоне прогрессирующего набора массы тела кожа начинает растягиваться и истончаться. Она становится сухой, шелушащейся, с просвечивающимися сосудами. На внутренней поверхности бедер, груди, а также плечах появляются красно-фиолетовые стрии (растяжки). При этом на лице проявляется акне.
- Остеопороз. Из-за быстрого непрекращающегося набора веса костная система не выдерживает нагрузку. Особенно страдает позвоночник. Кости начинают истончаться, разрушаться. Часто развиваются болезненные переломы, особенно в грудном и поясничном отделах позвоночника.
- Нарушения в работе сердечнососудистой системы. При синдроме Кушинга наблюдается повышенное давление, аритмии, экстрасистолии. Вследствие прогрессирующего ожирения и ослабления деятельности миокарда развивается сердечная недостаточность, которая может привести к летальному исходу.
- Стероидный диабет.Глюкокортикоиды, вырабатывающиеся в надпочечниках, повышают уровень глюкозы в крови. Из-за этого развивается стероидный диабет, который легко устраняется при помощи диеты и сахароснижающих медикаментов.
- Нарушения в половой системе. Т. к. функции надпочечников включают в себя секрецию половых гормонов, у женщин начинает резко увеличиваться уровень андрогенов, а у мужчин — эстрогенов. Женщины страдают от избыточного оволосения (гирсутизма), а мужчины — от гинекомастии (роста молочных желез), снижения потенции и феминизации фигуры. Также у женщин прекращаются менструации.
Диагностика и лечение
Диагностика гиперкортицизма основана на лабораторных и инструментальных методах исследования. Необходимо провести УЗИ, КТ либо МРТ надпочечников, чтобы исключить возможные новообразования.

После этого всегда назначают функциональные лабораторные тесты, которые используются для диагностики гипо- и гиперкортицизма:
- Определение количества кортизола в суточной порции мочи. Если его уровень повышен в 3 раза и более, то это указывает на гиперкортицизм.
- Дексаметазоновая проба. При нормальном функционировании надпочечников прием дексаметазона уменьшает количество кортизола в 2 раза и более, чего не будет наблюдаться при гиперкортицизме.
Лечение синдрома будет напрямую зависеть от причины. Если гиперкортицизм вызван приемом гормональных препаратов, то их нужно постепенно отменять. В случае, если речь идет о новообразованиях, должен решаться вопрос о возможности хирургического удаления и, при необходимости, последующего лучевого лечения. Также используют препараты, которые угнетают синтез гормонов надпочечников.
Лечение болезни Иценко-Кушинга описано в статье.

Наряду с этим используют медикаменты, которые помогают снять основные симптомы: сахароснижающие, гипотензивные, мочегонные, седативные, антиаритмические, сердечные гликозиды. Кроме того, клинические рекомендации включают строгую диету и адекватные физические нагрузки для снижения веса.
Поделиться ссылкой:
Гиперкортицизм у женщин — что это и как лечить заболевание?
Женский организм чувствительно реагирует на негативные проявления внешней и внутренней среды. У некоторых женщин возникает такой недуг, как гиперкортицизм, что это такое, и как с ним справиться, нам и предстоит узнать. Следует отметить, что данная проблема связана с гормональным фоном, поэтому лечебная терапия будет основана на приеме лекарственных средств. Важно узнать особенности этого патологического процесса, методы борьбы с ним, особенности проявлений и другие важные аспекты.
Какую роль выполняют гормоны надпочечников?
Продолжительное увеличение кровеносной системе гормонов, вырабатываемых надпочечниками, вызывает возникновение синдрома гиперкортицизма. Данный недуг отличается сбоем всех обменных процессов, нарушением функционирования важных систем организма. Факторами, которые привели к гормональному дисбалансу, выступают объемные образования надпочечников, гипофиза и остальных органов, а еще употребление медикаментов, в составе которых присутствуют глюкокортикоиды. Для устранения проявления недуга назначают различные лекарственные средства, а оказать воздействие на новообразование можно лучевым методом либо удаляют её из организма оперативным методом.
Кора надпочечников производит гормоны стероидного типа – минералкоркортиноиды, андрогены и глюкокортикоиды. Их синтез контролируется адренокортикотропным гормоном, например, кортикотропным либо АКТГ. Его выработку регулирует рилинг-гормон, вазопрессин гипоталамуса. Холестерин является общим источником для производства стероидов.
 Симптоматика гиперкортицизма
Симптоматика гиперкортицизмаСамым активным глюкокортикоидом является кортизол. Увеличение его количества приводит к остановке синтеза кортикотропина за счет обратной связи. Благодаря этому поддерживается гормональный баланс. Производство главного гормона минералокортикоидов, то есть альдостерона в меньшей степени зависит от АКТГ. Главным корректирующим механизмом его синтеза является ренин-антиотензиновая система, которая реагирует на изменение объема циркулирующей крови. Диагностика гиперкортицизма основа на сдаче необходимых анализов, после получения результата лечащий врач назначает соответствующее лечение.
В большом количестве производятся в железах половой системы. Глюкокортикоиды оказывают воздействие на все разновидности обменных процессов. Они повышают уровень глюкозы в кровеносной системе, способствуют расщеплению белка и перераспределения жировой ткани. Гормоны обладают противовоспалительным и успокаивающим действием, способствуют задержке натрия в организме и увеличивают давление.
Симптомы
Патологическое увеличение показателя глюкокортикоидов приводит к появлению синдрома гиперкортицизма. Пациенты утверждают о жалобах, связанных с изменением внешности и сбоем функционирования сердечно-сосудистой системы, а также костно-мышечной, репродуктивной, нервной систем. Клинические проявления заболевания также вызваны повышенным содержанием альдостерона и андрогенов, вырабатываемых надпочечников.
В детском возрасте наличие гиперкотицизма приводит к нарушению производства коллагена и уменьшается чувствительность важных органов к воздействию самотропного гормона. Данные изменения являются основной причиной остановки развития тела, а именно роста. После лечения патологического процесса может произойти восстановление структурных элементов костной ткани. Если в организме женщины присутствует большое количество глюкокортикоидов, тогда возникнут следующие клинические проявления:
- Ожирение, при котором происходит отложение жировой массы в районе лица и остальных участков тела.
- Кожные покровы становятся тонкими, а еще возникают растяжки багрового оттенка.
- Проблемы углеводных обменных процессов – сахарный диабет и предиабет.
- Возникновение остеопороза.
- Иммунодефицит вторичного типа с образованием всевозможных инфекционных недугов и грибковых заболеваний.
- Воспаление почек, а также образование твердых конкрементов.
- Нарушения психоэмоционального фона, депрессия, смена настроения.
Симптомы гиперкортицизма у женщин являются достаточно характерными, поэтому диагностировать недуг не очень тяжело. Главное сразу обратиться в медицинское учреждение, чтобы не допустить возникновения серьезных последствий:
- Увеличение артериального давления, при котором даже прием сильнодействующих средств не оказывает должного терапевтического эффекта.
- Слабость в мышцах.
- Нарушение гормонального фона с аритмией, сердечной недостаточностью и миокардиодистрофией.
- Отеки периферического типа.
- Систематическое и обильное мочеиспускание.
- Покалывание и судороги ног.
- Боль в голове.
Половые гормоны обеспечивают реализацию репродуктивных функций в организме. При их нехватке женщина не сможет забеременеть, тем не менее, повышенное количество этих компонентов также имеет ряд побочных эффектов, причем некоторые из них действительно опасные:
- Себорея, акне, угревая сыпь и другие проблемы с кожным покровом.
- Сбой цикла менструации.
- Повышенный волосяной покров на груди, лице, ягодицах и животе у представительниц слабого пола.
- Невозможность забеременеть.
- Уменьшение либидо.
- У мужчин недостаток эстрогенов увеличивает тембр голоса, повышает размер грудных желез, уменьшает рост полос на голове, в частности на лице.
- Нарушение эректильной функции.
Все вышеперечисленные симптомы заставляют пациентку обратиться в медицинское учреждение. Квалифицированному медику достаточно проанализировать жалобы и внешний вид женщины, чтобы определить точный диагноз.
Разновидности и лечение недуга
Главные проявления гиперкортицизма напрямую связаны с чрезмерным количеством кортизола, тогда его уровень определяют в слюне или суточном объеме мочи. Одновременно с этим нужно проверить концентрацию данного компонента в кровеносной системе. Чтобы уточнить разновидность патологического процесса необходимо провести ряд функциональных исследований, например, малый дексаметазоновый тест и большой. В разных лабораториях нормальные показатели этих гормонов отличаются. Проанализировать полученный результат можно только при помощи специалиста.
Для того, чтобы определить сопутствующие нарушения нужно проанализировать анализ мочи и крови, а также обращают внимание на креатинин, электролиты, глюкозу, мочевину и остальные биохимические значения. Отличной информативностью обладают такие инструментальные методы, как КТ, денситометрия, МРТ, УЗИ и ЭКГ. Чрезмерное производство гормонов надпочечников приводит к различным патологическим проявлениям, что заставляет применять сильнодействующие медикаменты. Однако перед тем, как переходить к лечению гиперкортицизма, необходимо определить его разновидность, поскольку каждая форма заболевания имеет характерные отличия и особенности, что проявляется не только в симптомах, но еще и в дальнейшем лечении болезни.
 Для того, чтобы определить сопутствующие нарушения нужно проанализировать анализ мочи и крови
Для того, чтобы определить сопутствующие нарушения нужно проанализировать анализ мочи и кровиПовышенный синтез глюкокортикоидов возникает под действием кортиколиберина и кортикотропина, либо вообще независимо от них. По этой причине выделяют АКТГ-независимые и зависимые от АКТГ разновидности заболевания. К последней относятся:
- функциональный гиперкортицизм;
- периферическая форма;
- экзогенный гиперкортицизм.
К первой группе разновидностей относятся такие формы:
- Гиперкортицизм центрального типа. Причиной данной патологии является новообразование гипофиза. В этом случае опухоль имеет небольшой размер, к примеру, до 1 сантиметра речь идет об микроаденомах, если они превышают данный показатель, тогда в организме присутствует макроаденома. Такие образования синтезируют чрезмерное количество АКТГ, он стимулирует выработку глюкокортикоидов, а между гормонами нарушается взаимосвязь. Лечение осуществляют протонным пучком, в некоторых случаях применяют комбинированные способы.
- АКТГ-эктопический синдром. Злокачественное образование разных органов синтезирует чрезмерное количество компонентов, которые по своему строению напоминают кортиколиберин либо кортикотропин. Они вступают в контакт с рецепторами АКТГ и увеличивают интенсивность производства гормонов. После определения места расположения опухоли её успешно оперируют.
Лечение гиперкортицизма у женщин осуществляется в большинстве случаев радикальными методами, то есть хирургическим удалением новообразования. Тем не менее, современные аптечные медикаменты также показывают хорошую результативность, поэтому их активно применяют в качестве лечебной терапии, увеличить эффективность можно за счет народных методов. Субклинический гиперкортицизм требует от лечащего врача высокой квалификации, поскольку недуг нужно правильно диагностировать и отличить от других форм заболевания. Для этого применяются различные диагностические мероприятия, задача которых – правильно и точно определить причину патологического процесса, степень поражения организма и дальнейшие методы лечения.
