Лечение токсокароза, лечение, цена в Москве
|
Токсокароз – заражение организма человека личинками разновидности Toxocara. Без правильного лечения болезнь опасна осложнениями, рецидивами и грозит жизни человека. Мы можем помочь избавиться от проблемы, оказав пациенту полное комплексное лечение по приятным ценам. |
Распространенные симптомы
- обостряются симптоматические проявления: чем интенсивнее происходит заражение, чем активнее личинки распределяются по тканям и органам, тем выше будет степень симптомов;
- пациент ощущает озноб;
- увеличивается температура;
- иногда проявляется аллергическая крапивница;
- воспаляются верхние дыхательные пути;
- начинается насморк;
- печень и селезенка увеличиваются в размерах;
- ощущаются боли в области живота;
- наступает паралич;
- поражаются мышцы;
- могут наблюдаться судороги, диарея, рвота и тошнота.

Как паразиты попадают в организм?
Заболевание отличается распространенностью возбудителей. Выделяют основные причины заражения:
- употребление в еду немытых фруктов, овощей;
- контакт с фекалиями животных;
- несоблюдение гигиены;
- нерегулярная дегельминтизация питомцев.
Что необходимо, чтобы начать лечение?
Если появляются типичные симптомы заболевания, стоит узнать, как проходит осмотр у врача и обратиться к нам. Врач начинает диагностику: осмотр, анализ крови, кала, рентген. При позитивных результатах пациент может заключить договор и начать лечение.
Как проходят процедуры?
Лечение болезни совершенствуется, и мы предоставляем современные методики, которые предлагает иммунология на сегодня. Паразитов выводим на протяжении 2-4 недель специальными средствами. Поддерживаем состояние пациента, избегаем побочных эффектов и дальнейших проблем с пищеварением.
К нам можно записаться по телефону или заполнить форму обратной связи и назначить консультацию в удобное время.
Телефон отделения: +7 (495) 695-56-95
Лечение токсокароза — врачи, лечащие заболевание
Гастроэнтерологи Москвы — последние отзывы

На модерации, 07 июня 2021
Кирилл Александрович хороший доктор. Он поставил диагноз и выписал мне заключение.
Галина, 06 июня 2021
Врач — вежливый и добрый человек. Знает свое дело! Всё хорошо объяснила, разъяснила. Назначила то, что нужно и рассказала всё по лечению. Вопросов нет. В следующий раз приду обязательно к ней!
Знает свое дело! Всё хорошо объяснила, разъяснила. Назначила то, что нужно и рассказала всё по лечению. Вопросов нет. В следующий раз приду обязательно к ней!
Яна, 04 июня 2021
Вызывала невестке врача на дом, так как очень тяжелый диагноз. Хотелось бы, чтобы врач всё же приехал пораньше, но нас предупреждали, что могут быть пробки и т.п. Претензий нет. У нас цирроз, а специалист по гепатиту, однако он сделал все рекомендации и написал нужные лекарства. Врач высококвалифицированный. Хорошо разбирается в этом деле. Всё доступно объяснил.
Галина, 03 июня 2021
Джонбек, 03 июня 2021
Доктор внимательный.
Наталья, 24 мая 2021
Очень душевный врач, которому можно всё доверить и рассказать. Она меня проконсультировала и ранее, когда я обращалась с проблемой доктор мне помогла.
Ольга, 27 апреля 2021
Прекрасный доктор.
На модерации, 07 июня 2021
Врач адекватный, аккуратный, доброжелательный и грамотный. Он слышит проблему пациента и готов помочь. Доктор все нам объяснил, рассказал, развеял сомнения, ответил на вопросы и дал чёткое понимание картины, которое на данный момент есть со здоровьем.
На модерации, 07 июня 2021
Доктор приветливый, внимательный и чуткий.
На модерации, 07 июня 2021
Показать 10 отзывов из 12414Toxocara, IgG, титр
Токсокароз – паразитарное заболевание, вызываемое нематодой семейства Anisakidae рода Тохосаra canis – гельминтом, который паразитирует на собаках и других представителях семейства псовых. Заражение человека происходит при проглатывании яиц токсокар, находящихся в почве, на шерсти животных, в продуктах питания. Заболевание проявляется двумя основными формами: висцеральной – синдромом «блуждающей личинки» – и глазной.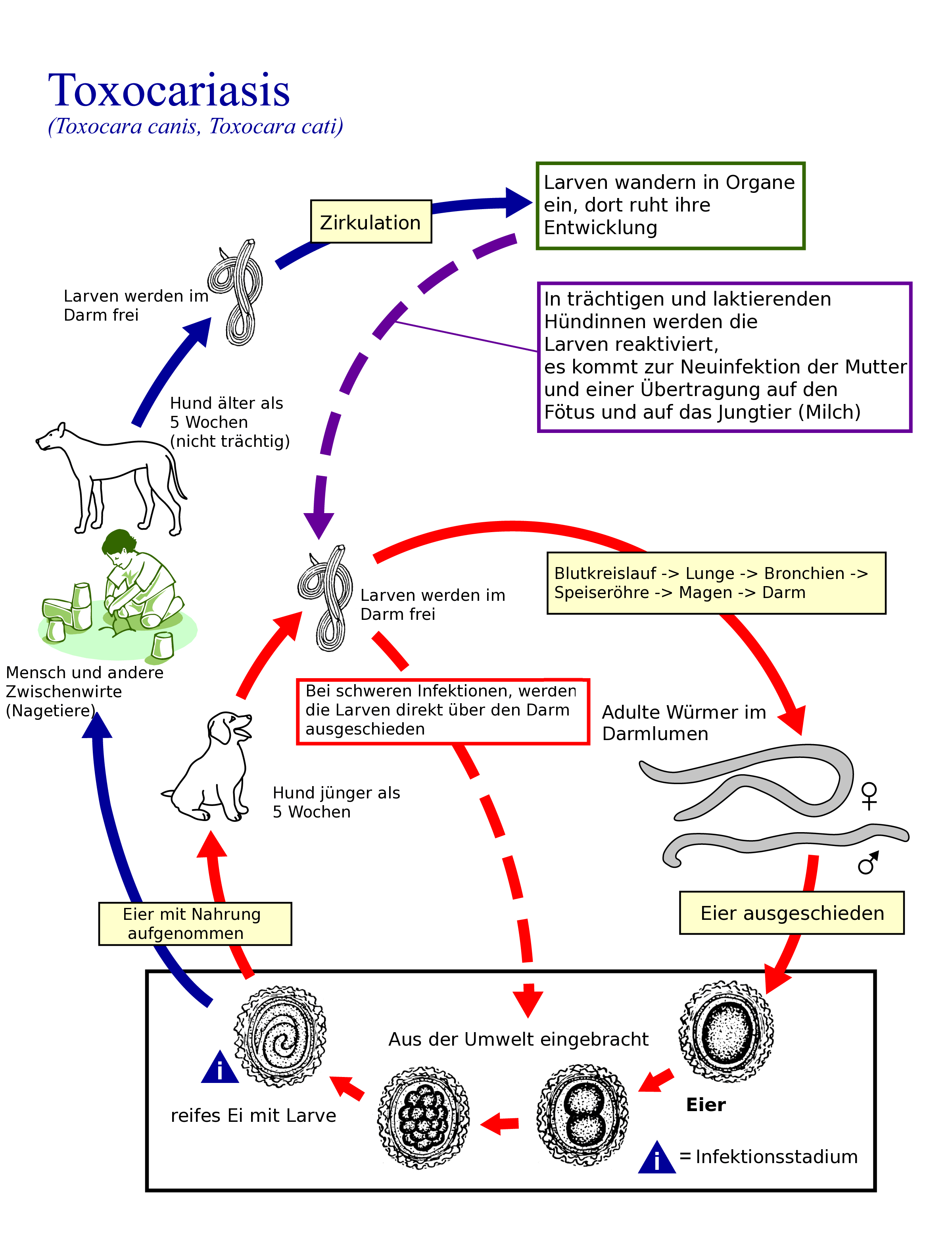 Токсокароз характеризуется длительным течением и частыми рецидивами.
Токсокароз характеризуется длительным течением и частыми рецидивами.
Определение антител класса IgG к возбудителю токсокароза – это основной серологический метод, позволяющий диагностировать инвазию токсокарами.
Синонимы русские
Антитела класса IgG к Toxocara, иммуноглобулины класса G к антигенам токсокар.
Синонимы английские
Anti-Toxocara IgG, Toxocara antibodies, IgG.
Метод исследования
Иммуноферментный анализ (ИФА).
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Исследование проводится для выявления инфицирования нематодой семейства Anisakidae рода Тохосаra canis – это круглые черви, которые вызывают токсокароз.
Токсокароз – распространенное во всем мире паразитарное заболевание, поражающее различные органы, включая глаза. Основным хозяином (источником инвазии) являются домашние и дикие животные семейства псовых (собаки, волки, лисы и т. д.), инфицированные T. canis. Инфицированность этих животных у нас в стране составляет до 70 %. В их организме происходит окончательное созревание паразита до взрослых особей, которые локализуются в тонком кишечнике и продуцируют яйца, выделяемые в окружающую среду с калом. При попадании в почву яйца гельминтов длительное время сохраняют жизнеспособность и инвазивность. Человек заражается при проглатывании яиц T. Canis, содержащихся в почве, на шерсти животных, а также употребляя в пищу недостаточно обработанные продукты питания. Попадая внутрь, личинки паразита начинают выходить из яиц в проксимальном отделе тонкой кишки. Затем они мигрируют через слизистую оболочку кишечника в кровеносную систему и через воротную вену попадают в печень, где частично оседают. Остальные личинки, прошедшие через печень, попадают через малый круг кровообращения в легкие, где тоже частично оседают.
Основным хозяином (источником инвазии) являются домашние и дикие животные семейства псовых (собаки, волки, лисы и т. д.), инфицированные T. canis. Инфицированность этих животных у нас в стране составляет до 70 %. В их организме происходит окончательное созревание паразита до взрослых особей, которые локализуются в тонком кишечнике и продуцируют яйца, выделяемые в окружающую среду с калом. При попадании в почву яйца гельминтов длительное время сохраняют жизнеспособность и инвазивность. Человек заражается при проглатывании яиц T. Canis, содержащихся в почве, на шерсти животных, а также употребляя в пищу недостаточно обработанные продукты питания. Попадая внутрь, личинки паразита начинают выходить из яиц в проксимальном отделе тонкой кишки. Затем они мигрируют через слизистую оболочку кишечника в кровеносную систему и через воротную вену попадают в печень, где частично оседают. Остальные личинки, прошедшие через печень, попадают через малый круг кровообращения в легкие, где тоже частично оседают.
Личинки токсокар, прошедшие через легкие, через большой круг кровообращения распространяются по всему организму, оседая в различных органах. Попавшие в ткани органов личинки гельминта не претерпевают дальнейшего нормального развития и в конечном счете там и погибают, инкапсулируясь и образуя гранулемы.
Мигрируя по организму, личинки оказывают на него различное воздействие: травмируют кровеносные сосуды, вызывая кровотечения и некроз. Важное значение имеют экскреторно-секреторные антигены личинок, оказывающие сенсибилизирующее действие на организм.
Тяжесть клинических проявлений заболевания связана не только с численностью паразитов, но и с уровнем аллергической чувствительности организма. При токсокарозе чаще всего поражаются печень, легкие, центральная нервная система, в том числе глаза, почки и скелетные мышцы.
Токсокароз может протекать в различных формах, часто бессимптомно. Клинически различают 2 формы: висцеральный синдром – «синдром блуждающей личинки» – и глазной токсокароз.
Основные симптомы инфицирования T. canis: лихорадка, лимфоаденопатия, общее недомогание, кожная сыпь, желудочно-кишечные расстройства, при массивных инвазиях – боли в правом подреберье, увеличение печени и селезенки, признаки поражения легких. Для глазной формы токсокароза характерно поражение одного глаза в виде снижения остроты зрения, гранулемы сетчатки, увеита, эндофтальмита, неврита зрительного нерва, кератита или наличия мигрирующих личинок в стекловидном теле. Хотя основные проявления заболевания зависят от пораженных органов, наиболее характерным лабораторным показателем является эозинофилия периферической крови.
У пациентов со сниженным иммунитетом при массивной инвазии токсокарами возможны тяжелые осложнения.
Диагноз «токсокароз» ставят на основании клинической картины, эозинофилии, данных эпидемиологического анамнеза и результатов серологического исследования.
Для чего используется исследование?
Исследование проводится с целью выявления инфицирования нематодой семейства Anisakidae, рода Тохосаra canis, которая вызывает токсокароз. Рекомендуется обследование людей, относящихся к группам риска: ветеринаров, животноводов, кинологов, детей с признаками лихорадки неясного происхождения и с эозинофилией крови.
Существует несколько методов, которые могут быть использованы для проверки на токсокароз. Один из них позволяет определять антитела возбудителя в крови.
Когда происходит контакт человека с Toxocara canis, его иммунная система реагирует, вырабатывая антитела IgM и IgG.
Иммуноглобулины класса G к Toxocara в определяемых количествах появляются в крови через 6-8 недель с момента инфицирования. Концентрация их нарастает и через 2-3 месяца достигает максимума, сохраняясь на определенном уровне в течение продолжительного времени. Степень повышения уровня антител в крови тесно связана с тяжестью заболевания.
Ложноположительные результаты анализа возможны у лиц с системными лимфопролиферативными заболеваниями и иммунодефицитом. Ложноотрицательные и сомнительные результаты анализа могут наблюдаться у лиц с поражением глаз в результате слабого антигенного воздействия.
Тест на антитела класса IgG к Toxocara является основным методом выявления токсокароза у человека и применяется для подтверждения диагноза.
В каких случаях назначают анализ?
- Если имеются признаки поражения печени, легких и/или лихорадка неясного происхождения на фоне эозинофилии в крови, указывающие на возможную инвазию нематодами.
- При внезапном снижении зрения, затрагивающего один глаз.
- По эпидемиологическим показаниям (контакт с собаками, землей – особенно у детей).
- Если известно, что человек употреблял недостаточно обработанные продукты, которые могли быть заражены T. Canis.
- Когда пациент входит в группу повышенного риска (животноводы, кинологи, фермеры, ветеринары).
Что означают результаты?
Референсные значения
|
КП |
Титр |
Результат |
|
КП |
— |
отрицательный |
|
|
1:100 |
слабоположительный |
|
|
1:200 |
|
|
|
1:400 |
|
|
|
1:800 |
положительный |
|
|
1:1600 |
|
|
|
1:3200 |
|
|
|
1:6400 |
|
|
|
1:12800 |
Для анализов крови на антитела класса IgG к возбудителю токсокароза, которые организм вырабатывает для борьбы с инфекцией, положительный результат указывает на то, что пациент инфицирован Toxocara canis. Вместе с тем отрицательный результат не всегда означает, что у пациента нет токсокароза.
Положительный результат теста на антитела IgG к Toxocara canis у ранее серонегативного пациента, а также значительный прирост титров в парных сыворотках, взятых с интервалом, подтверждает первичную инфекцию.
Отрицательный результат данного теста может свидетельствовать об отсутствии инфицирования или слишком раннем его сроке, когда не выработался иммунный ответ.
Повторные исследования уровня антител в крови больного позволяют оценивать проводимое лечение — о его эффективности свидетельствует снижение уровня антител.
Причины отрицательного результата:
- отсутствие инфицирования,
- глазной токсокароз (ввиду слабого иммунного ответа),
- слишком раннее инфицирование, когда не выработался иммунный ответ.
Причины положительного результата:
- текущий или перенесенный в прошлом токсокароз,
- скрытый токсокароз.
Важные замечания
- Диагностика токсокароза сложна. Это обусловлено тем, что в организме человека токсокары не достигают половозрелого состояния, поэтому нельзя выявить взрослых особей или их яйца в образцах кала или дуоденальном содержимом, как при других гельминтозах.
- Обязательно учитывают эпидемиологический анамнез: контакт с собаками, землей, употребление в пищу недостаточно обработанных продуктов.
- Заболевание не передается от человека к человеку.
- Основой профилактики токсокароза является соблюдение правил личной гигиены: мытье рук после контакта с почвой или животными. Нельзя употреблять в пищу плохо обработанные продукты питания, которые могут содержать яйца Toxocara canis.
- Владельцам собак необходимо своевременно обследовать своих питомцев и, если необходимо, проводить их дегельминтизацию.
Также рекомендуется
- Скрининговое обследование на гельминтозы (Opistorchis IgG, Toxocara IgG, Trichinella IgG, Echinococcus IgG)
Кто назначает исследование?
Инфекционист, терапевт, педиатр, гастроэнтеролог, аллерголог, офтальмолог.
Токсокароз кошек — симптомы и лечение
Возбудитель токсокароза
Токсокароз — это весьма распространенное заболевание у кошек. Заразную болезнь вызывает кошачья аскарида — токсокара.
Некоторые хозяева считают, что маленькие паразиты совсем не опасны и долгое время не обращают внимания на симптомы заражения. И совершенно, зря. Ведь кошачья токсокара может проникнуть и в организм человека. Гельминты долго живут и быстро плодятся. Далее, они вызывают болезни, которые долго не проходят, например, простуды, постоянные головные боли, усталость, диарею и т. д. В конечном итоге все может закончиться инфарктом. В этом будут повинны крохотные паразиты и нежелание лечиться вовремя.
Важная информация!
Заболеванию токсокарозом подвержены кошки любых возрастов и пород. Особенно восприимчивы к болезни новорожденные питомцы. Маленькому котенку токсокароз передается вместе с молоком матери. Известны случаи, когда инфицирование привело к летальному исходу животного.
В этой статье расскажем подробнее о возбудителе токсокароза, симптомах, лечении и мерах профилактики.
Развитие паразита
Кошачья токсокара в зрелом возрасте имеет на головном отделе боковые широкие крылья. Длина тела самцов достигает до 7-и сантиметров, а самок до 10-и сантиметров. Кроме размеров самцы отличаются наличием 26-и сосочков на конце хвоста. Цвета паразита варьируются от светло — желтых до кремовых оттенков. Шаровидные яйца гельминта имеют толстые шероховатые стенки. Рот представляет собой 3 губы. Гельминты питаются содержимым кишечника хозяина.
Основная часть жизни паразита проходит в организме кота. Жизненный цикл токсокары выглядит следующим образом:
- Животное проглатывает яйца паразита;
- Гельминт поселяется в пищеварительном тракте;
- Из яиц вылупляются личинки;
- Через кровь они разносятся по всему организму;
- Начинается повреждение внутренних органов.
Выходя через легкие, личинки токсокары снова попадают в кишечник хозяина и окончательно там оседают, здесь и происходит дозревание паразитов. Самка токсокары способна откладывать яйца в огромных количествах. Один грамм экскрементов может содержать до 100 тысяч яиц гельминтов
Как уже говорилось ранее, токсокароз опасен последствиями. Ослабленный организм животного легко поддается атакам различных болезней.
Токсокара воздействует на организм следующими негативными методами:
- Механическими
У взрослых особей есть зубы, острые шипы, крючья. Этими приспособлениями они травмируют слизистые тканей. Также миграция личинок нарушает целостность структур органов. Тем самым, травмирование тканей приводит к воспалительным процессам в организме.
Когда паразиты погибают, начинается разложение их тел. Отрава разносится по всему организму.
- Провокационными
Последствия от пребывания токсокары в организме: хронические заболевания, ослабление иммунной системы, возникновение новых патологий.
Таким образом, ослабленный иммунитет не способен бороться с вторжением инфекций и самочувствие больного со временем ухудшается. Токсокароз способен вызвать у кошек тяжелые заболевания почек, сердца, легких. Если болезнь своевременно не лечить, то все может закончиться гибелью животного.
Симптомы заражения токсокарозом
Яйца токсокары представляют опасность после двух линек. Процесс созревания занимает несколько недель. Но после того как созревание вступило в решающую фазу, личинки внутри яиц сохраняют жизнеспособность до нескольких лет даже находясь в почве.
Заражение животного происходит очень быстро несколькими путями:
- Когда экскременты зараженного животного высыхают, то зародыши гельминтов разносятся ветром. Если они ненароком попали на шерсть животного, то кошка заболевает, просто вылизывая свою шерсть.
- Нематода паразитирует на многих: свиньях, курах, мышах, червях, жуках и т. д. Поэтому, поедание сырого мяса зараженного животного не пройдет без последствий для пушистого питомца.
- Контакт с фекалиями зараженных животных
Хозяин питомца может не сразу заметить опасность заражения. Дело в том, что токсокароз не обладает ярко выраженными симптомами болезни.
Тем не менее, признаки токсокарозного заражения выглядят следующим образом:
- Агрессивность и зуд;
- Раздутие живота и расстройство кишечника;
- Ухудшение зрения;
- Шерсть теряет былой блеск, выпадает, всклокочена;
- Лимфоузлы увеличиваются;
- Происходит нарушение аппетита и снижение веса;
- Возможный кашель.
Точный уровень заболевания покажут анализы. Также результаты анализов покажут снижение гемоглобина.
Опасность токсокароза для человека
Обратите внимание!
Чаще всего человек заражается от собачьей токсокары, а не от кошачьей. Личинки первой больше по размерам и намного опаснее.
Однако опасность заразиться паразитами от кошек не исключена. Так в 1964 году зафиксирован смертельный случай заражения маленькой пятилетней девочки от кошки. Личинки токсокары существенно повредили мозг ребенка.
Как определить, что Вы стали жертвой паразитов?
Есть несколько симптомов на которые необходимо обратить повышенное внимание:
- Неприятный запах изо рта;
- Быстрая утомляемость;
- Перепады настроения;
- Частые простуды;
- Развиваются серьезные заболевания, вплоть до онкологических.
Соблюдение мер профилактики, и лечение питомца предупредят коварную болезнь.
Лечение кошек в домашних условиях
К счастью токсокароз успешно лечится на любой стадии заболевания. Основу лечения составляют противоглистные препараты. Обычно ветеринар составляет индивидуальную схему лечения. Наиболее распространенными и эффективными являются средства:
- Таблетки Каниквантел Плюс
У этого препарата практически нет побочных действий. Лекарство имеет вкус и запах мяса. Поэтому, кошки сами спешат скорей его попробовать. Для достижения успешного результата достаточно однократного приема.
Это мощное средство необходимо принять лишь один раз. Лекарство подходит и для котят, которым уже исполнилось 3 недели. Выпускается в виде суспензии или таблеток
- Препарат Мильбемакс
Лекарство с мясным ароматом подходит для котят и молодых особей. Нужное количество рассчитывается по инструкции. Она прилагается к препарату. Каждое из этих средств прекрасно работает и на стадии профилактических мер.
Меры профилактики
Для предупреждения токсокароза следует ежегодно и даже чаще проводить антигельминтную процедуру животного. Специалисты рекомендуют сроки, раз в три месяца. Не лишним будет и периодическая дезинфекция места обитания усатого питомца.
Для владельца подходят следующие рекомендации:
- Тщательное мытье рук с мылом;
- Соблюдение личной гигиены;
- Тщательная обработка мясных и рыбных блюд;
- Мытье горячей водой сырых овощей и фруктов.
Вовремя принятые меры профилактики позволят уберечь животное и себя самого от коварного заболевания и связанных с этим осложнений!
Токсокароз. Симптомы, диагностика, лечение. — Доказательная медицина для всех
Жизненный цикл и хозяева токсокар. Основным хозяином паразитов являются собаки и кошки. Основным источником заражения хозяев являются яйца во внешней среде. При проглатывании яиц из них выходят личинки, через кишечную стенку попадают в кровоток и мигрируют в легкие, где проходят несколько этапов личиночного развития, а затем, через пищевод вновь попадают в желудочно-кишечный тракт, где развиваются во взрослых особей. Взрослые черви откладывают яйца в кишечнике основных хозяев, откуда они с фекалиями попадают в окружающую среду. Часть личинок из кровеносного русла выходят в тканях внутренних органов и превращаются в «спящих» личинок. Это резерв как для пополнения кишечной популяции паразитов, так и для передачи потомству.В первом случае спящие личинки становятся активны, вновь проникают в кровеносное русло и проходят легочный, затем кишечный циклы развития.
Во втором случае личинки активизируются во время беременности собаки, проникают через плацентарный барьер, и превращаются в «спящих» личинок в тканях развивающихся плодов. После рождения щенков эти личинки также активизируются, и через кровь, затем легкие, попадают в кишечник щенков.
По международным ветеринарным стандартам все щенки считаются зараженными токсокарозом и должны проходить дегельминтизацию, начиная с 3-хнедельного возраста. Собачий вид, Toxocara canis, также поражает щенков через молоко при лактации суки. Кошачий вид этой способности лишен.
Яйца, попавшие во внешнюю среду, попадают в организм резервуарных хозяев (например, кроликов, свиней, в том числе и человека). В организме таких хозяев так же происходит миграция, токсокары поражают легкие, печень, центральную нервную систему. Цикл завершается, когда основной хозяин поедает зараженное мясо животного. Как видите, токсокары используют практически все возможные пути заражения своих хозяев.
Эпидемиология токсокароза. Токсокароз выявляется практически повсеместно, наибольшая встречаемость в областях с теплым и умеренным климатом. Зараженность как собак, так и людей, зависят от принятых в разных странах стандартов социальной гигиены, то есть привычки владельцев убирать фекалии своих питомцев. Самая низкая зараженность в Германии, в России практически все собаки заражены токсокарозом. Заболеваемость людей встречается достаточно часто, преимущественно заболевают дети. Заражение происходит в основном собачьим видом, заражение кошачьей токсокарой описано в единичных случаях. У людей токсокары никогда не образуют кишечных форм , всегда остаются тканевыми личинками. Пути передачи токсокарозаК человеку токсокары попадают через загрязненные руки, продукты питания, воду, изредка — через недостаточно обработанное термически зараженное мясо.
Симптомы токсокароза Как сказано выше, при попадании личинок токсокар в организм человека, они внедряются в стенку кишечника, попадают в кровеносное русло и мигрируют в различные органы и системы. Клиника и симптомы зависят от пораженных органов, причем периодически личинки мигрируют по организму, и симптомы меняются. Характерно появление проявлений аллергического характера, как ответ организма на инвазию. При поражении печени, в ней формируются узлы (гранулемы), что влечет за собой увеличение печени, и, возможно, нарушение ее функции. При миграции токсокар в легкие, заболевание проявляется в виде длительного кашля, преимущественно сухого и непродуктивного (т.е. без выделения мокроты), т.н. астматического компонента (бронхоспазма). Одним из самых серьезных последствий токсокароза является развитие астмы, которая может хронизироваться, то есть не исчезает после излечения токсокароза.Проявление поражений центральной нервной системы зависит от локализации токсокар. Это могут быть энцефалит, миелит, цереброваскулит… Поражение периферических нервов проявляется как радикулит, нарушения в работе опорно-двигательного аппарата, поражение черепных нервов.
Поражение глаз токсокарами приводит к появлению воспалительных заболеваний, развитию паразитарной гранулемы сетчатки, поражение зрительного нерва может привести к полной слепоте. Поражение мышц характеризуется появлением в них узлов, болями, нарушением функций. Несмотря на возможные серьезные поражения органов и систем, все же чаще токсокароз проявляется легкой симптоматикой. Сложность диагностики этого заболевания — в разнообразии симптомов и их изменчивости, часть больные ходят от врача одной специальности к другим, прежде, чем кто-то заподозрит токсокароз. Диагностика токсокарозаДиагноз ставится на основании симптомов и эпидемиологических данных. В лабораторных тестах встречаются следующие изменения:
- Лейкоцитоз и эозинофилия – увеличение количества лейкоцитов и эозинофилов в периферической крови. Эозинофилия может достигать высоких значений (20 — 40%), каких не бывает при банальных гельминтозах и служит важным диагностическим признаком. При поражении печени могут быть увеличены печеночные трансаминазы (АСТ и АЛТ), щелочная фосфатаза.
- Повышение иммуноглобулинов класса Е и G. Иммуноферментный анализ (ИФА), подтверждающий появление специфического к токсокаре иммуноглобулина G. Следует заметить, что чувствительность данного показателя низка, т.к. он демонстрирует не наличие заболевания, а то, что организм встречался с токсокарой. Для диагностики важно сочетание повышенного титра IgG к токсокаре и наличие эозинофилии крови. Поэтому бессмысленно делать анализ качественным методом (положительно — отрицательно), нужен только количественный анализ. Крайне редко повышенный уровень антител сочетается с нормальной эозинофилией. Обычно это происходит при незначительном заражении.
- Следует знать, что анализ кала в диагностике токсокароза не применяется.
- Лучевая диагностика: При поражении внутренних органов выявляются токсокарозные узлы в печени, легких, центральной нервной системе. Не редко такие образования путают с метастазами. Могут быть использованы как ультразвуковые, так и рентгеновские (рентгенография, компьютерная томография) и магнитно-резонансные методы исследования.
Легкие и умеренные формы токсокароза не требуют специфической терапии. При тяжелой форме заболевания требуется специфическая терапия. Для лечения токсокароза эффективны:
- Альбендазол
- Мебендазол. Менее эффективен, чем первый препарат и в настоящее время при токсокарозе не назначается.
При выраженной симптоматике, характерной для поражения центральной нервной системы, оправдано применение преднизолона. Во время лечения, вследствие поступления в организм антигенов токсокары, могут усиливаться симптомы, повышаться эозинофилия и уровень IgG.
Контроль излеченности Нормализация уровня IgG происходит в среднем через 6 мес. после эффективного лечения. Если симптомы сохраняются, а уровень IgG остается повышенным, возможно назначение повторного курса лечения. При эффективном лечении уровень эозинофилов должен снизиться до нормального уровня, но это может занять длительное время. При эффективном лечении эозинофилия снижается быстрее, чем уровень антител. Ранее, чем через 6 месяцев после лечения, повторять анализы на токсокароз бессмысленно. Профилактика токсокароза Основой профилактики является соблюдение правил личной гигиены. Следует исключить игры детей в песочницах, к которым имеют доступ собаки и кошки. Не следует использовать в пищу продукты и воду не прошедшие соответствующей термической обработки. Заражение от собственной собаки маловероятно. Проведенные исследования показали, что вероятность заражения токсокарозом равна для владельцев собак и невладельцев. Средством коллективной профилактики является уборка фекалий хозяевами собак на улице после ее дефекации.Токсокароз — Ветеринарные клиники Доктор Вет
Токсокароз (Toxocaros canum) — или аскариды плотоядных одно из наиболее часто встречающихся заболеваний собак и кошек, вызываемое круглыми гельминтами. Паразитируют гельминты в тонком отделе кишечника, иногда встречаются желчных ходах печени и поджелудочной железе. Особенные проблемы он вызывает при выращивании щенков и котят.
Возбудитель — Toxocara canis — серо-желтого цвета, длина самки 10—18 см (самцы меньше). Хвостовой коней самца изогнут.
Биология развития.
Яйца, выделенные наружу больными животными, достигают инвазионности при благоприятных условиях за 8—15 суток. Личинка, освободившаяся из яйца, попавшего в кишечник животного, внедряется в подслизистую оболочку, где попадает в кровеносные сосуды и с током крови переносится в печень, затем в сердце и легкие. Из бронхов со слизью попадает в ротовую полость и заглатывается животным. В тонком отделе кишечника гельминт достигает половой зрелости за 20—21 сутки (завершается аскаридный тип развития). Однако некоторые личинки в период миграции в организме с кровью попадают в ткани печени, сердца, почек и мышцы, где инкапсулируются и сохраняют жизнеспособность больше года. В дальнейшем при наступлении беременности v сук часть этих личинок активизируется и мигрирует через плаценту и кровь, вызывая внутриутробное заражение щенков. Такой процесс может повторяться неоднократно. После рождения щенят личинки мигрируют из легких и печени в кишечник, достигают половой зрелости через 20—21 сутки.
После родов щенки дальше заражаются галактогенно. Соматические личинки, циркулирующие в большом круге кровообращения, попадают в молочные железы и выделяются с материнским молоком. Выделение начинается через несколько дней после родов и достигает пика на второй неделе лактации. На этом уровне оно держится примерно неделю, а потом уменьшается. Это означает, что материнским молоком щенки заражаются обычно на 2 – 3 неделе жизни. После галактогенной инвазии, как правило, происходит гепатопульмональная миграция. Препатентный период 27 – 35 дней.
Заражение.
Собаки заражаются, поедая мясо лис, песцов, а также мышей и крыс, в теле которых сохраняются личинки длительное время, а также некоторых беспозвоночных, например, дождевых червей и тараканов. Продолжительность жизни гельминтов — 5 месяцев и более.
Заболевание распространено повсеместно, особенно в больших городах. Болеют в основном щенята и молодые животные, чаще всего в возрасте до 6 месяцев. Повсеместное распространение и высокая интенсивность инвазии Т. canis зависят от 3 факторов. Во-первых, самки паразитов чрезвычайно плодовиты. Один гельминт способен производить около 700 яиц на 1 г фекалий каждый день, и количество яиц, превышающее 15000 яиц/г. Во-вторых, яйца высоко резистентны к экстремальным температурам и могут выживать на земле годами. В-третьих, постоянным резервуаром инвазии являются соматические ткани суки, и личинки в них не восприимчивы к большинству антигельминтных средств.
В городских условиях особо неблагополучны детские игровые площадки и выгульные площадки собак, где яйца в большом количестве сохраняются месяцами.
Симптомы.
У более взрослых животных выраженных клинических признаков обнаружить не удается. У щенят регистрируют понос, рвоту, извращение аппетита, метеоризм, нервные явления. Щенята визжат, лают без причин, кусаются, худеют. Нередко у них при рвоте клубками выбрасываются токсокары. Больные щенята отстают в росте и развитии. Глубоко нарушается показатели крови: уменьшается количество эритроцитов, гемоглобина, увеличиваются лейкоциты и эозинофилы.
Аскариды вырабатывают токсин аскаридин, который вызывает нервные расстройства и быстро высвобождается из тел мёртвых гельминтов. Разрушение большого количества аскарид в кишечнике может, поэтому вызвать сильные судороги, а может даже привести к смерти поражённого животного. Съедание кала щенков сукой считается одним из этиологических факторов послеродовой эклампсии, вызванной аскаридином.
Диагноз.
Микроскопическое исследование кала для обнаружения яиц аскарид. Иногда происходит самопроизвольный выход гельминтов в кале или с рвотой.
В клиниках «Доктор Вет» диагноз ставится на основании клинических признаков и копрограммы.
Лечение и профилактика.
Для дегельминтизации в клиниках и аптеках «Доктор Вет» вам предложат следующие современные препараты:
Внутренние препараты в виде таблеток, суспензий и паст:
• Дронтал (пирантел-эмбонат + празиквантел) – для кошек
• Дронтал + (Празиквантел + Пирантел-эмбонат + Фебантела) – для собак
• Дирофен – паста (празиквантел + пирантела памоат)- для собак и кошек
• Азинокс (празиквантел) – для собак и кошек
• Квантум (мебендазол + празиквантел) – для собак
• Диронет (пирантела памоат + празиквантел + ивермектин) – для собак и кошек
• Празицид – суспензия (празиквантел + пирантела памоат) – для собак и кошек
• Празитаб (празиквантел + пирантел памоат) – для кошек
• Празитаб + (празиквантел +пирантел памоат + фебантел) – для собак
• Альбазен (альбендазол) – для всех с\х животных и птиц
Наружные препараты (на холку):
- Профендер ( эмодепсид + празиквантел) – для кошек
- Адвокат (имидаклоприд + моксидектин) – для собак
Даже если вы не наблюдаете у питомца явных признаков инвазии, рекомендуется производить дегельминтизацию 1 р.\ 3 мес., чтобы предотвратить возможное развитие паразитов, а также обезопасить свою семью от заражения. Дегельминтизацию следует производить и в тех случаях, если животное совсем не гуляет на улице, поскольку яйца паразита может принести любой человек на подошве обуви.
Читайте также
Диагностика и лечение токсокароза | Медицинский центр Аванта-Мед
Токсокароз — паразитарное заболевание, которое при отсутствии адекватного и своевременного лечения может привести к масштабному поражению внутренних органов и инвалидности.
Возбудителем является токсокара — паразит длиной до 18 сантиметров. Зрелые особи обитают в желудке и кишечнике псовых. За сутки взрослый червь способен отложить более 200 тысяч яиц. С фекалиями они попадают в почву, причем всего в одном грамме испражнений может содержаться до 15 тысяч возбудителей, что обуславливает мгновенность и высокую степень заражения человека.
Согласно статистическим данным, в России с целью лечения токсокароза к специалистам обращается 0,007-0,0007% населения в зависимости от региона.
Пути заражения и последствия
Основной причиной попадания токсокары в организм является несоблюдение личной гигиены. Источниками могут являться:
- шерсть и слюна зараженного животного,
- загрязненные бытовые предметы,
- грязные руки,
- плохо промытые овощи и фрукты,
- зараженная вода.
Известны единичные случаи передачи паразита ребенку с молоком матери во время грудного вскармливания, через плаценту, а также при употреблении в пищу некачественно приготовленного мяса, зараженного личинками.
После попадания в организм возбудитель мигрирует с током крови.
Токсокара способна поражать такие органы, как:
- органы ЖКТ,
- легкие,
- сердце,
- головной мозг,
- мышечные ткани,
- глаза.
На протяжении длительного времени патология себя никак не проявляет, одним из наиболее тревожных звонков является выраженное снижение иммунитета.
Симптомы токсокароза
Заболевание может протекать в латентной, стертой или манифестной формах. Последняя отличается ярко выраженной симптоматикой и наиболее характерна для детей до 11 лет. Взрослые чаще сталкиваются со стертой формой гельминтоза. Течение патологии более трех месяцев считается хроническим.
Симптомы заболевания зависят от области поражения. В связи с этим выделяются следующие формы:
-
Висцеральная.
Характеризуется поражением внутренних органов. Сопровождается аллергическими реакциями, интоксикацией, кашлем, одышкой, нарушением стула, неприятным привкусом в полости рта, метеоризмом, болями в животе и снижением веса. Особенно часто страдают печень, желчный пузырь,кишечник. При длительном течении заболевания возможны внутренние кровотечения.
-
Кожная.
Характеризуется формированием очагов с выраженным покраснением, зудом и болью. Часто ощущается движение под кожей.
-
Глазная.
Атаке подвергаются мышечные ткани и глазная орбита. Возбудитель вызывает воспаление конъюнктивы, отек тканей, боль и снижение остроты зрения вплоть до полной слепоты.
-
Неврологическая.
Наиболее тяжелая форма течения. При попадании глиста в головной мозг отмечаются сильные головные боли, рвота, напряжение шейных мышц, повышенная чувствительность, выраженная слабость, проблемы с вестибуляцией. У маленьких детей данная форма заболевания может привести к выраженной задержке развития и приступам немотивированной агрессии.
Обратиться к врачу рекомендуется как при появлении перечисленных жалоб,так и при высоком риске инфицирования (контакте с зараженным источником).
Обследование на паразита
Токсокароз, как и любое другое паразитарное заболевание, часто протекает скрыто. Поэтому для постановки точного диагноза будет недостаточно ограничиться лишь сдачей анализов крови.
Необходимо полное обследование,включающее следующие этапы:
- прием гастроэнтеролога, включающий в себя опрос, оценку жалоб, визуальный осмотр, пальпацию живота, аускультацию легких;
- ОАК — при токсокарозе характерно повышение СОЭ, эозинофилов, лейкоцитов и снижение гемоглобина;
- ИФА — для выявления уровня антител и антигенов в сыворотке крови;
- анализ кала по методу Парасепта;
- дуоденальное зондирование с последующим анализом содержимого.
Дополнительно,исходя из жалоб пациента на момент обращения, проводят УЗИ внутренних органов.
Лечение заболевания
При подозрении на заражение необходимо пройти комплекс вышеописанных диагностических процедур, после чего будет назначено лечение.
Самостоятельный прием препаратов категорически запрещен, так как может привести не только к искажению симптомов, но и к ухудшению состояния.
Лечение токсокароза выполняется в три этапа:
-
Подготовительный.
Включает снятие интоксикации, поддержание пораженных органов, стабилизацию состояния больного. Выполняется с применением физиотерапевтических процедур на аппаратахMAG-Expert, IONOSON-expert.
-
Основной.
Прием противопаразитарных препаратов. Препараты и дозировкаопределяютсяиндивидуально лечащим врачом.
-
Восстановление.
Выведение паразитов посредством интрадуоденального промывания, курс физиотерапии на аппаратах MAG-Expert, IONOSON-expert. Прием препаратов для снижения риска аллергической реакции на токсины паразита. Препараты назначаются врачом.
Добиться полного выздоровления можно только при четком соблюдении всех рекомендаций лечащего врача и пройдя все вышеуказанные этапы лечения.
Для диагностики и лечения паразитозов мы разработали специальные комплексные программы: «Обследование на паразитозы» и «Лечение паразитозов (описторхоз, лямблиоз, токсокароз)».
Медицинская клиника «Аванта-Мед» в Новосибирске предлагает сдать анализ на описторхоз, и пройти комплексное обследование и эффективное лечение по выгодной цене. Записаться на первичную консультацию к специалисту на удобное для вас время вы можете, позвонив нам по телефону 8 (383) 349-93-03.
Токсокароз: история болезни, виды, диагностика, лечение
Токсокароз — это заражение личинками аскариды собак ( Toxocara canis ) и кошек ( Toxocara cati ). Яйца круглых червей из фекалий собак и кошек часто встречаются в почве и песке в парках, общественных пляжах и других местах на открытом воздухе.
В нормальном жизненном цикле яйца аскариды попадают в организм другой собаки или кошки, а личинка мигрирует через стенку кишечника. Взрослые черви развиваются в тонком кишечнике и откладывают яйца, которые выводятся с калом, где они снова становятся заразными в почве.
Люди не являются естественными хозяевами, но могут заразиться, случайно проглотив яйца из почвы. Личинки вылупляются и проникают через стенку кишечника, путешествуя по другим частям тела, таким как печень, сердце и мозг. У человека личинки не развиваются в зрелых червей и не откладывают новые яйца. Однако они вызывают болезнь. Есть три общепризнанных синдрома.
Личинки Toxocara canis второй стадии вылупляются из яиц — Авторское право изображения: olgaru79 / Shutterstock
Типы токсокароза
Скрытый токсокароз встречается у детей.Это вызывает легкое заболевание с повышением температуры тела. Другие возможные симптомы включают кашель, плохой сон, головные боли и боли в животе. У детей могут появиться признаки инфицированных лимфатических узлов, опухшей печени или хрипов. Считается, что скрытый токсокароз вызывается длительным воздействием мигрирующих молодых червей.
Visceral larva migrans (VLM) — воспалительная реакция, вызванная гибелью личинок, мигрирующих через внутренние органы. В первую очередь он поражает детей в возрасте до пяти лет.С VLM:
связан ряд симптомов.- усталость
- потеря веса
- анорексия
- лихорадка
- кашель
- пневмония
- Бронхоспазм
- Боль в животе
- головная боль
- сыпь
- изъятий (редко)
Также могут присутствовать опухшая печень, инфицированные лимфатические узлы и хрипы. Могут развиться серьезные осложнения, такие как плевральный выпот, хроническая крапивница (крапивница), миокардит и дыхательная недостаточность.
Когда личинки мигрируют в глаза ( глазных мигрирующих личинок ), они могут вызвать проблемы со зрением, покраснение глаз или появление белого зрачка (лейкокории). Хориоретинит — воспаление сосудистой оболочки и сетчатки — и гранулемы — типичные наблюдения при осмотре. OLM может вызвать потерю зрения, фиброз сетчатки, ретинобластому и отслоение сетчатки.
OLM чаще всего встречается у детей в возрасте от пяти до десяти лет.
Диагностика токсокароза
VLM следует заподозрить у любого ребенка с необъяснимым фебрильным заболеванием и эозинофилией (увеличение определенного типа лейкоцитов).Мультисистемное заболевание, опухшая печень и употребление грязи в анамнезе — это другие признаки того, что у ребенка может быть ВЛМ. Ключевыми симптомами OLM являются односторонняя потеря зрения и косоглазие (смещение глаз).
Окончательный диагноз VLM может быть поставлен путем тестирования на общие антигены круглых червей и вещество группы крови А. Однако эти иммунологические тесты не являются надежными для OLM, потому что пациенты, как правило, имеют более низкие уровни антигена круглого червя в крови. ОЛМ диагностируется при офтальмологическом обследовании.
Лечение
Стандартное лечение токсокароза — пятидневный курс альбендазола. Иногда к нему добавляют кортикостероиды, чтобы подавить аллергическую реакцию на круглых червей. Для OLM предпочтительными методами лечения являются хирургическое вмешательство, стероиды и противоглистная (противопаразитарная) химиотерапия.
Дополнительная литература
CDC — Токсокароз — Ресурсы для медицинских работников
Диагностика висцерального токсокароза или глазного токсокароза основывается на наличии признаков VT или OT и истории контакта с потенциальным источником инфекционных яиц или личинок Toxocara (например,грамм. в недоваренном зараженном мясе или субпродуктах). Диагноз висцерального токсокароза основывается на совместимом заболевании и истории воздействия с положительными результатами серологического тестирования. В настоящее время рекомендуемый тест — это иммуноферментный анализ (ELISA) с антигенами личиночной стадии, обычно экскреторные / секреторные антигены высвобождаются при культивировании инфекционных личинок Toxocara . Специфичность этого анализа хорошая, хотя возможна перекрестная реактивность с антителом к человеческому круглому червю, Ascaris lumbricoides ; однако анализы с использованием экскреторных / секреторных антигенов Toxocara сводят к минимуму эту проблему.Положительные серологические результаты следует интерпретировать с учетом клинического статуса пациента. Обнаруживаемые антитела могут быть результатом инфекции в прошлом. Кроме того, серопозитивность может проявляться при бессимптомной инфекции Toxocara . Парные образцы сыворотки, демонстрирующие значительное повышение уровня антител с течением времени, могут быть полезны для подтверждения активной инфекции.
При глазном токсокарозе уровни антител Toxocara в сыворотке могут быть низкими или отсутствовать, несмотря на клиническое заболевание.В некоторых случаях антитело Toxocara может быть обнаружено в образцах водной или стекловидной жидкости из пораженного глаза и может быть связано с местным образованием антител или утечкой антител из кровотока. Образец глазной жидкости может быть исследован при более низком разведении, чем сыворотка, для повышения чувствительности ELISA.
Признаки и симптомы VT или ОТ могут быть вызваны мигрирующими личинками других гельминтов, включая Baylisascaris procyonis (как VT, так и ОТ), Strongyloides spp.(VT) и Paragonimus spp. (VT). Для дифференциальной диагностики может быть полезно пристальное внимание к течению заболевания, истории воздействия и серологическому анализу. Для ОТ, если личинка визуализируется в глазу, измерение размера может помочь отличить более крупные личинки Baylisascaris от Toxocara или других личинок.
Проявления токсокароза отражают количество мигрирующих личинок, когда личинки мигрировали в организме, а также степень иммунного ответа и воспаления, развившегося в ответ на присутствие личинок.Многие инфекции протекают бессимптомно. При тяжелых инфекциях большое количество личинок может мигрировать через печень, легкие или другие внутренние органы, вызывая воспаление и симптоматическое заболевание (ЖТ). В редких случаях личинки могут мигрировать в центральную нервную систему (ЦНС), вызывая эозинофильный менингоэнцефалит или образование гранулем в ЦНС. Признаки ЖТ включают жар, кашель, хрипы, боли в животе и гепатомегалию. Часто присутствует эозинофилия. Висцеральный токсокароз был предложен как причина астмы; однако могут быть многофакторные причины астмы, и необходимы дальнейшие исследования для установления причинной связи между токсокарозом и астмой.
Обычно ОТ представляет собой одностороннее заболевание, когда личинка проникает в единственный глаз. Общие признаки связаны с гранулематозным воспалением, особенно сетчаткой, увеитом и / или хориоретинитом. Пациенты могут иметь лейкокорию и снижение зрения в пораженном глазу, что можно принять за ретинобластому. Может развиться диффузный односторонний подострый нейроретинит или связки стекловидного тела.
Лечение альбендазолом или мебендазолом показано при висцеральном токсокарозе, хотя оптимальная продолжительность лечения не определена.Оба препарата метаболизируются в печени; Длительное применение альбендазола (от недель до месяцев) привело к развитию панцитопении у некоторых пациентов с нарушением функции печени. Пациенты, находящиеся на длительном лечении, должны контролироваться серийным подсчетом клеток крови. Однако альбендазол использовался для лечения миллионов пациентов во всем мире и в кампаниях массового введения лекарств, и он считается безопасным лекарством с низкими показателями токсичности. В дополнение к противопаразитарной терапии может быть показана симптоматическая терапия, включая лечение стероидами для контроля воспаления.
| Лекарство | Доза и продолжительность |
|---|---|
| Альбендазол | 400 мг внутрь два раза в день в течение пяти дней (доза для взрослых и детей) |
| Мебендазол | 100-200 мг внутрь два раза в день в течение пяти дней (доза для взрослых и детей) |
Альбендазол для перорального применения доступен для использования людьми в США.
Мебендазол для перорального применения доступен для использования людьми в США.
При глазном токсокарозе цель лечения — минимизировать повреждение глаза. Системное противопаразитарное лечение альбендазолом или мебендазолом в тех же дозах, что и при висцеральном заболевании, может быть полезным при активном заболевании. Попытки удалить личинку хирургическим путем могут оказаться безуспешными. Может быть показан контроль воспаления в глазу с помощью местных или системных стероидов. Для пациентов с нездоровой болезнью улучшение результатов может быть результатом хирургического вмешательства для предотвращения дальнейшего повреждения из-за хронического воспаления.
Выявление и лечение глазного токсокароза
Аджай Сингх, доктор медицины, E.T. Каннингем-младший, доктор медицины, доктор медицинских наук, магистр здравоохранения, и Джей М. Стюарт, доктор медицины, Сан-ФранцискоДиагностика глазного токсокароза может быть сложной задачей как потому, что это состояние относительно необычно, так и потому, что его проявления обычно варьируются от пациента к пациенту. В недавнем исследовании распространенности, клинических особенностей и причин потери зрения у пациентов с глазным токсокарозом, проведенном в больнице Фрэнсиса I.Proctor Foundation, Калифорнийский университет, Сан-Франциско, общая распространенность инфекции глаза Toxocara была относительно низкой и составляла 1 процент от общей популяции увеита.1 Тем не менее, глазной токсокароз остается важной причиной увеита, особенно у детей и подростков. Взрослые.
Заражение человека нематодами Toxocara canis или Toxocara cati может вызывать как системный, так и глазной токсокароз. Окончательными хозяевами для этих видов нематод являются собаки и кошки соответственно.Люди заражаются этим заболеванием при проглатывании яиц с зародышем, обычно из зараженных сырых овощей или инфицированного сырого мяса (курица, кролик и баранина), 2 из загрязненных источников воды или через геофагию. Большинство повреждений глаз возникает в результате воспалительной реакции, которая возникает после смерти личинки. По причинам, которые до конца не изучены, глазной и системный токсокароз обычно диагностируют у пациентов разного возраста. В частности, было замечено, что системный токсокароз, также называемый мигрирующими висцеральными личинками, как правило, поражает детей в возрасте до 3 лет, возможно, из-за повышенной частоты пика среди этой группы, 3 тогда как глазной токсокароз обычно проявляется у детей старшего возраста и молодых Взрослые.
Клиническая презентация
Глазной токсокскаридоз является односторонним у 90 процентов пациентов.1,4,5 Традиционно считается, что это заболевание поражает в первую очередь младенцев и детей младшего возраста, но недавние исследования выявили случаев заражения токсокарой у ряда подростков и молодых людей. . Неизвестно, вызван ли этот сдвиг в демографии более глубоким пониманием эпидемиологии глазного токсокароза, изменением схемы направления к специалистам или истинным изменением групп риска.1,5 Контакт с домашними собаками и кошками, особенно с щенками и котятами, которые с большей вероятностью переносят инфекцию, считается важным фактором риска для детей. Общие симптомы, которые приводят пациентов в клинику, включают нечеткое зрение и плавающие помутнения. Также могут присутствовать боль и светобоязнь, но обычно они незначительны6. У молодых пациентов глазная инфекция может быть незаметна до тех пор, пока они не пройдут проверку зрения в школе или не разовьются косоглазие или лейкокория.
Рисунок 1.Два отдельных пациента (A и B) с излеченными гранулемами заднего полюса вследствие токсокароза глаза. Обратите внимание на заметные складки сетчатки и образование эпиретинальной мембраны. |
Глазной токсокароз проявляется в виде гранулемы заднего полюса (см. Рисунок 1) у 25–50 процентов пациентов.1,4,5,6 Причина такой очевидной склонности к заднему полюсу неясна. , хотя было высказано предположение, что гематогенно распространяющиеся нематоды могут с большей вероятностью поселиться в небольших перифовеальных концевых артериях.И наоборот, может быть просто то, что поражения желтого пятна, скорее всего, будут симптоматическими и, следовательно, побудить пациентов обратиться за медицинской помощью. Остро, Toxocara retinochoroiditis выглядит как мутное, плохо очерченное белое пятно с покрывающим его витритом. Когда воспаление проходит, поражение становится отчетливым, хорошо разграниченным, приподнятым белым образованием размером от половины до четырех диаметров диска. Нарушение пигментного эпителия сетчатки часто окружает поражение, и складки сетчатки, отходящие от очага поражения, встречаются довольно часто.При ближайшем рассмотрении можно обнаружить темно-серый центр, который, как предполагалось, является остатками личинки 6,7, а также кровеносные сосуды сетчатки, входящие в гранулему. Toxocara гранулемы также могут развиваться на диске зрительного нерва, и в этом случае потеря зрения может быть значительной; может присутствовать афферентный зрачковый дефект, и обследование глазного дна может выявить перипапиллярную отслойку и / или экссудаты сетчатки по типу макулярной звезды (нейроретинит).
Около 50 процентов всех глаз с токсокарозом проявляются в виде периферической гранулемы (см. Рисунок 2) .1,4,5,6 В острой форме поражение выглядит как мутная белая масса на периферическом дне глазного дна, которая может имитировать сугроб, наблюдаемый у пациентов с парспланитом. Со временем консолидация и сокращение поражения приводит к появлению периферической приподнятой массы, часто с расширяющимися кзади складками сетчатки (см. Рис. 3) . В некоторых случаях экссудаты сетчатки могут быть обширными.
| Рис. 2. Два отдельных пациента с периферическими гранулемами из-за глазного токсокароза.Обратите внимание на заметные, расширяющиеся кзади складки сетчатки и, в случае А, обширный экссудат. |
Менее 25 процентов глаз с токсокарозом имеют плотное воспаление стекловидного тела, имитирующее эндофтальмит (см. Рисунок 3) .1,4,6 В отличие от многих других форм увеита, признаки эндофтальмита Toxocara часто более выражены. выражено, чем симптомы. Фактически, как уже отмечалось, боль и светобоязнь обычно минимальны или отсутствуют. При обследовании с помощью щелевой лампы обычно выявляется легкая или умеренная вторичная реакция передней камеры с разбросанными небольшими кератическими осадками на эндотелии роговицы.Задние синехии могут развиваться время от времени, но нечасто. Образование гипопиона, хотя и сообщается, встречается редко8. Визуализация глазного дна через воспаление стекловидного тела обычно затруднена. В тяжелых случаях может развиться экссудативная отслойка сетчатки. Когда воспаление спадает, стекловидные оболочки могут образовывать ретролентальную массу, которая в тяжелых случаях может вызывать отслоение цилиарного тела, гипотонию и туберкулез.
Основные причины потери зрения у пациентов с глазным токсокарозом в значительной степени зависят от локализации и тяжести воспаления.Зрение обычно ухудшается у пациентов с эндофтальмитом Toxocara из-за помутнения воспалительной среды, кистозного макулярного отека и / или образования катаракты. Гранулемы заднего полюса, напротив, обычно вызывают потерю зрения из-за прямого поражения желтого пятна или диска зрительного нерва, вторичного образования сетчатых складок или эпиретинальных мембран или, в редких случаях, развития хориоидальной неоваскуляризации. Снижение зрения у пациентов с токсокарозом периферических глаз обычно является следствием поражения желтого пятна в виде простирающихся кзади серповидных складок или экссудата.Кроме того, амблиопия может развиться у молодых пациентов с помутнением срединного слоя и / или поражением желтого пятна.
Рисунок 3. Эндофтальмит токсокар. Обширный витрит скрывает детали глазного дна, так что диск зрительного нерва (стрелка) едва виден. |
Диагностика
Хотя анамнез, обзор систем и полное обследование глаз при расширении являются наиболее важными, несколько дополнительных тестов также могут быть полезны в диагностике токсокароза глаз.Эозинофилия сыворотки указывает на инфекцию, но обычно присутствует только в условиях активной системной инфекции. Эозинофилы, обнаруженные в водной или стекловидной жидкости, являются более прямым индикатором глазной инфекции, но такие жидкости редко доступны для тестирования. Анализы для обнаружения антител против Toxocara в сыворотке используются наиболее часто и могут быть полезны для подтверждения клинического диагноза, но, как известно, они мало чувствительны. Повышенная чувствительность может быть достигнута с помощью анализа внутриглазных жидкостей с помощью ELISA 9,10, но такое тестирование доступно только в нескольких изолированных исследовательских центрах.Таким образом, во всех смыслах и целях глазной токсокароз часто является клиническим диагнозом.
Методы визуализации могут предоставить дополнительную информацию многим пациентам. Оптическая когерентная томография гранулем заднего полюса обычно демонстрирует высоко отражающую массу, расположенную над RPE11, а также может показать факторы, потенциально способствующие потере зрения, такие как наличие интраретинальной или субретинальной жидкости. В-сканирование УЗИ особенно полезно, когда витрит или другие помутнения не позволяют увидеть глазное дно.
Редко диагноз глазного токсокароза ставится гистопатологически после идентификации мертвой личинки в центре эозинофильной гранулемы (см. Рисунок 4) .
Лечение
Решение о начале терапии зависит от стадии инфекции. Клинические проявления в состоянии покоя без активного воспаления не требуют противовоспалительного или противоглистного лечения. Для тех редких пациентов, которые обращаются с поражением глаз на фоне висцеральной мигрирующей личинки, наиболее эффективным является системное лечение одним из производных бензимидазола (альбендазолом, тиабендазолом и мебендазолом) в сочетании с местными и / или системными кортикостероидами по показаниям.12,13 Хотя сравнительных исследований нет, лучшая переносимость альбендазола и его общедоступность в большинстве стран делают его предпочтительным противоглистным препаратом в большинстве случаев.
Кортикостероиды можно вводить местно, периокулярно, внутриглазно или системно, в зависимости от локализации и тяжести воспаления. Циклоплегия / мидриатика часто показана при воспалении передней камеры, чтобы минимизировать риск образования задних синехий, и ее следует выбирать и дозировать в зависимости от тяжести воспаления.У выбранных пациентов следует рассмотреть возможность витрэктомии Pars plana для удаления воспалительных тканей, снятия тракции витреомакулярного тракта и устранения отслоения сетчатки (см. Рисунок 5) ,14 Были также предприняты попытки хирургического удаления живой личинки из субретинального пространства15. подвижную личинку можно уничтожить с помощью лазерной фотокоагуляции.
Профилактика
Надлежащая утилизация наполнителя для туалета, дегельминтизация инфицированных домашних животных, полное приготовление мяса, тщательное ополаскивание фруктов и овощей и надлежащая практика мытья рук являются важными мерами предотвращения заражения человека.16 Накрытие песочниц на общих детских площадках и открытых огородах также полезно, поскольку помогает предотвратить заражение, а повышение температуры, вызванное независимым укрытием, способствует уничтожению существующих яиц.
Рис. 4. Окрашенный H&E срез периферической сетчатки, показывающий мертвую личинку Toxocara canis в центре эозинофильной гранулемы. Этот срез был вырезан из исходного гистопатологического блока, который был впервые изучен и опубликован в 1965 году.19 |
Хотя в настоящее время молекулярные вакцины не доступны, они могут когда-нибудь оказаться полезными для борьбы с заражением собак и кошек. К настоящему времени миозинов Toxocara были идентифицированы как потенциальные кандидаты в антигены для такой вакцины18.
Для диагностики глазного токсокароза требуется высокий индекс подозрительности. Чаще всего страдают дети и молодые люди. Воспаление обычно одностороннее с одним из трех проявлений: гранулема заднего полюса, периферическая гранулема или эндофтальмит Toxocara .Анализ сыворотки на антитела против Toxocara может быть полезным, но, как известно, он нечувствителен, поэтому к отрицательным результатам следует относиться с осторожностью. Часто бывает полезным визуализация, особенно ОКТ и В-сканирование. Большинству пациентов с глазным токсокарозом полезно лечение кортикостероидами, но не антигельминтными средствами, поскольку воспаление возникает в результате реакции организма на мертвого червя. Однако при активной системной инфекции или при офтальмоскопическом наблюдении живой подвижной личинки следует рассмотреть возможность применения противоглистного агента.Витрэктомия Pars plana показана избранным пациентам с длительно существующими обломками стекловидного тела, тракцией или регматогенной отслойкой сетчатки14
Рис. 5. Гранулема заднего полюса у 10-летней девочки с домашним скунсом и двухмесячным анамнезом ухудшения зрения и плавающими помутнениями, поражающими ее левый глаз (A). Зрение на презентации было 20/100. Сывороточный IgG к токсокарам был положительным при разведении 1:16.Для иссечения гранулемы и удаления эпиретинальных мембран была выполнена витрэктомия pars plana (B). Окончательный послеоперационный обзор был 20/25.
Д-р Сингх — научный сотрудник, а д-р Стюарт — преподаватель кафедры офтальмологии Медицинской школы UCSF. Свяжитесь с ними в отделении офтальмологии Медицинской школы UCSF, 10 Koret Way, K301, Сан-Франциско, Калифорния 94143-0730, телефон: (415) 476-0496, факс: (415) 476-0336, электронная почта: stewartj @ Vision.ucsf.edu.
Доктор Каннингем — директор службы увеитов Калифорнийского Тихоокеанского медицинского центра и клинический профессор офтальмологии Медицинской школы Стэнфордского университета. Свяжитесь с ним в West Coast Retina Medical Group, Inc., 185 Berry St., Lobby 5, Suite 130, San Francisco, CA 94107-1739. Телефон: (415) 972 4600, факс: (415) 975 0999, электронная почта: [email protected]
1. Стюарт JM, Cubillan LD, Cunningham ET Jr. Распространенность, клинические особенности и причины потери зрения среди пациентов с глазным токсокарозом.Retina 2005; 25: 1005-13.
2. Нагакура К., Татибана Х., Канеда Й., Като Ю. Токсокароз, возможно, вызванный употреблением в пищу сырого цыпленка. Журнал Infect Dis 1989; 160: 735-6.
3. Шанц PM, Weis PE, Pollard ZF, et al. Факторы риска токсокаральной мигрирующей глазной личинки: исследование случай-контроль. Am J Public Health 1980; 70: 1269.
4. Wilkinson CP, Welch RB. Внутриглазные токсокары. Am J Ophthalmol 1971; 71: 921-30.
5. Ёкои К., Гото Х., Сакаи Дж., Усуи М.Клинические особенности глазного токсокароза в Японии. Ocul Immunol Inflamm 2003; 11: 269-75.
6. Щиты JA. Глазной токсокароз. Обзор. Surv Ophthalmol 1984; 28: 361-81
7. Foster CS. Глазной токсокароз. В: Фостер и Витале. Диагностика и лечение увеита. Филадельфия: W.B. Сондерс, 2002: 428-436.
8. Аппельманс М., Михильс Дж., Рокет П. Увеит с эозинофильным гипопионом, вызванный личинками нематод. Bull Soc Belge Ophtalmol 1965; 140: 505-12
9.Магнавал Дж. Ф., Малард Л., Морассин Б., Фабр Р. Иммунодиагностика глазного токсокароза с использованием вестерн-блоттинга для обнаружения специфических антител к Toxocara IgG и CAP для измерения специфических антител к Toxocara IgE. Дж. Гельминтол 2002; 76: 335-9.
10.Benitez del Castillo JM, Herreros G, Guillen JL. Двусторонний глазной токсокароз, продемонстрированный иммуноферментным анализом водянистой влаги. Am J Ophthalmol 1995; 119: 514-6.
11. Хигашидэ Т., Акао Н., Сирао Э., Сирао Ю.Результаты оптической когерентной томографии и ангиографии пациента с субретинальной гранулемой токсокар. Am J Ophthalmol 2003; 136: 188-90.
12. Sturchler D, Schubarth P, Gualzata M, Gottstein B, Oettli A. Тиабендазол против альбендазола в лечении токсокароза: клиническое испытание. Энн Троп Мед Паразитол 1989; 83: 473-8.
13. Sabrosa NA, de Souza EC. Нематодные инфекции глаз: токсокароз и диффузный односторонний подострый нейроретинит. Curr Opin Ophthalmol 2001; 12: 450–454.
14. Amin HI, McDonald HR, Han DP, Jaffe GJ, et al. Обновление витрэктомии для тракции желтого пятна при глазном токсокарозе. Сетчатка 2000; 20: 80-5.
15. de Souza EC, Nakashima Y. Диффузный односторонний подострый нейроретинит. Отчет о трансвитреальном хирургическом удалении субретинальной нематоды. Офтальмология 1995; 102: 1183-6.
16. Харви Дж. Б., Робертс Дж. М., Шанц П. М.. Обзор рекомендаций ветеринаров по лечению кишечных паразитов у собак и борьбе с ними: значение для общественного здравоохранения.J Am Vet Med Assoc 1991; 199: 702-7.
17. Уга С., Катаока Н. Меры по контролю заражения яиц токсокарами в песочницах общественных парков. Am J Trop Med Hyg 1995; 52: 21-4.
18. Обваллер А., Дюшен М., Брюн Н., Штайпе В, Трипп С., Крафт Д., Видерманн Г., Ауэр Н., Аспок Н. Рекомбинантное рассечение тяжелой цепи миозина Toxocara canis показывает сильную кластеризацию антигенных областей. Parasitol Res 2001; 87: 383-9.
19. Хоган MJ, Кимура SJ, Спенсер WH.Мигрирующая висцеральная личинка и периферический ретинит. JAMA 1965; 194: 1345-7.
Медицинская помощь, хирургическая помощь, консультации
Автор
Сунь Ху, доктор медицины, доктор философии Председатель, профессор кафедры паразитологии Медицинского колледжа Халлимского университета, Республика Корея
Раскрытие информации: не подлежит разглашению.
Соавтор (ы)
Су-Унг Ли, доктор философии , менеджер по исследованиям и разработкам, Chuncheon Bioindustry Foundation, Корея
Раскрытие информации: не подлежит разглашению.
Специальная редакционная коллегия
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Получил зарплату от Medscape за работу. для: Medscape.
Гордон Л. Вудс, доктор медицины Консультант, отделение внутренней медицины, Университетский медицинский центр
Гордон Л. Вудс, доктор медицины, является членом следующих медицинских обществ: Общество общей внутренней медицины
Раскрытие информации: не подлежит разглашению.
Главный редактор
John L Brusch, MD, FACP Член-корреспондент Гарвардской медицинской школы; Персонал-консультант, Департамент медицины и Службы инфекционных заболеваний, Кембриджский альянс здравоохранения
Джон Л. Бруш, доктор медицинских наук, FACP является членом следующих медицинских обществ: Американский колледж врачей, Американское общество инфекционных заболеваний
Раскрытие информации: не подлежит разглашению.
Дополнительные участники
Пранатхарти Харан Чандрасекар, MBBS, MD Профессор, заведующий отделением инфекционных болезней, факультет внутренней медицины, Медицинский факультет Государственного университета Уэйна
Пранатхарти Харан Чандрасекар, бакалавр медицины и медицины, является членом следующих медицинских обществ: Американский колледж врачей , Американское общество микробиологии, Международное принимающее общество с ослабленным иммунитетом, Американское общество инфекционных заболеваний
Раскрытие: Ничего не раскрывать.
клинических признаков, диагностика, лечение и профилактика
Asia Pac Allergy. 2014 июл; 4 (3): 134–141.
, 1, 2 , 1 и 1Сон Джун Ан
1 Кафедра офтальмологии, Больница Бунданг Сеульского национального университета, Медицинский колледж Сеульского национального университета, Соннам, 463-707 Корея.
2 Отделение офтальмологии, Столичный госпиталь Вооруженных сил, Соннам 463-040, Корея.
Na-Kyung Ryoo
1 Отделение офтальмологии, Госпиталь Бунданг Сеульского национального университета, Медицинский колледж Сеульского национального университета, Соннам 463-707, Корея.
Се Джун Ву
1 Отделение офтальмологии, Больница Бунданг Сеульского национального университета, Медицинский колледж Сеульского национального университета, Соннам 463-707, Корея.
1 Отделение офтальмологии, Госпиталь Бунданг Сеульского национального университета, Медицинский колледж Сеульского национального университета, Соннам 463-707, Корея.
2 Отделение офтальмологии, Столичный госпиталь Вооруженных сил, Соннам 463-040, Корея.
Автор, ответственный за переписку. Переписка: Се Джун У. Отделение офтальмологии, Больница Бунданг Сеульского национального университета, Медицинский колледж Сеульского национального университета, 82 Gumi-ro 173beon-gil, Bundang-gu, Seongnam 463-707, Корея. Тел .: + 82-31-787-7377, Факс: + 82-31-787-4057, rk.ca.uns@1noojesПоступила в редакцию 20 июля 2014 г .; Принято 23 июля 2014 г.
Copyright © 2014.Азиатско-Тихоокеанская ассоциация аллергии, астмы и клинической иммунологии. Это статья в открытом доступе, распространяемая в соответствии с условиями некоммерческой лицензии Creative Commons Attribution (http://creativecommons.org/licenses/by-nc/3.0/), которая разрешает неограниченное некоммерческое использование, распространение и воспроизведение на любом носителе при условии правильного цитирования оригинальной работы. Эта статья цитируется в других статьях PMC.Abstract
Несмотря на то, что токсокароз человека является одной из самых распространенных зоонозных инфекций во всем мире, он остается одной из забытых тропических болезней.Хотя большинство инфекций человека протекает бессимптомно, классически признаются два основных синдрома токсокароза человека: системный токсокароз, который включает заболевания основных органов; и глазной токсокароз (ОТ), заболевание глаза или зрительного нерва, вызванное миграцией личинок токсокар в глаз. ОТ обычно является односторонним заболеванием, которое обычно проявляется в виде гранулемы сетчатки, желтоватого или беловатого воспалительного образования в заднем полюсе или периферической сетчатке. Сама гранулема или другие сопутствующие заболевания, такие как эпиретинальная мембрана, отек желтого пятна и отслоение сетчатки, могут привести к необратимому повреждению сетчатки и потере зрения на глазах при ОТ.Клинический диагноз ОТ диагностируется путем выявления клинических признаков при офтальмологическом обследовании. Серологические тесты, такие как иммуноферментный анализ (ELISA) для обнаружения сывороточных антител против личинок Toxocara, могут подтвердить диагноз. Кроме того, сывороточный иммуноглобулин E и обнаружение антител к токсокарам в глазной жидкости с помощью ELISA могут оказать дополнительную помощь в диагностике. Стандартное лечение ОТ — кортикостероиды у пациентов с активным внутриглазным воспалением. Хотя роль противогельминтной терапии неясна, сообщалось о благоприятном исходе комбинированной терапии кортикостероидами и альбендазолом в глазах с активным воспалением.Профилактика за счет повышения осведомленности общественности и снижения риска заражения также важна. Недавно сообщалось о связи между употреблением сырого мяса или печени и токсокарозом, особенно у взрослых пациентов. Необходимо провести дальнейшие исследования потенциального источника инфекции, диагностики и лечения.
Ключевые слова: Диагностика, Токсокароз, Лечение, Окулярный токсокароз
ТОКСОКАРИАЗ, ГЛАЗНЫЙ ТОКСОКАРИАЗ
Токсокароз — одна из самых распространенных зоонозных инфекций во всем мире, чаще всего вызываемая Toxocara canis , реже — Toxocara canis , а реже — другими возбудителями. [1, 2].Токсокароз распространяется по всему миру, а серопозитивность антител к токсокарам колеблется от 2,4% [3] до 76,6% [4]. Исторически сложилось так, что в 1952 году Бивер и др. [5] идентифицировали этиологический агент, личинок T. canis , в эозинофильных гранулемах в биоптатах печени трех детей. Четыре года спустя Николс [6] продемонстрировал присутствие личинок второй стадии T. canis на гистологических срезах 24 глаз, энуклеированных при подозрении на внутриглазные злокачественные новообразования.Эти данные привели к общей этиологии системных и глазных заболеваний — токсокарозу человека.
Люди заражаются Toxocara, когда они непреднамеренно проглатывают зародыши яиц или личинок, которые были пролиты с фекалиями инфицированных животных или сырых паратеновых хозяев () [1, 2, 7]. После того, как человек проглотил яйца, инфекционные личинки высвобождаются в тонкий кишечник, а затем они проникают через стенку кишечника, попадают в кровоток и мигрируют в органы, где вызывают воспалительные реакции и симптомы [1, 2].Клинический спектр токсокароза у людей варьируется от бессимптомной инфекции до тяжелого поражения органов, в зависимости от паразитарной нагрузки, мест миграции личинок и воспалительной реакции хозяина [1]. В частности, в зависимости от пораженного органа могут возникать два четко определенных клинических синдрома: системный токсокароз (также известный как мигрирующая висцеральная личинка) и глазной токсокароз (ОТ) [1].
Упрощенный рисунок, показывающий жизненный цикл Toxocara canis , а также пути его передачи и миграции у человека.
ОТ — это клинически четко выраженное проявление внутриглазной инфекции, вызванной личинками токсокар [1, 7]. ОТ затрагивает как детей, так и взрослых, средний возраст начала заболевания колеблется от 6,4 [8] до 51,7 [9] лет в различных исследованиях. Известно, что это важная причина нарушения зрения в детстве [10]. Хотя токсокароз человека является одной из наиболее распространенных зоонозных инфекций во всем мире, существует лишь несколько отчетов, в которых оценивается частота ОТ. Например, количество случаев потери зрения в офтальмологических клиниках в Алабаме в течение 6 месяцев составило 11 случаев на 1000 пациентов, а один случай на 1000 человек в общей популяции, по оценкам, имел ОТ [11].Исследование, проведенное на ирландском языке, оценило распространенность ОТ как 9,7 на 100 000 школьников (4-19 лет) [12]. Одно японское эпидемиологическое исследование в Азии показало, что на ОТ приходится 1,1% всех случаев увеита [13]. В прошлом считалось, что большинство ОТ развивается у педиатрических пациентов. Однако в последнее время ОТ в основном страдают взрослые пациенты, особенно азиаты, что может быть связано с их пищевыми привычками [9, 14, 15]. В Корее системный токсокароз был основной причиной высокой распространенности эозинофилии, составляющей 67-87% (4.0-12,2%). Около 60-90% пациентов с системным токсокарозом употребляли в анамнезе сырую коровью печень [15]. Недостаток знаний и халатность приводят к тому, что многие пациенты с токсокарозом остаются брошенными, а часть пациентов может страдать от ОТ.
Поскольку ОТ остается относительно неизвестным широкой публике, а также клиницистам, здесь рассматриваются клинические особенности, диагностика, лечение и профилактика ОТ с акцентом на новые разработки в серологической диагностике и новые результаты клинических исследований в литературе.
КЛИНИЧЕСКИЕ ХАРАКТЕРИСТИКИ
Возраст обращения пациентов с ОТ может варьироваться от 1 до 77 лет [9, 16, 17]. В большинстве предыдущих исследований сообщалось, что это чаще встречается у мужчин, поскольку соотношение мужчин и женщин обычно было больше 1: 1 [8, 12, 18, 19, 20, 21, 22], вплоть до 4,5: 1 [23 ]. Большинство случаев были односторонними, а двусторонние случаи были менее 40% [20] в литературе. Его клинические проявления можно классифицировать по одной из четырех форм: гранулема заднего полюса, периферическая гранулема, нематодный эндофтальмит и атипичные проявления [16].
Гранулема заднего полюса (), очаговая, беловатая субретинальная или интраретинальная воспалительная масса, обычно менее 1 диаметра диска с пигментацией или без нее, присутствует в заднем полюсе с признаками острого воспаления и мутного стекловидного тела или без них [16]. Wilkinson и Welch [24] показали, что эта форма является наиболее частой формой клинической картины, составляющей 44% случаев ОТ. Поражения желтого пятна, скорее всего, будут симптоматическими и, следовательно, побуждают пациентов обращаться за медицинской помощью, что, возможно, объясняет предрасположенность к гранулеме заднего полюса.
Фотографии глазного дна гранулемы сетчатки у 67- (A) и 31-летнего мужчины (B) с глазным токсокарозом. (A) Гранулема заднего полюса выглядит как овальное поражение белого цвета на заднем полюсе сетчатки. (B) Периферическая гранулема представлена аморфной беловатой массой с тракционной мембраной и отслоением сетчатки.
Периферическая гранулема (), очаговый приподнятый белый узелок на периферии сетчатки, может иметь различную степень окружающих оболочек и пигментных изменений [16].У некоторых пациентов с периферической гранулемой воспаление может быть диффузным и проявляться в виде «сугроба» [10]. Можно наблюдать фиброцеллюлярные связки, идущие к задней части сетчатки или зрительному нерву, иногда образующие складку сетчатки. Локализованная тракция сетчатки также может привести к тракционной отслойке сетчатки или регматогенной отслойке сетчатки из-за образования отверстий или разрывов сетчатки.
Эндофтальмит нематод — это тип панувеита, проявляющийся в виде покраснения болезненного глаза с диффузным внутриглазным воспалением [16].В тяжелых случаях наблюдается гипопион и плотный клеточный инфильтрат в стекловидном теле. Гранулема сетчатки может наблюдаться через помутнение стекловидного тела по мере его исчезновения [24]; Следовательно, для дифференциальной диагностики важны кропотливые усилия по обнаружению гранулемы сетчатки. Пациенты с нематодным эндофтальмитом, как правило, немного моложе, чем пациенты с локализованной гранулемой.
Атипичные проявления включают воспаление и отек головки зрительного нерва (проявляющееся как неврит зрительного нерва), подвижность субретинальных личинок и диффузный хориоретинит [1, 7, 10].Также могут наблюдаться такие признаки переднего сегмента, как конъюнктивит, кератит, иридоциклит, очаговые узелки радужки и катаракта [1]. В нашем недавнем сообщении небольшое, круглое, белое помутнение, подобное гранулеме, перемещающееся на субкапсулярном уровне хрусталика, наблюдалось в глазах с ОТ [25].
Помимо воспаления глаз и проявлений, связанных с гранулемой, следует внимательно рассмотреть сопутствующие заболевания глаз с ОТ, так как они могут быть другими источниками потери зрения и могут прогрессировать при отсутствии лечения.Такие сопутствующие витреоретинальные патологии при ОТ включают эпиретинальную мембрану, помутнение стекловидного тела, тракционную / регматогенную отслойку сетчатки, отек желтого пятна, катаракту и отверстие желтого пятна [9, 10]. Хотя типичное проявление ОТ, гранулемы с внутриглазным воспалением, можно лечить медикаментозно, случаи с комбинированными витреоретинальными сопутствующими заболеваниями иногда требуют хирургического вмешательства для анатомического и визуального восстановления.
В нескольких отчетах указывались причины потери зрения у пациентов с ОТ. Стюарт и др.[10] сообщили, что витрит является наиболее частой причиной потери зрения при ОТ, за ним следуют кистозный макулярный отек, тракционная отслойка сетчатки и эпиретинальная мембрана. Кроме того, в глазах с макулярной гранулемой сама гранулема может привести к значительной потере зрения, поскольку она повреждает пораженную сетчатку и фоторецепторы [9]. Таким образом, причины потери зрения на глазах при ОТ можно разделить на 3 категории: повреждение сетчатки, вызванное самой гранулемой, сопутствующие заболевания сетчатки и внутриглазное воспаление.В нашей серии случаев ОТ средняя острота зрения с наилучшей коррекцией составляла 20/64 эквивалента Снеллена на исходном уровне, что было сопоставимо с эквивалентом 20/56 Снеллена при последнем посещении, когда внутриглазное воспаление в основном уменьшалось [9]. Это указывает на то, что в случаях ухудшения зрения следует учитывать и тщательно оценивать другие причины, такие как поражение сетчатки гранулемой или другие сопутствующие заболевания, во время клинического обследования пациентов с ОТ.
Примечательно, что уникальной особенностью ОТ по сравнению с другими воспалительными заболеваниями или заболеваниями сетчатки является внутриглазная миграция () [9, 26, 27].В двух описаниях клинических случаев индивидуально продемонстрирована внутриглазная миграция гранулемы [26, 27]. Было два типа внутриглазной миграции: непрерывная (гранулема мигрировала рядом с первоначально наблюдаемым местоположением) или прерывистая (новая гранулема далеко от исходного местоположения) [9]. В течение клинического периода непрерывная и прерывистая миграция гранулемы наблюдалась в 12,9% и 4,3% глаз с ОТ, соответственно [9]. Поскольку мигрирующая гранулема является патогномоничной для ОТ, эта уникальная особенность может быть полезна для дифференциации ОТ от других заболеваний сетчатки, таких как глазной токсоплазмоз, саркоидоз, туберкулез и грибковые инфекции [9].
Две модели миграции гранулемы Toxocara: непрерывная (A) и прерывистая (B). (A) Гранулема переходит на височную сторону через месяц после первого посещения (A, слева). Пунктирная линия на панели A обозначает контрольную линию, соединяющую две контрольные точки. (B) По сравнению с исходным уровнем в макуле и нижневисочной сетчатке появляются две новые гранулемы.
ДИАГНОСТИКА
Окончательный диагноз глазного токсокароза может быть получен путем гистологической демонстрации личинки токсокары или ее фрагментов при биопсии инфицированной ткани.Однако сбор подходящего биопсийного материала опасен и труден для глаз с ОТ и редко оправдан клиническими соображениями. Таким образом, современный диагноз ОТ ставится клинически по выявлению типичных офтальмологических признаков и по наличию сывороточных антител к личинкам токсокар [1, 7, 16].
Как упоминалось выше, клинические проявления локализованной гранулемы в заднем полюсе или периферии сетчатки типичны для постановки предполагаемого диагноза ОТ. В случаях нематодного эндофтальмита, при котором исследование глазного дна невозможно из-за помутнения стекловидного тела, для дифференциальной диагностики могут быть полезны специальные дополнительные тесты, такие как ультразвуковое исследование (отображение сильно отражающей массы с полосой стекловидного тела или без нее), и следует повторно выявить наличие гранулемы сетчатки. — оценивается для постановки точного диагноза, когда стекловидное тело становится прозрачным [1, 24].
Серологически стандартным современным тестом для диагностики токсокароза человека является непрямой иммуноферментный анализ (ИФА), основанный на экскреторно-секреторных антигенах T. canis . ELISA (Biokema-Affinity Products, Crissier-Lausanne, Швейцария) [28] при титре сыворотки более 1:32 имеет 78% чувствительность для выявления токсокароза [29] и Hagler et al. [30] предположили, что титр сыворотки 1: 8 достаточен для подтверждения диагноза глазного токсокароза, если у пациента есть признаки и симптомы, совместимые с этим заболеванием.В дополнение к коммерческому набору ELISA, серодиагностика с помощью ELISA с использованием неочищенного антигена личинок токсокар, разработанная исследователями из Сеульского национального университета в Южной Корее, также показала приемлемую диагностическую ценность с чувствительностью 92,2% и специфичностью 86,6% [31]. Сообщалось, что рекомбинантные антигены [32] могут предложить дополнительные решения для серологической диагностики, обеспечивая повышенную чувствительность и специфичность по сравнению с нативными экскреторно-секреторными антигенами. Однако из-за неспособности паразита развиться во взрослую форму у человека был проведен поиск T.canis или Яйца T. cati в фекалиях человека не нужны. Общенациональное исследование в США показало, что 17 из 25 пациентов (68%) с ОТ, у которых были зарегистрированы результаты ELISA, имели положительные результаты [16]. Однако чувствительность и специфичность ELISA для диагностики ОТ не были полностью оценены на больших выборках. Более того, к сожалению, такие антитела часто могут быть неопределяемыми или их титр может быть ниже порогового уровня в сыворотках пациентов с ОТ [33], возможно, из-за относительно низкой паразитарной нагрузки у пациентов с ОТ.Следовательно, отсутствие сывороточных антител не исключает диагноза ОТ. В этом случае другие дополнительные тесты могут быть полезны для подтверждения инфекции Toxocara.
В качестве дополнительного теста у пациентов с токсокарозом человека была определена роль определения антител к иммуноглобулину Е (IgE) [7, 34]. Что касается роли в ОТ, наша серия случаев на ОТ показала, что 69,6% клинически и серологически диагностированных пациентов показали повышенные уровни IgE, что позволяет предположить, что IgE может играть дополнительную роль в диагностике ОТ [9].Кроме того, уровни IgE показали снижение после лечения токсокароза человека, что указывает на то, что это может быть полезно для мониторинга терапевтического эффекта. Это требует дальнейшего изучения роли антител IgE у пациентов с ОТ.
Хотя системная эозинофилия является важным признаком системного токсокароза [14, 35, 36, 37, 38], количество эозинофилов обычно не увеличивается у пациентов с ОТ. Например, наша серия случаев показала, что только 11,6% (10 из 86) пациентов с ОТ имели эозинофилию [9].Таким образом, подсчет эозинофилов может быть не так полезен, как тест ELISA или уровень общего IgE; однако эозинофилия может указывать на возможность одновременного возникновения системного и глазного токсокароза [1, 34], что требует системной оценки и соответствующего лечения.
Некоторые авторы предположили, что улучшенная чувствительность может быть достигнута с помощью ELISA-анализа внутриглазных жидкостей [17, 33, 39]. Однако при использовании того же порогового значения для сывороточных антител положительные показатели ELISA для стекловидного тела были всего лишь 33% среди пациентов с ОТ, что требует дальнейшего исследования подходящего порогового значения для обнаружения ОТ [9].В случаях хирургического лечения остатки организмов Toxocara иногда обнаруживаются в образцах витрэктомии, полученных во время операции, что является прямым доказательством внутриглазной инфекции личинки Toxocara [40]. Цитологическое исследование водянистой влаги или стекловидного тела также может быть полезным для подтверждения диагноза ОТ. Однако в настоящее время отсутствуют доступные данные о частоте выявления цитологии стекловидного тела или биопсии среди глаз с ОТ, и, таким образом, цитология и биопсия могут быть зарезервированы для пациентов с подозрением на ОТ, которым предварительно запланирована витреоретинальная хирургия.
ЛЕЧЕНИЕ
Глаза с ОТ можно лечить медикаментозно или хирургическим путем, в зависимости от тяжести внутриглазного воспаления и сопутствующих заболеваний. Во-первых, в случае активного воспаления следует рассмотреть возможность медикаментозной терапии. В настоящее время стандартным лечением глазного токсокароза является назначение кортикостероидов пациентам с активным внутриглазным воспалением. Местные и системные кортикостероиды полезны при лечении внутриглазного воспаления и могут уменьшить помутнение стекловидного тела и образование мембран [9, 24, 39, 41, 42].
Роль антигельминтной терапии при ОТ остается спорной, поскольку не было рандомизированных контролируемых испытаний по использованию антигельминтных средств при ОТ. Опубликованы результаты лишь нескольких контролируемых испытаний глистогонных препаратов для лечения системного токсокароза [43, 44]. Поскольку невозможно точно оценить паразитологическое излечение, результатом, использованным в опубликованных испытаниях, было просто улучшение клинических признаков и симптомов. Альбендазол (400 мг 2 раза в день в течение 7-14 дней) является рекомендуемым стандартным препаратом для лечения системного токсокароза и, по-видимому, превосходит тиабендазол (принимаемый в дозе 50 мг / кг / день в течение 3-7 дней) [43], который также сильно тормозит миграцию личинок [45].Диэтилкарбамазин (вводимый в дозе 3-4 мг / кг / день в течение 21 дня, начиная с 25 мг / день для каждого взрослого пациента и постепенно увеличивая дозу) также оказался эффективным для лечения системного токсокароза [44].
Однако не доказано, что антигельминтная терапия может убить внутриглазных личинок токсокар, поскольку внутриглазные фармакокинетические и фармакодинамические исследования антигельминтных средств не проводились. Таким образом, роль антигельминтной терапии при ОТ остается неясной. Тем не менее, использование глистогонных препаратов в сочетании с кортикостероидами показало благоприятные результаты во многих исследованиях.Например, Barisani-Asenbauer et al. [41] сообщили, что системный альбендазол (800 мг два раза в день для взрослых и 400 мг два раза в день для детей) в сочетании со стероидом приводил к улучшению зрения без рецидивов увеита у 5 пациентов в течение 13,8-месячного периода наблюдения. В нашем исследовании комбинированная терапия кортикостероидами и альбендазолом значительно снизила 6-месячные рецидивы (17,4%) по сравнению с группой, принимавшей только кортикостероиды (54,5%), хотя терапевтическое улучшение воспаления и зрения было сходным с терапией альбендазолом и без нее [9] .Считается, что гибель личинки связана с воспалительной реакцией, которая не доказана. Однако монотерапия альбендазолом у пациентов с ОТ с неактивным внутриглазным воспалением не выявила обострения внутриглазного воспаления [9]. В отношении подходящей дозировки системной терапии альбендазолом клиницисты не пришли к единому мнению. Например, 200 мг два раза в день в течение одного месяца и 400 или 800 мг два раза в день в течение 2 недель были рекомендованы для пероральной терапии альбендазолом для пациентов с ОТ, которые никогда не сравнивались в одном исследовании [9, 41] .
Также существует сообщение о том, что подвижная субретинальная личинка уничтожена с помощью фотокоагуляции [46]. В другом сообщении было показано, что интравитреальный ранибизумаб эффективен для лечения хориоидальной неоваскуляризации, вторичной по отношению к ОТ [47].
Медикаментозная терапия системными или местными кортикостероидами эффективна для уменьшения внутриглазного воспаления и улучшения симптомов, связанных с воспалением, но имеет ограниченную эффективность для устранения структурных осложнений сетчатки. Отслоение сетчатки, эпиретинальная мембрана и стойкое помутнение стекловидного тела являются частыми хирургическими показаниями к витреоретинальной хирургии, выполняемой на глазах с помощью ОТ, и несколько авторов сообщили о результатах хирургического лечения.Giuliari et al. [48] сообщили о хороших анатомо-функциональных результатах хирургического лечения у 45 пациентов с ОТ. В нашей серии случаев 32 из 101 пациента (31,7%) потребовалось хирургическое лечение, каждому по поводу эпиретинальной мембраны (n = 19), помутнения стекловидного тела (n = 9) и / или отслоения сетчатки (n = 2). Успешный хирургический результат был достигнут у 68,4%, 88,9% и 50% пациентов с эпиретинальной мембраной, помутнением стекловидного тела и отслоением сетчатки соответственно [9]. Обеспечивая структурную модификацию, т. Е., пилинг мембраны, удаление помутнения стекловидного тела или повторное прикрепление сетчатки, хирургическое вмешательство при ОТ могут привести к стабилизации или улучшению зрительной функции.
ПРОФИЛАКТИКА
В условиях недостаточной осведомленности об ОТ, повышение осведомленности общественности о токсокарозе и снижение воздействия токсокар на человека имеют важное значение для предотвращения этого заболевания. Чтобы снизить риск заражения, в первую очередь следует выяснить источник передачи.
Предыдущие исследования установили, что владение собакой или кошкой является фактором риска заражения токсокарой.Прямой контакт с необработанными инфицированными щенками считается важным источником передачи инфекции. Однако общенациональный опрос, проведенный в Соединенных Штатах, показал, что процент владения домашними животными среди пациентов с ОТ был менее 50% (45% для собак и 26% для кошек), что свидетельствует о том, что контакт с нелеченными инфицированными щенками может недостаточно объяснить источники передачи . Случайное проглатывание яиц с зародышем в результате геофагии также было предложено как еще один важный источник передачи [1, 2, 7].Поскольку заболевание обычно возникает у детей, следует уделять особое внимание соблюдению правил гигиены, например мытье рук, особенно после пребывания в зонах повышенного риска, таких как песочницы, парк под открытым небом и игровые площадки. Действительно, песочницы, парки под открытым небом и детские площадки могут быть сильно загрязнены зародышами яиц токсокары, поскольку люди обычно выгуливают своих питомцев в этих местах [2, 49, 50, 51, 52], а в теплых условиях яйца с зародышами могут оставаться жизнеспособными в течение многих лет. [53]. Кроме того, владельцев домашних животных следует посоветовать незамедлительно избавляться от фекалий, часто убирать жилые помещения домашних животных и отвозить домашних животных к ветеринару для регулярной дегельминтизации [16].
У взрослых пациентов источник передачи может несколько отличаться от источника передачи у детей, поскольку вероятность случайного проглатывания яиц с эмбрионами ниже. Недавно сообщалось о связи между сырым мясом, особенно сырой коровьей печенью, и токсокарозом среди взрослого населения [9, 14]. В некоторых странах Азии сырое мясо потребляют, в основном, взрослые, что может увеличить число взрослых пациентов с токсокарозом [15]. В Корее употребление сырой коровьей печени в анамнезе было обнаружено у 60-90% пациентов с системным токсокарозом и у 80.8% ОТ. Отношение шансов ОТ составляло 14,9 для употребления сырой коровьей печени и 2,28 для употребления сырого мяса [9]. Это указывает на то, что источник заражения токсокарозом и демографические особенности пациентов могут различаться в зависимости от географических и поведенческих (особенно, пищевых) моделей. Практикующий специалист в области общественного здравоохранения должен учитывать местный культурный контекст при выявлении вероятных источников инфекции у пациентов с токсокарозом и обучать людей не есть сырое мясо, чтобы предотвратить заражение токсокарой.
ВЫВОДЫ
Наши нынешние представления о диагностике, лечении и профилактике токсокароза человека и поражения глаз ограничены, хотя это одна из самых распространенных зоонозных инфекций во всем мире. Клинический диагноз ОТ можно диагностировать по определенным признакам. Однако серологический диагноз, который дает доказательства инфекции Toxocara, может в значительной степени подтвердить диагноз у пациентов с предполагаемым ОТ. Таким образом, необходимо дальнейшее улучшение диагностики для лучшего обнаружения и быстрой диагностики ОТ.В частности, в будущих исследованиях следует изучить потенциальные источники инфекции и стандартизировать медикаментозное и хирургическое лечение ОТ, чтобы минимизировать анатомические и функциональные последствия. Просвещение общественности и кампании по предотвращению переваривания сырых продуктов животного происхождения, особенно печени, также могут снизить заболеваемость токсокарозом и ОТ.
Ссылки
1. Rubinsky-Elefant G, Hirata CE, Yamamoto JH, Ferreira MU. Токсокароз человека: диагностика, распространенность серотипов в мире и клинические проявления системных и глазных форм.Ann Trop Med Parasitol. 2010; 104: 3–23. [PubMed] [Google Scholar] 2. Деспомье Д. Токсокароз: клинические аспекты, эпидемиология, медицинская экология и молекулярные аспекты. Clin Microbiol Rev.2003; 16: 265–272. [Бесплатная статья PMC] [PubMed] [Google Scholar] 3. Стенсволд ЧР, Сков Дж., Моллер Л.Н., Йенсен П.М., Капель С.М., Петерсен Э., Нильсен Х.В. Распространенность токсокароза человека в Дании. Clin Vaccine Immunol. 2009. 16: 1372–1373. [Бесплатная статья PMC] [PubMed] [Google Scholar] 4. Fan CK, Hung CC, Du WY, Liao CW, Su KE.Сероэпидемиология инфекции Toxocara canis среди школьников горных аборигенов, проживающих в загрязненных районах на востоке Тайваня. Trop Med Int Health. 2004; 9: 1312–1318. [PubMed] [Google Scholar] 5. Бивер П.К., Снайдер С.Х., Каррера Г.М., Дент Дж. Х., Лафферти Дж. У. Хроническая эозинофилия, вызванная мигрирующей висцеральной личинкой; отчет о трех случаях. Педиатрия. 1952; 9: 7–19. [PubMed] [Google Scholar] 6. Николс Р.Л. Этиология висцеральной мигрирующей личинки. I. Диагностическая морфология инфекционных личинок токсокар второй стадии.J Parasitol. 1956; 42 (4 секция 1): 349–362. [PubMed] [Google Scholar] 7. Смит Х., Холланд С., Тейлор М., Магнавал Дж. Ф., Шанц П., Майзельс Р. Насколько распространен токсокароз у человека? К стандартизации наших знаний. Trends Parasitol. 2009. 25: 182–188. [PubMed] [Google Scholar] 8. Biglan AW, Glickman LT, Lobes LA., Jr. Сыворотка и антитело к токсокарам стекловидного тела при эндофтальмите нематод. Am J Ophthalmol. 1979; 88: 898–901. [PubMed] [Google Scholar] 9. Ан SJ, Woo SJ, Jin Y, Chang YS, Kim TW, Ahn J, Heo JW, Yu HG, Chung H, Park KH, Hong ST.Клиника и течение глазного токсокароза у взрослых. PLoS Negl Trop Dis. 2014; 8: e2938. [Бесплатная статья PMC] [PubMed] [Google Scholar] 10. Стюарт JM, Cubillan LD, Cunningham ET., Jr. Распространенность, клинические особенности и причины потери зрения среди пациентов с глазным токсокарозом. Сетчатка. 2005. 25: 1005–1013. [PubMed] [Google Scholar] 11. Maetz HM, Kleinstein RN, Federico D, Wayne J. Оценка распространенности глазного токсоплазмоза и токсокароза в Алабаме. J Infect Dis. 1987; 156: 414. [PubMed] [Google Scholar] 12.Good B, Holland CV, Taylor MR, Larragy J, Moriarty P, O’Regan M. Глазной токсокароз у школьников. Clin Infect Dis. 2004. 39: 173–178. [PubMed] [Google Scholar] 13. Гото Х., Мочизуки М., Ямаки К., Котаке С., Усуи М., Оно С. Эпидемиологическое исследование внутриглазного воспаления в Японии. Jpn J Ophthalmol. 2007; 51: 41–44. [PubMed] [Google Scholar] 14. Choi D, Lim JH, Choi DC, Paik SW, Kim SH, Huh S. Токсокароз и употребление сырой коровьей печени у пациентов с эозинофилией. Корейский J Parasitol. 2008. 46: 139–143.[Бесплатная статья PMC] [PubMed] [Google Scholar] 16. Вудхолл Д., Старр М.С., Монтгомери С.П., Джонс Дж.Л., Лам Ф., Рид Р.У., Мурти Р.С. Глазной токсокароз: эпидемиологические, анатомические и терапевтические варианты на основе опроса узких офтальмологов. Офтальмология. 2012; 119: 1211–1217. [PubMed] [Google Scholar] 18. Йокои К., Гото Х., Сакаи Дж., Усуи М. Клинические особенности глазного токсокароза в Японии. Ocul Immunol Inflamm. 2003; 11: 269–275. [PubMed] [Google Scholar] 19. Мирда Б.Р., Хокар СК. Глазной токсокароз у населения Северной Индии.J Trop Pediatr. 2002. 48: 328–330. [PubMed] [Google Scholar] 20. Park SP, Park I, Park HY, Lee SU, Huh S, Magnaval JF. Пять случаев глазного токсокароза подтверждены серологическими исследованиями. Корейский J Parasitol. 2000. 38: 267–273. [Бесплатная статья PMC] [PubMed] [Google Scholar] 21. Гиллеспи Ш., Диннинг У. Дж., Фоллер А., Кроукрофт Н. С.. Спектр глазного токсокароза. Глаз (Лондон) 1993; 7 (Pt 3): 415–418. [PubMed] [Google Scholar] 22. Ёсида М., Сирао Й, Асаи Х, Нагасе Х, Накамура Х, Окадзава Т., Кондо К., Такаянаги Т.Х., Фудзита К., Акао Н.Ретроспективное исследование глазного токсокароза в Японии: корреляция с распространенностью антител и офтальмологическими данными пациентов с увеитом. J Helminthol. 1999. 73: 357–361. [PubMed] [Google Scholar] 23. Ван В.Л., Кано М.Р., Пинс К.Дж., Грин Р.Л. Эхографические характеристики глазного токсокароза. Офтальмология. 1991; 98: 28–32. [PubMed] [Google Scholar] 24. Уилкинсон С.П., Уэлч РБ. Внутриглазные токсокары. Am J Ophthalmol. 1971; 71: 921–930. [PubMed] [Google Scholar] 25. Ан SJ, Woo SJ, Hyon JY, Park KH. Образование катаракты, связанное с токсокарозом глаз.J Cataract Refract Surg. 2013; 39: 830–835. [PubMed] [Google Scholar] 26. Сиваратнам Д., Субрайан В., Али Н.А. Трансвитреальная миграция личинки Toxocara, приводящая ко второй хориоретинальной гранулеме. Jpn J Ophthalmol. 2008. 52: 416–417. [PubMed] [Google Scholar] 27. Судзуки Т., Джоко Т., Акао Н., Охаши Ю. После миграции личинки токсокары в сетчатке с помощью оптической когерентной томографии и флуоресцентной ангиографии. Jpn J Ophthalmol. 2005. 49: 159–161. [PubMed] [Google Scholar] 28. Жакье П., Готштейн Б., Стингелин И., Эккерт Дж.Иммунодиагностика токсокароза у людей: оценка нового набора для иммуноферментного анализа. J Clin Microbiol. 1991; 29: 1831–1835. [Бесплатная статья PMC] [PubMed] [Google Scholar] 29. Шанц PM. Личинка токсокары мигрирует сейчас. Am J Trop Med Hyg. 1989; 41 (3 доп.): 21–34. [PubMed] [Google Scholar] 30. Хаглер WS, Поллард ZF, Джарретт WH, Доннелли Э. Результаты операции по поводу окулярного Toxocara canis. Офтальмология. 1981; 88: 1081–1086. [PubMed] [Google Scholar] 31. Джин И, Шен С., Хэ С, Сон В.М., Чой М.Х., Хонг СТ.Серодиагностика токсокароза методом ИФА с использованием неочищенного антигена личинок Toxocara canis. Корейский J Parasitol. 2013; 51: 433–439. [Бесплатная статья PMC] [PubMed] [Google Scholar] 32. Лукас А., Муллин Н.П., Теттех К.К., Моенс Л., Майзелс Р.М. Новый лектин С-типа, секретируемый паразитической нематодой, обитающей в тканях. Curr Biol. 1999; 9: 825–828. [PubMed] [Google Scholar] 33. Шарки Дж. А., Маккей П. С.. Глазной токсокароз у пациента с неоднократно отрицательным титром по ИФА на Toxocara canis. Br J Ophthalmol. 1993; 77: 253–254. [Бесплатная статья PMC] [PubMed] [Google Scholar] 34.Элефант Г.Р., Симидзу С.Х., Санчес М.С., Джейкоб С.М., Феррейра А.В. Серологическое наблюдение за больными токсокарозом после химиотерапии, основанное на обнаружении антител IgG, IgA и IgE с помощью иммуноферментного анализа. Анал J Clin Lab. 2006. 20: 164–172. [Бесплатная статья PMC] [PubMed] [Google Scholar] 35. Со М, Юн СК. Сероэпидемиологическое исследование токсокароза среди пациентов с эозинофилией в Чхунчхон-Намдо. Корейский J Parasitol. 2012; 50: 249–251. [Бесплатная статья PMC] [PubMed] [Google Scholar] 36. Kim YH, Huh S, Chung YB.Распространенность токсокароза среди здоровых людей с эозинофилией. Корейский J Parasitol. 2008; 46: 29–32. [Бесплатная статья PMC] [PubMed] [Google Scholar] 37. Квон Н.Х., О MJ, Ли SP, Ли Би Джей, Чхве, округ Колумбия. Распространенность и диагностическая ценность токсокароза при неизвестной эозинофилии. Ann Hematol. 2006. 85: 233–238. [PubMed] [Google Scholar] 38. Ариас Иригойен J, сенатор Санчес CJ. Токсокароз: причина гипер-IgE и эозинофилии. J Исследование Allergol Clin Immunol. 1995; 5: 232–234. [PubMed] [Google Scholar] 39. Shields JA.Глазной токсокароз. Обзор. Surv Ophthalmol. 1984; 28: 361–381. [PubMed] [Google Scholar] 40. Магуайр AM, Грин WR, Michels RG, Erozan YS. Восстановление внутриглазного Toxocara canis путем витрэктомии pars plana. Офтальмология. 1990; 97: 675–680. [PubMed] [Google Scholar] 41. Барисани-Асенбауэр Т., Мака С.М., Хауфф В., Камински С.Л., Домановиц Х., Хеер И., Ауэр Х. Лечение глазного токсокароза альбендазолом. J Ocul Pharmacol Ther. 2001; 17: 287–294. [PubMed] [Google Scholar] 42. Bird AC, Smith JL, Curtin VT. Нематодный неврит зрительного нерва.Am J Ophthalmol. 1970; 69: 72–77. [PubMed] [Google Scholar] 43. Stürchler D, Schubarth P, Gualzata M, Gottstein B, Oettli A. Тиабендазол против альбендазола в лечении токсокароза: клиническое испытание. Ann Trop Med Parasitol. 1989. 83: 473–478. [PubMed] [Google Scholar] 44. Magnaval JF. Сравнительная эффективность диэтилкарбамазина и мебендазола для лечения токсокароза человека. Паразитология. 1995. 110 (Pt 5): 529–533. [PubMed] [Google Scholar] 45. Абдель-Хамид А.А. Влияние тиабендазола на миграцию личинок Toxocara canis у мышей.J Parasitol. 1984; 70: 226–231. [PubMed] [Google Scholar] 46. Zygulska-Machowa H, Ziobrowski S. Случай глазного токсокароза, леченный ксеноновой фотокоагуляцией. Klin Oczna. 1987. 89: 213–214. [PubMed] [Google Scholar] 47. Lyall DA, Hutchison BM, Gaskell A, Varikkara M. Интравитреальный ранибизумаб в лечении хориоидальной неоваскуляризации, вторичной по отношению к глазному токсокарозу, у 13-летнего мальчика. Глаз (Лондон) 2010; 24: 1730–1731. [PubMed] [Google Scholar] 48. Джулиари ГП, Рамирес Г, Кортез РТ. Хирургическое лечение токсокароза глаз: анатомо-функциональные результаты у 45 пациентов.Eur J Ophthalmol. 2011; 21: 490–494. [PubMed] [Google Scholar] 49. Queiroz ML, Simonsen M, Paschoalotti MA, Chieffi PP. Частота заражения почвы яйцами Toxocara canis в южном регионе муниципалитета Сан-Паулу (SP, Бразилия) за 18-месячный период. Rev Inst Med Trop Сан-Паулу. 2006. 48: 317–319. [PubMed] [Google Scholar] 50. Кастильо Д., Паредес С., Занарту С., Кастильо Дж., Меркадо Р., Муньос В., Шеноне Х. Загрязнение окружающей среды Toxocara sp. яйца на площадях и в парках Сантьяго, Чили, 1999.Bol Chil Parasitol. 2000; 55: 86–91. [PubMed] [Google Scholar] 51. Джакометти А., Кириони О, Фортуна М., Осимани П., Антоничелли Л., Дель Прете М.С., Рива А., Д’Эррико М.М., Петрелли Э., Скализ Г. Экологические и серологические доказательства наличия токсокароза в городской зоне Анконы, Италия . Eur J Epidemiol. 2000. 16: 1023–1026. [PubMed] [Google Scholar] 52. Akdemir C. Висцеральная личинка мигрирует среди детей в Кютахья (Турция) и оценка игровых площадок для яиц T. canis. Turk J Pediatr. 2010. 52: 158–162.[PubMed] [Google Scholar]Токсокароз: скрытая угроза с прогрессирующими последствиями для общественного здравоохранения | Инфекционные болезни бедности
Деспомье Д. Токсокароз: клинические аспекты, эпидемиология, медицинская экология и молекулярные аспекты. Clin Microbiol Rev.2003; 16: 265–72.
PubMed PubMed Central Статья Google Scholar
Overgaauw PA, van Knapen F. Ветеринарные аспекты и аспекты общественного здравоохранения Toxocara spp.Vet Parasitol. 2013; 193: 398–403.
PubMed Статья Google Scholar
Голландия CV. Пробелы в знаниях в эпидемиологии Toxocara : загадка остается. Паразитология. 2017; 144: 81–94.
PubMed Статья CAS Google Scholar
Macpherson CN. Эпидемиология и значение токсокароза для общественного здравоохранения: зооноз мирового значения.Int J Parasitol. 2013; 43: 999–1008.
PubMed Статья Google Scholar
Zibaei M. Глистные инфекции и сердечно-сосудистые заболевания: Toxocara вид вызывает заболевание. Curr Cardiol Rev.2017; 13: 56–62.
PubMed PubMed Central Статья Google Scholar
Strube C, Heuer L, Janecek E. Toxocara spp.инфекции у паратенических хозяев. Vet Parasitol. 2013; 193: 375–89.
PubMed Статья Google Scholar
Fan CK, Holland CV, Loxton K, Barghouth U. Церебральный токсокароз: немое прогрессирование до нейродегенеративных расстройств? Clin Micobiol Rev.2015; 28: 663–86.
Артикул Google Scholar
Fan CK, Liao CW, Cheng YC. Факторы, влияющие на проявление токсокароза у человека: генетика и окружающая среда.Vet Parasitol. 2013; 193: 342–52.
PubMed Статья CAS Google Scholar
Чен Дж., Чжоу Д.Х., Нисбет А.Дж., Сюй М.Дж., Хуанг С.И., Ли М.В., Ван Ч.Р., Чжу XQ. Достижения в области молекулярной идентификации, таксономии, генетической изменчивости и диагностики Toxocara spp. Заразить Genet Evol. 2012; 12: 1344–8.
PubMed Статья Google Scholar
Николетти А.Токсокароз. Handb Clin Neurol. 2013; 114: 217–28.
PubMed Статья Google Scholar
Чен Дж., Сюй М.Дж., Чжоу Д.Х., штаб-квартира Сун, Ван Ч.Р., Чжу XQ. Паразитарные зоонозы собак и кошек в Китае. Векторы паразитов. 2012; 5: 152.
PubMed PubMed Central Статья Google Scholar
Rubinsky-Elefant G, Hirata CE, Yamamoto JH, Ferreira MU. Токсокароз человека: диагностика, распространенность серотипов в мире и клинические проявления системных и глазных форм.Ann Trop Med Parasitol. 2010; 104: 3–23.
PubMed Статья CAS Google Scholar
Hotez PJ, Wilkins PP. Токсокароз: самая распространенная в Америке запущенная инфекция бедности и гельминтоз мирового значения? PLoS Negl Trop Dis. 2009; 3: e400.
PubMed PubMed Central Статья Google Scholar
Fillaux J, Magnaval JF. Лабораторная диагностика токсокароза человека.Vet Parasitol. 2013; 193: 327–36.
PubMed Статья CAS Google Scholar
Морейра GM, TelmoPde L, Mendonça M, Moreira AN, McBride AJ, Scaini CJ, Conceição FR. Токсокароз человека: современные достижения в диагностике, лечении и вмешательстве. Trends Parasitol. 2014; 30: 456–64.
PubMed Статья Google Scholar
Wilder HC. Эндофтальмит нематод.Trans Am Acad Ophthalmol Otolaryngol. 1950; 55: 99–104.
PubMed CAS Google Scholar
Париз М.Э., Хотез П.Дж., Слуцкер Л. Забытые паразитарные инфекции в США: потребности и возможности. Am J Trop Med Hyg. 2014; 90: 783–5.
PubMed PubMed Central Статья Google Scholar
Zhu XQ, Korhonen PK, Cai H, Young ND, Nejsum P, von Samson-Himmelstjerna G, et al.Генетический план зоонозного патогена Toxocara canis . Nat Commun. 2015; 6: 6145.
PubMed PubMed Central Статья CAS Google Scholar
Гассер РБ, Корхонен П.К., Чжу XQ, Янг Н.Д. Использование генома Toxocara для поддержки исследований токсокароза и новых вмешательств. Adv Parasitol. 2016; 91: 87–110.
PubMed Статья Google Scholar
Ли МВт, Линь Р.К., Штаб-квартира Сун, Ву XY, Чжу XQ. Полные митохондриальные геномы трех видов Toxocara , имеющих значение для здоровья человека и животных. BMC Genomics. 2008; 9: 224.
PubMed PubMed Central Статья CAS Google Scholar
Гассер РБ. Идеальное время для использования передовых молекулярных технологий для изучения фундаментальной биологии видов Toxocara . Vet Parasitol. 2013; 193: 353–64.
PubMed Статья Google Scholar
Mizgajska-Wiktor H, Jarosz W. Сравнение загрязнения почвы яйцами Toxocara cani s и Toxocara cati в сельских и городских районах Великопольского района в 2000-2005 гг. Wiad Parazytol. 2007. 53: 219–25. (на польском языке)
PubMed Google Scholar
Гавор Дж., Борецка А. Загрязнение окружающей среды яйцами Toxocara в Мазовецком воеводстве как риск токсокароза у детей.Wiad Parazytol. 2004; 50: 237–41.
PubMed Google Scholar
Борецка А., Гавор Дж., Недворок М., Сордил Б. Встречаемость Toxocara spp. яйца в бытовой среде детей с диагностированным токсокарозом в Лодзинском воеводстве. Wiad Parazytol. 2010; 56: 141–4.
PubMed Google Scholar
Викрамасингхе С., Ятавара Л., Раджапаксе Р.П., Агацума Т. Toxocara canis и Toxocara vitulorum : молекулярная характеристика, дискриминация и филогенетический анализ на основе митохондриальных (субъединица АТФ-синтазы 6 и 12S) и ядерных рибосомных (ITS-2 и 28S) генов. Parasitol Res. 2009; 104: 1425–30.
PubMed Статья Google Scholar
Wickramasinghe S, Yatawara L, Rajapakse RP, Agatsuma T. Toxocara vitulorum (Ascaridida: Nematoda): содержание, расположение и состав митохондриальных генов по сравнению с другими видами Toxocara .Мол Биохим Паразитол. 2009; 166: 89–92.
PubMed Статья CAS Google Scholar
Le TH, Anh NT, Nguyen KT, Nguyen NT, do TT T, Gasser RB. Toxocara malaysiensis Инфекция домашних кошек во Вьетнаме — новая зоонозная проблема? Заразить Genet Evol. 2016; 37: 94–8.
PubMed Статья Google Scholar
Zhu XQ, Jacobs DE, Chilton NB, Sani RA, Cheng NABY, Gasser RB.Молекулярная характеристика варианта Toxocara от кошек в Куала-Лумпуре, Малайзия. Паразитология. 1998. 117: 155–64.
PubMed Статья CAS Google Scholar
Гиббонс Л.М., Джейкобс Д.Е., Сани РА. Toxocara malaysiensis n. Sp. (Nematoda: Ascaridoidea) от домашней кошки ( Feliscatus Linnaeus , 1758). J Parasitol. 2001; 87: 660–5.
PubMed Статья CAS Google Scholar
Fogt-Wyrwas R, Mizgajska-Wiktor H, Pacoń J, Jarosz W. Внутривидовые вариации между последовательностями ITS Toxocara canis , Toxocara cati и Toxascaris leonine от разных видов хозяев в Юго-Западной Польше. J Helminthol. 2013; 87: 432–42.
PubMed Статья CAS Google Scholar
Zhu XQ, Gasser RB, Jacobs DE, Hung GC, Chilton NB. Взаимоотношения между некоторыми аскаридоидными нематодами на основе данных о последовательности рибосомной ДНК.Parasitol Res. 2000; 86: 738–44.
PubMed Статья CAS Google Scholar
Li MW, Lin RQ, Song HQ, Sani RA, Wu XY, Zhu XQ. Электрофоретический анализ изменчивости последовательностей в трех участках митохондриальной ДНК для аскаридоидных паразитов, имеющих значение для здоровья человека и животных. Электрофорез. 2008; 29: 2912–7.
PubMed CAS Google Scholar
Smith H, Holland C, Taylor M, Magnaval JF, Schantz P, Maizels R. Насколько распространен токсокароз у человека? К стандартизации наших знаний. Trends Parasitol. 2009. 25: 182–8.
PubMed Статья Google Scholar
Саид И., Тайра К., Капел СМ. Toxocara canis у экспериментально зараженных серебристых и песцов. Parasitol Res. 2005; 97: 160–6.
PubMed Статья Google Scholar
Гимарайнш AM, Алвес Э.Г., де Резендеде Г.Ф., Родригес MC. Toxocara sp. яйца и Ancylostoma sp. личинки в общественных парках, Бразилия. Rev Saude Publica. 2005; 39: 293–5. (на португальском)
PubMed Статья Google Scholar
Tiyo R, Guedes TA, Falavigna DL, Falavigna-Guilherme AL. Сезонное заражение площадей и газонов паразитами с зоонозным потенциалом в южной части Бразилии. J Helminthol.2008; 82: 1–6.
PubMed Статья CAS Google Scholar
Дада Б.Дж., Линдквист В.Д. Распространенность Toxocara spp. яйца в некоторых общественных местах и в местах отдыха на шоссе в Канзасе. J Helminthol. 1979; 53: 145–6.
PubMed Статья CAS Google Scholar
Chorazy ML, Ричардсон DJ. Исследование загрязнения окружающей среды яйцеклетками аскарид, Уоллингфорд, Коннектикут.Vector Borne Zoonotic Dis. 2005; 5: 33–9.
PubMed Статья Google Scholar
Düwel D. Распространенность яиц Toxocara в песке детских игровых площадок во Франкфурте / М. Ann Trop Med Parasitol. 1984; 78: 633–6.
PubMed Статья Google Scholar
Рокицкий Ю., Кухарска А.П., Дзидо Дж., Карчевска Д. Заражение детских площадок в городе Гданьск яйцами паразитов.Wiad Parazytol. 2007; 53: 227–30. (на польском языке)
PubMed Google Scholar
Emehelu CO, Fakae BB. Распространенность яиц Toxocara canis на детских площадках детских садов в Нсукке, Нигерия. В J Zoonoses. 1986; 13: 158–61.
CAS Google Scholar
Отейфа Н.М., Мустафа М.А. Потенциальный риск заражения токсокарозом в районе Гелиополис, Каир, Египет.J Egypt Soc Parasitol. 1997. 27: 197–203.
PubMed CAS Google Scholar
Гунасилан Л., Ганесан П.И., Рамадасс П., Башир М.А., Рагхаван Н. Распространенность яиц токсокары в окружающей среде. J Indian Vet. 1992; 69: 308–9.
Google Scholar
Симидзу Т. Распространенность яиц токсокары в песочницах в городе Токусима и его окрестностях.J Vet Med Sci. 1993; 55: 807–11.
PubMed Статья CAS Google Scholar
Киган Дж. Д., Голландия CV. Сравнение эмбрионации Toxocara canis в контролируемых условиях в почве и волосах. J Helminthol. 2013; 87: 78–84.
PubMed Статья Google Scholar
Родди Г., Холланд С., Стаффорд П., Вулф А. Загрязнение шерсти лисицы яйцами Toxocara canis .J Helminthol. 2008. 82: 293–6.
PubMed Статья CAS Google Scholar
Родди Г., Стаффорд П., Холланд К.В., Вулф А. Загрязнение шерсти собак яйцами Toxocara canis . Vet Parasitol. 2008; 152: 85–93.
PubMed Статья Google Scholar
Ли А.С., Шанц П.М., Казакос КР, Монтгомери С.П., Боуман Д.Д. Эпидемиологические и зоонозные аспекты аскаридных инфекций у собак и кошек.Trends Parasitol. 2010. 26: 155–61.
PubMed Статья Google Scholar
Дубинский П., Хавасиова-Рейтерова К., Петко Б., Ховорка И., Томасовикова О. Роль мелких млекопитающих в эпидемиологии токсокароза. Паразитология. 1995; 110: 187–93.
PubMed Статья Google Scholar
Антолова Д., Рейтерова К., Митерпакова М., Станко М., Дубинский П.Тираж Toxocara spp. в пригородных и сельских экосистемах Словацкой Республики. Vet Parasitol. 2004; 126: 317–24.
PubMed Статья CAS Google Scholar
Reperant LA, Hegglin D, Tanner I., Fischer C., Deplazes P. Грызуны как общие индикаторы зоонозных паразитов хищников в городской среде. Паразитология. 2009. 136: 329–37.
PubMed Статья CAS Google Scholar
Magnaval JF, Glickman LT, Dorchies P, Morassin B. Основные моменты токсокароза человека. Корейский J Parasitol. 2001; 39: 1–11.
PubMed PubMed Central Статья CAS Google Scholar
Акао Н., Охта Н. Токсокароз в Японии. Parasitol Int. 2007; 56: 87–93.
PubMed Статья Google Scholar
Йошикава М., Нисиофуку М., Мория К., Одзи Ю., Исидзака С., Касахара К. и др.Семейный случай висцерального токсокароза, вызванного употреблением сырой бычьей печени. Parasitol Int. 2008; 57: 525–9.
PubMed Статья Google Scholar
Stoicescu RM, Mihai CM, Giannakopoulou AD. Выраженная гиперэозинофилия у малыша: отчет о болезни. J Med Life. 2011; 4: 105–8.
PubMed PubMed Central CAS Google Scholar
Musso C, Castelo JS, Tsanaclis AM, Pereira FE.Распространенность гранулем печени, индуцированных Toxocara , выявленных с помощью иммуногистохимии, в серии аутопсий в Детской клинической больнице в Витории, ES, Бразилия. Арка Вирхова. 2007; 450: 411–47.
PubMed Статья Google Scholar
Хартлеб М., Янушевский К. Тяжелое поражение печени при мигрирующих висцеральных личинках. Eur J Gastroenterol Hepatol. 2001; 13: 1245–9.
PubMed Статья CAS Google Scholar
Kuenzli E, Neumayr A, Chaney M, Blum J. Сердечные заболевания, связанные с токсокарозом — систематический обзор литературы. Acta Trop. 2016; 154: 107–20.
PubMed Статья Google Scholar
Kayes SG, Oaks JA. Развитие гранулематозного ответа при токсокарозе мышей. Начальные события Am J Pathol. 1978; 93: 277–94.
PubMed CAS Google Scholar
Дромер С, Константин А, Амар Дж., Колье М., Билли Т., Шамонтин Б. и др. Ревматологические аспекты токсокароза (висцеральная мигрирующая личинка), по поводу 2 случаев. Преподобный Рум Эд Фр. 1993; 60: 621–4.
PubMed CAS Google Scholar
Шетти А.К., Авилес Д.Х. Нефротический синдром, связанный с инфекцией Toxocara canis . Ann Trop Paediatr. 1999; 19: 297–300.
PubMed Статья CAS Google Scholar
Prunier F, Delepine S, Victor J, de Gentile L, Moreau C, Laporte J, et al. Фибробластический эндокардит Лоффлера. Отчет о случае, осложнившем токсокароз. Arch Mal Coeur Vaiss. 2001; 94: 226–30. (на французском языке)
PubMed CAS Google Scholar
Исмаил М.А., Халафаллах О. Toxocara canis и хроническая крапивница у пациентов из Египта. J Egypt Soc Parasitol. 2005; 35: 833–40.
PubMed Google Scholar
Стюарт JM, Cubillan LD, Cunningham ET Jr. Распространенность, клинические особенности и причины потери зрения среди пациентов с глазным токсокарозом. Сетчатка. 2005. 25: 1005–13.
PubMed Статья Google Scholar
Центры по контролю и профилактике заболеваний. Глазной токсокароз — США, 2009–2010 гг. MMWR Morb Mortal Wkly Rep. 2011; 60: 734–6.
Google Scholar
Quinnell RJ. Генетика предрасположенности к гельминтозной инфекции. Int J Parasitol. 2003. 33: 1219–31.
PubMed Статья CAS Google Scholar
Norhaida A, Suharni M, Liza Sharmini AT, Tuda J, Rahmah N. rTES-30USM: клонирование с помощью сборочной ПЦР, экспрессия и оценка полезности при обнаружении токсокароза S228. Ann Trop Med Parasitol. 2008; 102: 151–60.
PubMed Статья CAS Google Scholar
Xinou E, Lefkopoulos A, Gelagoti M, Drevelegas A, Diakou A, Milonas I, Dimitriadis AS. Результаты КТ и МРТ при церебральной токсокаральной болезни. AJNR Am J Neuroradiol. 2003; 24: 714–8.
PubMed CAS Google Scholar
Watthanakulpanich D, Smith HV, Hobbs G, Whalley AJ, Billington D. Применение экскреторно-секреторных антигенов Toxocara canis и антител подкласса IgG (IgG1-4) в серодиагностических анализах токсокароза человека.Acta Trop. 2008; 106: 90–5.
PubMed Статья CAS Google Scholar
Нордин Р., Смит Х.В., Мохамад С., Майзелс Р.М., Фонг М.И. Сравнение IgG-ELISA и IgG4-ELISA для серодиагностики Toxocara . Acta Trop. 2005; 93: 57–62.
PubMed Статья CAS Google Scholar
Jin Y, Shen C, Huh S, Sohn WM, Choi MH, Hong ST. Серодиагностика токсокароза методом ELISA с использованием неочищенного антигена личинок Toxocara canis .Корейский J Parasitol. 2013; 51: 433–9.
PubMed PubMed Central Статья Google Scholar
Jacobs DE, Zhu XQ, Gasser RB, Chilton NB. Методы на основе ПЦР для идентификации потенциально зоонозных аскаридоидных паразитов собак, лисиц и кошек. Acta Trop. 1997; 68: 191–200.
PubMed Статья CAS Google Scholar
Li MW, Lin RQ, Chen HH, Sani RA, Song H, Zhu XQ.Инструменты ПЦР для проверки идентичности аскаридных нематод собак и кошек. Зонды Mol Cell. 2007; 21: 349–54.
PubMed Статья CAS Google Scholar
Рай С.К., Уга С., Ву З., Такахаши Ю., Мацумура Т. Использование полимеразной цепной реакции в диагностике токсокароза: экспериментальное исследование. Юго-Восточная Азия J Trop Med Public Health. 1997; 28: 541–4.
PubMed CAS Google Scholar
Van De N, Trung NV, le Duyet V, Chai JY. Молекулярная диагностика больного глазным токсокарозом во Вьетнаме. Корейский J Parasitol. 2013; 51: 563–7.
PubMed PubMed Central Статья Google Scholar
Lim SJ, Lee SE, Kim SH, Hong SH, You YS, Kwon OW, et al. Распространенность Toxoplasma gondii и Toxocara canis среди пациентов с увеитом. Ocul Immunol Inflamm. 2014; 22: 360–6.
PubMed Статья CAS Google Scholar
Macuhova K, Kumagai T., Akao N, Ohta N. Петлевой изотермический анализ амплификации для обнаружения и различения яиц Toxocara canis и Toxocara cati непосредственно из образцов песка. J Parasitol. 2010; 96: 1224–7.
PubMed Статья CAS Google Scholar
Tomita N, Mori Y, Kanda H, Notomi T. Петлевая изотермическая амплификация (LAMP) генных последовательностей и простое визуальное обнаружение продуктов.Nat Protoc. 2008; 3: 877–82.
PubMed Статья CAS Google Scholar
Аревало Дж. Ф., СП Эспиноза, Ф. Аревало. Глазной токсокароз. J Pediatr Ophthalmol Strabismus. 2012; 50: 76–86.
PubMed Статья Google Scholar
Campbell JP, Wilkinson CP. Визуализация в диагностике и лечении глазного токсокароза. Int Ophthalmol Clin. 2012; 52: 145–53.
PubMed Статья Google Scholar
Morais FB, MacielAL ATE, Muccioli C, Al-lemann N. Результаты ультразвукового исследования при глазном токсокарозе. Arq Bras Ophthalmol. 2012; 75: 43–7.
Артикул Google Scholar
Hashida N, Nakai K, Nishida K. Диагностическая оценка глазного токсокароза с использованием оптической когерентной томографии с высоким проникновением. Case Rep Ophthalmol.2014; 5: 16–21.
PubMed PubMed Central Статья Google Scholar
Ахмед А.С., Бисвас Дж. Увейтис: поиск причины. Тайвань J Ophthalmol. 2013; 3: 134–40.
Артикул Google Scholar
Ким Й.Дж., Мун СН, Чанг Дж.Х. Токсокароз диска зрительного нерва. J Neuroophthalmol. 2013; 33: 151–2.
PubMed Статья Google Scholar
Tran VT, Lumbroso L, LeHoang P, Herbort CP. Ультразвуковая биомикроскопия при периферическом ретиновитреальном токсокарозе. Am J Ophthal. 1999; 127: 607–9.
PubMed Статья CAS Google Scholar
Родман Дж., Пиццименти Дж. Диагностическая визуализация глазного токсокароза in vivo. Clin Exp Optom. 2009. 92: 146–14.
PubMed Статья Google Scholar
Чен Кью, Гу Дж, Цзян Р., Чжоу М., Чанг К.Роль ультразвуковой биомикроскопии в диагностике токсокароза глаз. Br J Ophthalmol. 2018 Май; 102 (5): 642–6.
PubMed Статья Google Scholar
Sánchez SS, García HH, Nicoletti A. Результаты клинической и магнитно-резонансной томографии нейротоксокароза. Фронт Neurol. 2018; 9: 53.
PubMed PubMed Central Статья Google Scholar
Рохилла С., Джайн Н., Ядав Р., Дхаулаканди ДБ.Мигрирующая висцеральная личинка печени. BMJ Case Rep.2013; 13: 2013.
Google Scholar
Раджеш С., Патидар Ю., Растоги А., Бихари С. Изображение месяца: мигрирующая висцеральная личинка печени. Am J Gastroenterol. 2015; 110: 497.
PubMed Статья CAS Google Scholar
Ким Ю.К., Ким С.С., Мун В.С., Чо БХ, Ли Си, Ли Дж. Результаты МРТ очаговых эозинофильных заболеваний печени.AJR Am J Roentgenol. 2005; 184: 1541–8.
PubMed Статья Google Scholar
Magnaval JF, Charlet JP. Сравнительная эффективность тиабендазола и мебендазола при лечении токсокароза. Терапия. 1987. 42: 541–4. (на французском языке)
PubMed CAS Google Scholar
Stürchler D, Schubarth P, Gualzata M, Gottstein B, Oettli A. Тиабендазол против альбендазола в лечении токсокароза: клиническое испытание.Ann Trop Med Parasitol. 1989; 83: 473–8.
PubMed Статья Google Scholar
Павловски З. Токсокароз у человека: клиническое проявление и дилемма лечения. J Helminthol. 2001; 75: 299–305.
PubMed Статья CAS Google Scholar
Woodhall DM, Fiore AE. Токсокароз: обзор для педиатров. J Pediatric Infect Dis Soc. 2014; 3: 154–9.
PubMed Статья Google Scholar
Ranasuriya G, Mian A, Boujaoude Z, Tsigrelis C. Легочный токсокароз: клинический случай и обзор литературы. Инфекционное заболевание. 2014; 42: 575–8.
PubMed Статья CAS Google Scholar
Хрючкова Г. Новые подходы к иммунопрофилактике при токсокарозе. В: Holland CV, Smith HV, редакторы. Toxocara : загадочный паразит.Оксфордшир: CAB International; 2006. с. 174–94.
Google Scholar
Martínez-Pulgarín DF, Muñoz-Urbano M, Gomez-Suta LD, Delgado OM, Rodriguez-Morales AJ. Глазной токсокароз: новые диагностические и терапевтические перспективы. Последние публикации Pat Antiinfect Drug Discov. 2015; 10: 35–41.
PubMed Статья Google Scholar
Фрейзер М., Андерсон М.Л., Софоклеус С.Лечение токсокароза глаз альбендезолом: описание случая. Оптометрия. 2009. 80: 175–80.
PubMed Статья Google Scholar
Satou T, Horiuchi A, Akao N, Koike K, Fujita K, Nikaido T. Toxocara canis : поиск потенциального лекарства среди алкалоидов бета-карболина — исследования in vitro и на мышах. Exp Parasitol. 2005; 110: 134–9.
PubMed Статья CAS Google Scholar
Осман А.А. Лечебная битва с личиночным токсокарозом: мы все еще далеко позади? Acta Trop. 2012; 124: 171–8.
PubMed Статья Google Scholar
Wiśniewska-Ligier M, Woniakowska-Gęsicka T, Sobolewska-Dryjańska J, Markiewicz-Jówiak A, Wieczorek M. Анализ течения и лечения токсокароза у детей: многолетнее наблюдение. Parasitol Res. 2012; 110: 2363–71.
PubMed Статья Google Scholar
Вудхолл Д., Старр М.К., Монтгомери С.П., Джонс Дж.Л., Лум Ф., Рид Р.В. и др. Глазной токсокароз: эпидемиологические, анатомические и терапевтические варианты на основе опроса узких офтальмологов. Офтальмология. 2012; 119: 1211–7.
PubMed Статья Google Scholar
Choi KD, Choi JH, Choi SY, Jung JH. Токсокарная оптическая нейропатия: клинические особенности и офтальмологические данные. Int J Ophthalmol. 2018; 11: 520–3.
PubMed PubMed Central Google Scholar
Эберхардт О., Биалек Р., Нагеле Т., Дичганс Дж. Эозинофильный менингомиелит при токсокарозе: клинический случай и обзор литературы. Clin Neurol Neurosurg. 2005; 107: 432–8.
PubMed Статья CAS Google Scholar
Graeff-Teixeira C, da Silva AC, Yoshimura K. Обновленная информация об эозинофильном менингоэнцефалите и его клинической значимости. Clin Microbiol Rev.2009; 22: 322–48.
PubMed PubMed Central Статья CAS Google Scholar
Goffette S, Jeanjean AP, Duprez TP, Bigaignon G, Sindic CJ. Эозинофильный плеоцитоз и миелит, связанные с инфекцией Toxocara canis . Eur J Neurol. 2000. 7: 703–6.
PubMed Статья CAS Google Scholar
Хомбу А., Йошида А., Кикучи Т., Нагаясу Е., Куроки М., Маруяма Х. Лечение синдрома мигрирующей личинки с помощью длительного приема альбендазола. J Microbiol Immunol Infect. 2017; S1684-1182 (17): 30142–1.
Google Scholar
Deplazes P, van Knapen F, Schweiger A, Overgaauw PA. Роль домашних собак и кошек в передаче гельминтозов зоонозов в Европе с особым вниманием к эхинококкозу и токсокарозу. Vet Parasitol. 2011; 24: 41–53.
Артикул Google Scholar
Parsons JC. Аскаридные инфекции кошек и собак. Ветеринарная клиника North Am Small Anim Pract.1987; 17: 1303–7.
Артикул Google Scholar
ВОЗ. Действия по снижению опасности для здоровья человека, исходящей от животных. ВОЗ Хрон. 1978; 32: 307–10.
Google Scholar
Мальейро А., Анибал Ф. Ф., Мартинс-Филью О. А., Тейшейра-Карвалью А., Перини А., Мартинс М. А., Медейруш А. И., Турато В. М., Асенсио М. П., Брандао ИТ, Номизо А., Силва С. Л., Фаччиоли Л. Х. Вакцинация pcDNA-IL-12 блокирует эозинофильное воспаление, но не гиперчувствительность дыхательных путей после инфицирования мыши Toxocara canis .Вакцина. 2008; 26: 305–15.
PubMed Статья CAS Google Scholar
Basualdo J, Sparo M, Chiodo P, Ciarmela M, Minvielle M. Пероральное введение потенциального пробиотика ( Enterococcus faecalis CECT 7121), по-видимому, снижает количество паразитов у мышей, инфицированных Toxocara canis . Ann Trop Med Parasitol. 2007. 101: 559–62.
PubMed Статья CAS Google Scholar
Chiodo PG, Sparo MD, Pezzani BC, Minvielle MC, Basualdo JA. In vitro и in vivo эффекты Enterococcus faecalis CECT7121 на Toxocara canis . Mem Inst Oswaldo Cruz. 2010; 105: 615–20.
PubMed Статья CAS Google Scholar
де Авила Л.Ф., Консейсао, Франция, Telmo Pde L, Dutra GF, de los Santos DG, Martins LH, Berne ME, da Silva PE, Scaini CJ. Saccharomyces boulardii снижает интенсивность заражения мышей токсокарозом.Vet Parasitol. 2012; 187: 337–40.
PubMed Статья Google Scholar
Kudtarkar A, Shinde UP, Bharkad G, Singh K. Твердые липидные наночастицы альбендазола для лечения инфекции Toxocara canis : исследования эффективности in vivo. Nanosci Nanotechnol-Asia. 2017; 7: 80–91.
CAS Google Scholar
Wilkinson CP, Welch RB. Внутриглазный Toxocara .Am J Ophthalmol. 1971; 71: 921–30.
PubMed Статья CAS Google Scholar
Йокои К., Гото Х., Сакаи Дж., Усуи М. Клинические особенности глазного токсокароза в Японии. Ocul Immunol Inflamm. 2003. 11: 269–75.
PubMed Статья Google Scholar
до Лаго А., Андраде Р., Муччиоли С., Белфорт Р. мл. Оптическая когерентная томография предполагаемой субретинальной гранулемы Toxocara : клинический случай.Arq Bras Oftalmol. 2006; 69: 403–5.
PubMed Статья Google Scholar
Gass JD, Gilbert WR, Guerry RK, Scelfo R. Диффузный односторонний подострый нейроретинит. Офтальмология. 1978; 85: 521–45.
PubMed Статья CAS Google Scholar
de Souza EC, Nakashima Y. Диффузный односторонний подострый нейроретинит. Отчет о трансвитреальном хирургическом удалении субретинальной нематоды.Офтальмология. 1995; 102: 1183–6.
PubMed Статья CAS Google Scholar
Коричневый DH. Глазной Toxocara canis . I Экспериментальная иммунология. Энн Офтальмол. 1971; 3: 907–10.
PubMed CAS Google Scholar
Гиллеспи С.Х., Диннинг В.Дж., Воллер А., Кроукрофт Н.С. Спектр глазного токсокароза. Глаз (Лонд). 1993; 7: 415–8.
Артикул Google Scholar
Ан SJ, Ryoo NK, Woo SJ. Глазной токсокароз: клиника, диагностика, лечение и профилактика. Asia Pac Allergy. 2014; 4: 134–41.
PubMed PubMed Central Статья Google Scholar
Ahn SJ, Woo SJ, Jin Y, Chang YS, Kim TW, Ahn J, et al. Клиника и течение глазного токсокароза у взрослых.PLoS Negl Trop Dis. 2014; 8: e2938.
PubMed PubMed Central Статья CAS Google Scholar
Glickman LT, Magnaval JF, Domanski LM, Shofer FS, Lauria SS, Gottstein B, et al. Висцеральная мигрирующая личинка у взрослых французов: синдром новой болезни? Am J Epidemiol. 1987; 125: 1019–34.
PubMed Статья CAS Google Scholar
Финстерер Дж., Ауэр Х.Нейротоксокароз. Rev Inst Med Trop Сан-Паулу. 2007. 49: 279–87.
PubMed Статья Google Scholar
Richartz E, Buchkremer G. Церебральный токсокароз: редкая причина когнитивных нарушений. Вклад в дифференциальную диагностику деменции. Nervenarzt. 2002. 73: 458–62. (на немецком языке)
PubMed Статья CAS Google Scholar
Bachli H, Minet JC, Gratzl O.Церебральный токсокароз: возможная причина эпилептических припадков у детей. Чайлдс NervSyst. 2004. 20: 468–72.
Google Scholar
Морейра-Силва С.Ф., Родригес М.Г., Пимента Д.Л., Гомеш С.П., Фрейре Л.Х., Перейра ИП. Токсокароз центральной нервной системы: сообщалось о двух случаях. Rev Soc Bras Med Trop. 2004; 37: 169–74.
PubMed Статья Google Scholar
Фортенберри Дж. Д., Кенни Р. Д., Младший Дж. Мигрирующая висцеральная личинка, вызывающая статическую энцефалопатию у младенца. Pediatr Infect Dis J. 1991; 10: 403–6.
PubMed Статья CAS Google Scholar
Caldera F, Burlone ME, Genchi C, Pirisi M, Bartoli E. Toxocara энцефалит с поражением автономной нервной системы. Инфекционное заболевание. 2013; 41: 691–4.
PubMed Статья CAS Google Scholar
Gasser RB, Zhu XQ, Jacobs DE, Hu M, Chilton NB. Молекулярно-генетическая характеристика представителей рода Toxocara — таксономические, популяционно-генетические и эпидемиологические соображения. В: Holland CV, Smith HV, редакторы. Toxocara : загадочный паразит. Соединенное Королевство: Уоллингфорд; 2006. с. 18–31.
Google Scholar
Magnaval JF, Faufingue JH, Morassin B, Fabre R. Катионный белок эозинофилов, специфические IgE и IgG4 при токсокарозе человека.J Helminthol. 2006; 80: 417–23.
PubMed Статья CAS Google Scholar
Магнавал Дж. Ф., Берри А., Фабр Р., Морассин Б. Катионный белок эозинофилов как возможный маркер активной инфекции человека Toxocara . Аллергия. 2001; 56: 1096–9.
PubMed Статья CAS Google Scholar
Mohamad S, Azmi NC, Noordin R. Разработка и оценка чувствительного и специфического теста для диагностики токсокароза человека с использованием трех рекомбинантных антигенов (TES-26, TES-30USM и TES-120).J Clin Microbiol. 2009; 47: 1712–7.
PubMed PubMed Central Статья CAS Google Scholar
Peixoto PL, Nascimento E, Cançado GG, Miranda RR, Rocha RL, Araújo RN, et al. Идентификация антигенов-кандидатов от взрослых стадий Toxocara canis для серодиагностики токсокароза человека. Mem Inst Oswaldo Cruz. 2011; 106: 200–6.
PubMed Статья Google Scholar
Magnaval JF, Fabre R, Maurières P, Charlet JP, de Larrard B. Применение процедуры вестерн-блоттинга для иммунодиагностики токсокароза человека. Parasitol Res. 1991; 77: 697–702.
PubMed Статья CAS Google Scholar
Yamasaki H, Araki K, Lim PK, Zasmy N, Mak JW, Taib R, Aoki T. Разработка высокоспецифичного рекомбинантного Toxocara canis второй стадии экскреторно-секреторного антигена личинки для иммунодиагностики токсокароза человека .J Clin Microbiol. 2000; 38: 1409–13.
PubMed PubMed Central CAS Google Scholar
Magnaval JF. Сравнительная эффективность диэтилкарбамазина и мебендазола для лечения токсокароза человека. Паразитология. 1995; 110: 529–33.
PubMed Статья Google Scholar
Баррера М.Г., Леонарди Д., Болмаро Р.Э., Эченик К.Г., Оливьери А.С., Саломон С.Дж. и др.Оценка in vivo микросфер альбендазола для лечения мигрирующих личинок Toxocara canis . Eur J Pharm Biopharm. 2010; 75: 451–4.
PubMed Статья CAS Google Scholar
Леонарди Д., Эченик К., Ламас М.С., Саломон С.Дж. Высокая эффективность альбендазола-ПЭГ 6000 в лечении инфекции, вызванной мигрирующей личинкой Toxocara canis . J Antimicrob Chemother. 2009. 64: 375–8.
PubMed Статья CAS Google Scholar
Хориучи А., Сато Т., Акао Н., Койке К., Фудзита К., Никайдо Т. Влияние свободного альбендазола и альбендазола, заключенного в полиэтиленгликоль-липосомы, на подвижность и количество личинок у мышей, инфицированных Toxocara canis . Vet Parasitol. 2005; 129: 83–7.
PubMed Статья CAS Google Scholar
Грчкова Г., Велебный С. Лечение инфекций Toxocara canis у мышей с помощью включенных в липосомы карбаматов бензимидазола и иммуномодулятора глюкана.J Helminthol. 2001; 75: 141–146.
PubMed CAS Google Scholar
Hrckova G, Velebny S, Obwaller A, Auer H, Kogan G. Оценка последующей терапии фенбендазолом, включенным в стабилизированные липосомы, и иммуномодулятор глюкана у мышей, инфицированных личинками Toxocara canis . Acta Trop. 2007. 104: 122–32.
Артикул CAS Google Scholar
Токсокароз — NHS
Токсокароз — редкая инфекция, вызываемая паразитами аскариды.Люди могут заразиться им при обращении с почвой или песком, загрязненными фекалиями инфицированных животных.
Паразиты аскариды чаще всего встречаются у кошек, собак и лисиц и обычно поражают маленьких детей.
Это связано с тем, что дети с большей вероятностью соприкоснутся с зараженной почвой, когда они играют и засовывают руки в рот.
Однако случаи заболевания зарегистрированы у людей всех возрастов.
Признаки и симптомы
У большинства людей заражение этими личинками круглых червей не вызывает никаких симптомов, и паразиты умирают в течение нескольких месяцев.
Однако у некоторых людей наблюдаются легкие симптомы, например:
В редких случаях личинки аскариды поражают такие органы, как печень, легкие, глаза или мозг, и вызывают серьезные симптомы, например:
- усталость
- потеря аппетита или похудание
- Кожные высыпания
- хрипы или затрудненное дыхание
- изъятий (припадков)
- нечеткое или нечеткое зрение, обычно поражающее только один глаз
- очень красный и болезненный глаз
Когда обращаться к GP
Обратитесь к терапевту как можно скорее, если вы считаете, что у вас или вашего ребенка есть симптомы, которые могут быть вызваны токсокарозом.
Если один из ваших глаз поражен токсокарозом, существует риск необратимой потери зрения. Однако своевременное лечение может снизить вероятность этого.
Обычно токсокароз можно обнаружить с помощью анализа крови, хотя при поражении глаз может потребоваться проверка зрения на наличие паразитов.
Почему это происходит
Паразиты аскариды, вызывающие токсокароз (называемые токсокарами), обитают в пищеварительной системе собак, кошек и лисиц.Черви производят яйца, которые выделяются с фекалиями инфицированных животных и загрязняют почву.
Яйца становятся заразными только через 10–21 день, поэтому свежие фекалии животных не представляют непосредственной опасности. Однако, как только яйца попадут в песок или почву, они могут выжить в течение многих месяцев.
Люди могут заразиться, если зараженная почва попадет им в рот. Как только яйца попадают в человеческое тело, они попадают в кишечник, прежде чем вылупятся и выпустят личинки (самая ранняя стадия развития).Эти личинки могут путешествовать по большинству частей тела.
Однако, поскольку люди не являются нормальным хозяином для этих личинок, они не могут развиваться дальше этой стадии и производить яйца. Это означает, что инфекция не может передаваться между людьми.
Снижение риска
Лучший способ снизить вероятность развития токсокароза — соблюдать гигиену.
Например, мытье рук теплой водой с мылом после контакта с домашними животными или контакта с песком или почвой.
Если у вас есть домашняя кошка или собака, их следует регулярно очищать от глистов, а их фекалии следует немедленно утилизировать.
Подробнее о профилактике токсокароза.
Как лечить
Если у вас нет симптомов или симптомы легкие, лечение обычно не требуется.
Однако вам понадобятся лекарства, если у вас серьезная инфекция, поражающая ваши органы. Для уничтожения личинок паразита используется лекарство, называемое глистогонным.
Чаще всего используется альбендазол, альтернативой является мебендазол.
Эти лекарства обычно не вызывают побочных эффектов, хотя у некоторых людей могут возникать головные боли или боли в животе.
Помимо глистогонных средств, часто назначают стероидные препараты (кортикостероиды), чтобы уменьшить воспаление, вызванное тяжелой инфекцией.
Если токсокароз поражает глаз, вместо глистогонных средств используются стероидные препараты. Также может потребоваться операция — например, при отслоении сетчатки.
Большинство людей полностью выздоравливают и не испытывают никаких долгосрочных осложнений. Однако существует риск необратимой потери зрения при поражении одного из глаз.
Подробнее о лечении токсокароза.
Насколько распространен токсокароз?
Токсокароз редко встречается в Великобритании, хотя трудно точно определить, сколько случаев происходит ежегодно, поскольку заболевание часто диагностируется неправильно или недиагностируется.
